N-(3-этиладамантил-1)-этилкарбамат, обладающий противовирусной активностью, и способ его получения
Похожие патенты | МПК / Метки | Текст | Заявка | Код ссылки
Текст
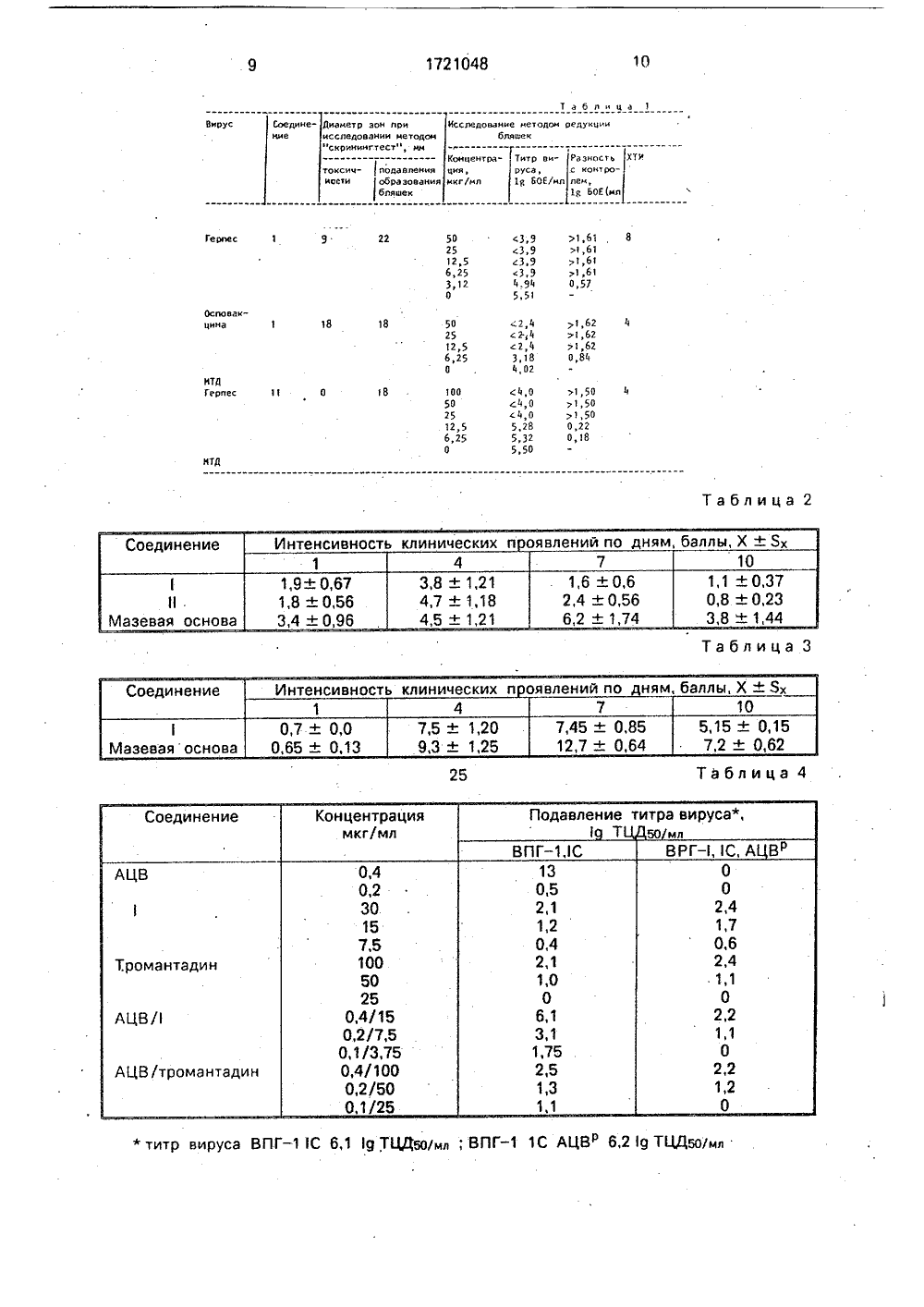
(9) ОП БРЕТЕНИЯ АНИ ЕЛЬСТВУ ОМУ СВ АВ итут чно ого ла- КоЛ,С,нко гов,омитение относится к инениям адамантак М-(3-этиладаман к способу его полуил адам антил-эт новым химнового рятил)-этчения.илкарбам Изобре ческим саед конкретно карбамату и 1-(3-Эт формулыи- а,ат ГОСУДАРСТВЕННЫЙ КОМИТЕТПО ИЗОБРЕТЕНИЯМ И ОТКРЫТИЯМПРИ ГКНТ СССР(71) Самарский политехнический инстим. В,В. Куйбышева, Белорусскйй науисследовательский институт эпидемигии и микробиологии, Минсгосударственный медицинский институтИнститут вирусологии им, Д.И, Ивановс(56) Аггпе п)пе 1 Тогзсй, 1973, 23, М 5, с,АгсЬ РЬаггп, 1975, 308 М 10, с, 348.Патент Франции М 1588472,кл. С 07 С, 1950.Агге а Тогзс, 1973, 23, М 24, с, 5Патент Франции М 2224446, кл. С 07 С 103/19,1)5 С 07 С 269/06, 271/24. А 61 К 31/ Соп 1 аст Оегп)абаз, 1984, 10, М 5, с. 317. (54) М-(3-ЭТИЛАДАМАНТИЛ)-ЭТИЛ КАРБАМАТ, ОБЛАДАЮЩИЙ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ(57) Изобретение относится.к замещенным карбаматам, в частности к получению И-(3- этиладамантил)этилкарбамата, обладающего антивирусной активностью, что может быть использовано в медицине, Цель - создание нового .более активного вещества указанного класса, Синтез ведут смешиванием эмульсии 1-этиладамантана с СНзС(О)ОН и НИОЗ при массовом соотношении 1:(1 - 1,5):(3,5 - 4,5) с последующим добавлением этилового эфира карбаминовой кислоты при 50 - 100 С, Выход 950, т, кип.173 - 174 С (11 мм рт.ст,), П д = 1,4998, противовирусная активность выше действия известного тромантадина в 2 раза в отношении вирусов герпеса и обладает активностью против вирусов осповакцины и аденовирусов З-типа, 2 с.п. ф-лы, 4 табл,обладает противовируснои активностью в отношении вирусов герпеса, осповакцины и аденовирусов и лечебным эффектом при а экспериментальном герпетическом кератоконъюнктивите лабораторных животных. Данное соединение, его свойства и способ получения в литературе не описаны.Известны соединения адамантанового ряда, обладающие противогерпетическим действием: эфиры адамантилгидроксиламина с этоксиуксусной и М-диметиламиноэтоксиуксусной кислотами; производные40 45 50 адамантилтиомочевины; диалкиладамантандикарбаматы.Однако в результате недостаточно высокой противогерпетической активности и сложности методов получения указанные соединения не применяют в качестве средств для лечения герпетических инфекций.В медицинской практике за рубежом широко применяют для лечения заболеваний герпетической природы эффективный препарат адамантанового ряда - тромантадин - гидрохлорид 1-(1-адамантил)-2 Я 2-диметиламино)этоксиа цетамида,Тромантадин обладает сходным с данным соединением механизмом противогерпетического действия.Однако тромантадин обладает целым рядом существенных недостатков;.недостаточная высокая противогерпетическая активность, отсутствие вирусингибирующего действия на вирус осповакцины и аденовирусы, сложная и многостадийная технология получения (из адамантана - шесть технологических стадий).Существуют данные о возможности аллергических дерматитов, вызываемых тромантадином.Все это обусловливает необходимость поиска новых, более эффективных противогерпетических препаратов адамантанового ряда.Наиболее близким к предлагаемому является способ получения 1-адамантилзамещенных карбаматов, заключающийся во взаимодействии адамантановых углеводородов с 10 - 25-кратным моля рным избытком азотной кислоты с последующим добавлением в реакционную смесь эфиров карбаминовой кислоты (4-кратный молярный избыток) при температуре не выше 30 С и выдержкой в течение 1 ч.Выход составляет 59-84 ,Известный способ обладает следующими недостатками: недостаточно высоким выходом целевых продуктов и взрывоопасностью реакционной массы.В случае адамантана оптимальным с точки зрения детонационной способности является молярное соотношение адамантан: азотная кислота 1:11 по уравнению С 10 Н 16.+ 11 НМОз = 10 СО 2+ 5,5 Ы 2+ 13 Н 20. Таким образом, на первой стадии процесса образуется взрывчатая смесь. Высокая концентрация окислов азота в реакционной массе приводит к резкому тепло- и газовыделению при добавлении эфира карбаминовой кислоты за счет реакции нит 10 15 20 25 30 35 розирования, что усложняет технологическое оформление процесса; в продуктах реакции присутствует трудноотделяемая примесь - нитрат соответствующего адамантанола (до 3 - 5), так как известно, что в среде азотной кислоты происходит замещение уретановой (карбаматной) группы на нитратную. Все органические нитраты теримчески нестабильны, Таким образом, снижается стабильность целевых продуктов при хранении,Цель изобретения - получение нового соединения, обладающего более высоким противовирусным действием М-(3-этиладамантил)этилкарбамата и синтез его с высоким выходом по простой технологии.Согласно изобретению М-(3-этиладамантил)этилкарбамат получают взаимодействием эмул ьси и 1-этил адаманта на в уксусной кислоте с азотной кислотой в массовом отношении 1;1,0 - 1,5:3,5 - 4;5 соответственно, и далее с этиловым эфиром карбаминовой кислоты при нагревании при температуре 50 - 100 С и выделением целевого продукта.Использование уксусной кислоты как специфического растворителя при взаимодействии этиладамантана с азотной кислотой приводит к тому, что устраняется взрывоопасность реакционной смеси за счет резкого изменения стехиометрического отношения (для окисления уксусной кислоты до углекислого газа и воды также необходима азотная кислота); увеличивается выход целевого продукта (до 89 - 95 ) за счет снижения кислотности реакционной среды и, следовательно, повышения устойчивости образующегося карбамата, а также по причине более высокой регио- и хемоселективности реакции в мягких условиях(разбавление). Снижение количества уксусной кислоты приводит к утрате указанных преимуществ, Увеличение ее избытка экономически неоправданно. При уменьшении количества азотной кислоты ниже указанных пределов в реакционной смеси остается исходн ым 1-атил адаманта н. Снижение температуры ниже 50 С резко замедляет скорость реакции, и выход целевого продукта падает. Верхний температурный предел обусловлен точкой кипения реакционной массы,Положительный эффект изобретения заключается в получении й-(3-этиладамантал)этилкарбамата, обладающего более высокой активностью и широким спектром противовирусного действия, чем соединение, близкое по структуре и применению, тромантадин, а также в повышении выходаи обеспечении безопасной технологии получения данного соединения.П р и м е р 1. К эмульсии 20 мл(18,7 г)1-этиладамантана в 18,5 мл уксусной кислоты при температуре не более 30 С добавляют 43. мл (65 г) 96 - 100-ной азотнойкислоты, выдерживают 1 ч при 25-30 С идобавляют 50 г этилового эфира карбаминовой кислоты, следя за тем, чтобы температура не превышала 30 С, выдерживают 0,5 ч 10при 100 С и выливают в ледяную воду. Выпавшее масло экстрагируют гексаном, промывают 5 -ным раствором карбонатанатрия, водой, сушат б/в сульфатом натрия.Гексан отгоняют и остаток перегоняют в вакууме.Выход 26,2 г (92), т. кип. 173174 С/11 мм, по = 1,4998, В = 0,58(хлороформ),ИК-спектр ( Р, см "); 3385, 3010, 1710, 201520, 1290, 1220, 1045. Спектр ПМР (д, м,д.):0,69 г(ЗН); 0,86 - 2,16 м (19 Н); 3,86 к(2 Н); 6,53с (1 Н).Найдено,: й 5,40С 15 Н 25 М 02 ,25Вычислено, : М 5,58.П р и м е р 2. К эмульсии 20 мл (18,7 г)1-этиладамантана в 28 мл ледяной уксуснойкислоты при температуре не более 30 С добавляют 56 мл (84 г) 96 - 100-ной азотной 30кислоты, выдерживают 15 мин при 25 - 30 Си добавляют 65 г этилового эфира карбаминовой кислоты, выдерживают 3 ч при 50 С ивыливают в воду. ВыдеЛение целевого продукта аналогично примеру 1. Выход 25,4 г 35(89 ). Физико-химические характеристикиидентичны примеру 1,П р и м е р 3. К эмульсии 20 мл(18.7 г)1-этиладамантана в 25 мл уксусной кислотыпри 25 - 30 С добавляют 50 мл (75 г) 96- 40100 -ной азотной кислоты, выдерживают0,5 ч при 25 - 30 С и добавляют при 20-30 С60 г этилового эфира карбаминовой кислоты. Выдерживают 1 ч при 75 С и выливаютв воду, Выход 27,1 г (95 ). Выделение и 45физико-химические свойства аналогичныпримеру 1.Влияние соотношения реагентов на выход продукта.Нижние значения. К эмульсии 20 мл 50(18,7 г) 1-этиладамантана в 18,5 мл ледянойуксусной кислоты при температуре не более20 С добавляют 43 мл (65 г) 96 .-ной азотной кислоты, выдерживают 0,5 ч при 20 -25 С и при 25-30 С добавляют 50 г 55этилового эфира карбаминовой кислоты,выдерживают 0,5 ч при 50 С и выливают вводу. После экстракции гексаном, отгонки растворителя и перегонки в вакууме получают 25,7 г (90) целевого продукта,Средние значения. К эмульсии 20 мл(18,7 г) 1-этиладамантана в 23 мл ледянойуксусной кислоты при 20 - 25 С добавляют50 мл (75 г) 98 ф-ной азотной кислоты, выдерживают 1 ч при 25 С и при 25-30 С добавляютт 60 г этилового эфира карбами новойкислоты, выдерживают 45 мин при 70 - 75" Си выливают в воду. После выделения выход25,9 г(91).Верхние значения. К эмульсии 20 мл(18,7 г) 1-этиладамантана в 28 мл ледянойуксусной кислоты при 25 С добавляют 56 мл(84 г) 100;-ной азотной кислоты, выдерживают 1 ч и при 25 - 30 С добавляют 70 г этилового эфира карбаминовой кислоты,выдерживают 1 ч при 100 С и выливают вводу. После выделения выход 26,2 г (92 ),При этом получить целевой продукт безиспользования уксусной кислоты невозможно, а при проведении процесса при комнатной температуре продукт получают только свыходом 45,9 ,й-(3-Этиладамантил)этилкарбамат -бесцветная вязкая жидкость с легким желтоватым оттенком, хорошо растворимая вгексане, вазелиновом масле, бензоле, хлороформе,ацетоне, спирте,диметилсульфоксиде, устойчивая на свету и при длительномхранении,Биологические испытания данного соединения показывают, что оно обладает выраженным антивирусным действием вотношении вирусов герпеса, превосходящим в 2 раза действие известного противовирусного соединения тромантадин, атакже противовирусной активностью против вирусов осповакцины и аденовирусовЗ-типа,й -(3-Э тил адама н т ил) этил кар ба маттакже обладает лечебным эффектом приэкспериментальном герпетическом кератоконъюнктивите лабораторных животных(морские свинки, кролики).При проведении испытаний использованы тканевые культуры первично-трипсинизированных фибробластов эмбрионов кури клеток почки эмбрионов человека, вирусыгерпеса простого 1-типа(Штаммы 1 С и "Коптев"),Токсические свойства й-(3-этиладамантил)этилкарбамата исследованы на указанных культурах, Данное соединениеявляется малотоксичным соединением.Максимальная толерантная концентрация50 мкг/мл.ЮБо = 1830 мг/кг, для тромантадинаЦ)ио = 71 кг/кг (на мышах).Определен химиотерапевтический индекс (ХТИ) как отношение максимальной толерантной концентрации к минимальноактивной концентрации (МТД/МАК),Установлено, что данное соединение 5обладает выраженной способностью подавлять размножение вирусов герпеса и осповакцины в тканевой культуре,В табл. 1 показаны результаты игибирования размножения вирусов в 10фибробластах эмбрионов кур й-(3-этиладамантил)этилкарбамата (1) и тромантадина (11),При этом ХТИ М-этиладамантилэтилкарбамата в 2 раза выше, чем у.тромантадина. Кроме того, в экспериментах наклетках почки эмбрионов человека установлено; что М-(3-этиладамантил)-этилкарбамат подавляет развитие цитопатическогоэффекта аденовируса на 75в концентрации, соответствующей. МТД или 1/2 от нее,В экспериментах на животных данноесоединение применяют в виде 1-ной мазина стандартной глазной основе аптечногоприготовления с ежедневным 2 - 4-кратным 25закладыванием мази, В экспериментах наморских свинках применение мази М-(3-атил адама нтил)-этил ка рба мата обес печи ваетболее быструю регрессию всей суммы клинических признаков герпетического кератоконъюнктивита в сравнении с эффектом1 ,-ной мази тромантадина.В табл. 2 показаны результаты влияния1 /-ных мазей й-(3-этиладамантил)-этилкарбаматаи тромантадина (Н) на лечение 35экспериментального герпетического хератоконъюнктивита морских свинок,Противогерпетическая эффективностьИ-(3-этиладамантил)-этилкарбамата подтверждена также в экспериментах на краликах,В табл. 3 показаны результаты влиянияК-(3-этиладамантил)-этилкарбамата (1) натечение экспериментального герпетического кератоконъюнктивита кроликов, 45Выраженный ингибирующий эффектпредлагаемого соединения сохраняет приинфицировании клеток Чего вирусом герпеса 1-типа, устойчивым к ацикловиру, (АЦВ)препарату нуклеозидной природы. 50В табл, 4 показаны результаты ингибирования репродукции ВПГ(штаммы 1 С,АЦВР) данным соединением , тромантадином, ацикловиром и их сочетаний.Если при использовании ацикловира в 55отношении штамма вируса ВПГ, 1 С АЦВРне обнаружено снижения титра вируса, тосоединение в дозах 30 и 15 мкгlмл подавляет репродукцию вируса на 2,4 и 1,7 у ТОДБО/мл соответственно,Использование низких концентраций (практически не оказывающих влияния на ВПГ) й-(3-этиладамантила)-этилкарбамата и цикловира приводит к выраженному синергидному антигерпетическому действию,Комбинация тромантадина с ацикловиром показывает аддитивный эффект в отношении ВПГ,Таким образом, предлагаемое соединение Й-(3-этиладамантил)-этилкарбамат обладает выраженными п ротивовирусными свойствами, проявляя активность в отношении вирусов герпеса, осповакцины и аденовируса, высокоэффективно в отношении штамма вируса герпеса, резистентного к действию известного препарата цикловира, Полученное соединение имеет выраженный синергидный эффект в сочетании с ацикловиром,Таким образом, новое производное адамантана представляет собой перспективное действующее начало для разработки высокоэффективной формы нового противовирусного препарата с широким спектром действия. Формула изобретения 1, М-(3-Этиладамантил)-этилкарбамат формулы С,ИИНСООСрН обладающий противовирусной активностью.2. Способ получения М-(3-этиладамантил)-этилкарбамата формулыИНСООСН от л и ч а ю щ и й с я тем, что к эмульсии 1-этиладамантана в уксусной кислоте добавляют азотную кислоту при массовом соотношении 1:1,0 - 1,5;3,5 - 4,5 соответственно с последующим добавлением этилового эфира карбаминовой кислоты и нагревании при температуре 50 - 100 С и выделением целевого продукта,1721048 Таблица 1 Еоедине- Диаметр зон приние исследовании методомискринингтест", им В рус Исследование нетодом редукции бляшек Титр еи- Разность руса, с контро В БОЕ/мл лем,1 О БОЕ(мл ХТИ Концентра"ция,мкгlмл подавленияобраэоеаниябляшек токсичности Герпес 1 9 22 Оспоеакцина 1 18 18 НТДГерпес 18 11 О НТД Таблица 2 Таблица 3 Таблица 4 25 титр вируса ВПГ - 11 С 6,1 1 ЯТЦЦ 50/мл, ВПГ1 С А МЛ 50 25 12,5 6,25 3,12 0 50 25 12,5 6,25 0 100502512,56,250 с 3,9 с 3,9 с 3,9 с 3,9 4 94 5,51 с 2,4 с 2,4 с 2,4 3, 18 4,02 с 4,0 с 4,0 с 4,0 5,28 5,50
СмотретьЗаявка
4813502, 26.02.1990
САМАРСКИЙ ПОЛИТЕХНИЧЕСКИЙ ИНСТИТУТ ИМ. В. В. КУЙБЫШЕВА, БЕЛОРУССКИЙ НАУЧНО-ИССЛЕДОВАТЕЛЬСКИЙ ИНСТИТУТ ЭПИДЕМИОЛОГИИ И МИКРОБИОЛОГИИ, МИНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ ИНСТИТУТ, ИНСТИТУТ ВИРУСОЛОГИИ ИМ. Д. И. ИВАНОВСКОГО АМН СССР
КЛИМОЧКИН ЮРИЙ НИКОЛАЕВИЧ, МОИСЕЕВ ИГОРЬ КОНСТАНТИНОВИЧ, ВЛАДЫКО ГАЛИНА ВИКЕНТЬЕВНА, АНДРЕЕВА ОЛЬГА ТРИФОНОВНА, БОРЕКО ЕВГЕНИЙ ИВАНОВИЧ, КОРОБЧЕНКО ЛЮДМИЛА ВИКТОРОВНА, ВОТЯКОВ ВЕНИАМИН ИОСИФОВИЧ, РУСЯЕВ ВЯЧЕСЛАВ АНАТОЛЬЕВИЧ, ФЕЙГИН ЛЕОНИД СЕМЕНОВИЧ, НИКОЛАЕВА СВЕТЛАНА НИКОЛАЕВНА, ВЕРВЕТЧЕНКО СВЕТЛАНА ГРИГОРЬЕВНА, КАЗИНЕЦ ОЛЬГА НИКОЛАЕВНА, БЕРЛОВ ГЕРМАН АЛЕКСАНДРОВИЧ, ГАЛЕГОВ ГЕОРГИЙ АРТЕМЬЕВИЧ, ПРАВДИНА НАТАЛИЯ ФЕДОРОВНА, ШОБУХОВ ВАДИМ МАКСИМОВИЧ, КОЛОМИЕЦ АНАТОЛИЙ ГАВРИЛОВИЧ, РЫТИК ПЕТР ГРИГОРЬЕВИЧ, ПЕНКЕ ИЛМАР ХАРЬЕВИЧ
МПК / Метки
МПК: A61K 31/27, C07C 269/06, C07C 271/24
Метки: n-(3-этиладамантил-1)-этилкарбамат, активностью, обладающий, противовирусной
Опубликовано: 23.03.1992
Код ссылки
<a href="https://patents.su/5-1721048-n-3-ehtiladamantil-1-ehtilkarbamat-obladayushhijj-protivovirusnojj-aktivnostyu-i-sposob-ego-polucheniya.html" target="_blank" rel="follow" title="База патентов СССР">N-(3-этиладамантил-1)-этилкарбамат, обладающий противовирусной активностью, и способ его получения</a>
Предыдущий патент: Способ получения гидрохлоридов (-) -арил аминомасляных кислот
Следующий патент: Способ получения диметилсульфоксида-д
Случайный патент: Диффузионный вакуумный насос