2, 6-диметил-3, 5-бис-(1-адамантилоксикарбонил)-4-(2 дифторметоксифенил)-1, 4-дигидропиридин, обладающий антиангинальным действием
Похожие патенты | МПК / Метки | Текст | Заявка | Код ссылки
Текст
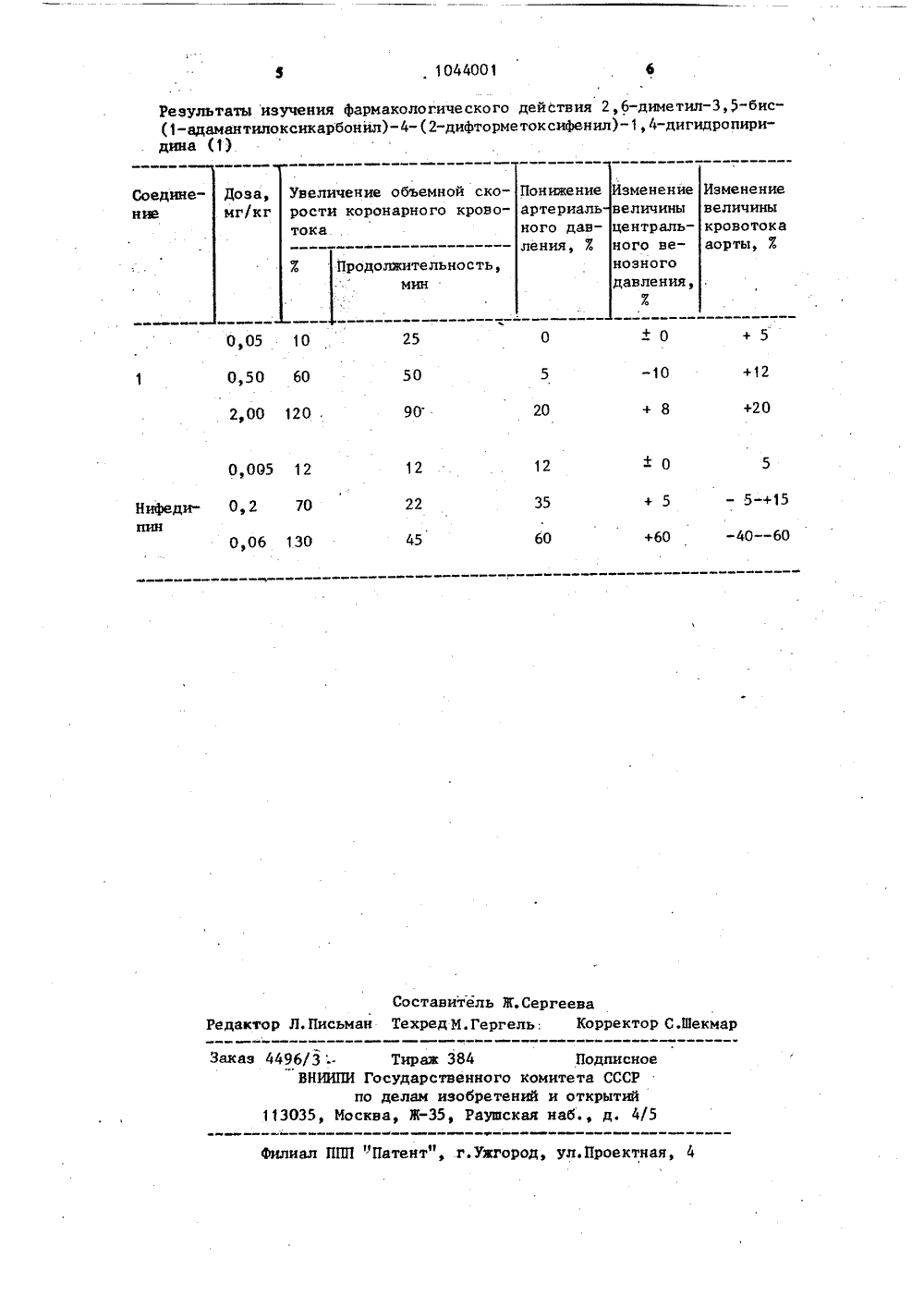
(9) ( ГОСУДАРСТВЕННЫЙ КОМИТЕТ СССРПО ДЕЛАМ ИЗОбРЕТЕНИЙ И ОТНРЫТИЙ 4(511 С 07 Р 211/86, А 61 К 31/44 ПИСАН ИЗОБРЕ ИДЕТЕЛЬСТВУ НИЯ(71) Ордена Трудового Крмени институт органическАН Латвийской ССР(53) 547.822.3(088.8) в коваасного Зцаого синтеза 0 НССНВТОРСКОМУ СВ ТИЛ,5-БИС- (1-АДАМАННИЛ) -4- (2-ДИФТОРМЕТОКСИГИДРОПИРИДИН, ОБЛАДАЮЩИЙ НЫМ ДЕЙСТВИЕМе тил, 5-бис- (1-аг аманнил)-4-(2-дифторметоксиигидропиридин формулы: Н ладающий антиангинальным действи1044 ОО 1 1 О ООССОО н,ссн,15 Изобретение относится к новому химическому соединению, конкретно к 2,6-диметил,5-бис-(1-адамантилоксикарбонил)-4-(2-дифторметоксифенил)-1,4-дигидропиридину формулы Нобладающему антиангинальным действием.Это соединение может найти применение в медицине.Известен 2, 6-диме тил- о - нитрофенил,5-диметоксикарбонил,4-дигид ропиридин (препарат нифедипин), близкий по структуре и по спектру фарма-. кологического действия .Недостатками нифедипина являются высокая токсичность (Ы р 190 мг/кг),25 нестабильность на свету, а также вызываемые им побочные эффекты .(резкое понижение давления, тахикардия).Наиболее близкое по структуре соеДинение -2,б-диметил,5-бис О (1 - адамантилоксикарбонил)-1,4-дигид - ропиридин обладает радиозашитной активностьюЦелью изобретения является расширение арсенала средств воздействия на живой организм, а также снижение токсичности и устранение побочных эффектов.Цель достигается описываемым 2,6-диметил,5 в б-(1 - адамантилокси-Ао карбонил)-4-(2-дифторметоксифенил) - 1,4-дигидропиридином приведенной формулы, обладающим антиангинальным действ ием.Указанное соединение получают конденсацией 1-адамантилового эфира ацетоуксусной кислоты, о-дифторметоксибензальдегида и аммиака в органическом растворителе (этанол, диоксан, метанол) или конденсацией 1-адамантилового эфира Д -аминокротоновой кислоты и о -дифторметоксибензальдегида. Исходные 1-адамантиловые эфиры 55 ацетоуксусной кислоты и 3 -аминокротоновой кислоты получают по известной методике. 2П р и м е р. А. 23 5 г (О 1 моль)1-адамантилового эфира /3-аминокротоновой кислоты и 8,6 г (0,05 моль)0-дифторметоксибензальдегида растворяют в 50 мл этанола и кипятят в течение 7 ч. После охлаждения оставляют на 1 день, фильтруют выпавшийосадок, высушивают при комнатнойтемпературе. Получают 15, 2 г (507)светло-желтого кристаллического вещеоства, т.пл, 126-128 С (из этанола).Найдено, 7: С 70,8; Н 7,2;11 2,2.СН 110, Г,Вычислено,%: С 71, 15; Н 7, 13;11 2,3.Спектр ПМР в СБС 1, 8 . 1,60 (с.,12 Н, 6 -Н-адамантилрадикала), 1,972,08 (м 18 Н, -Н и-Н в адамантилрадикала), 2,18 (с., 6 Н, 2,6 - СН),5,07 (с., 1 Н, 4-Н), 5,.63 (с 1 Н, ИН),6,39 (т., 1 Н, 7=78 Гц, ОС 11 Г),6,95-7,38 м.д. (м., 4 Н, -СНд-).УФ - спектр в этаноле, б маркс, (1 Я):(3,82) .Б. 16,4 г (0,07 моль) 1-адамантилового эфира ацетоуксусной кислоты,5, 4 г (0,035 моль) о -дифторметоксибензальдегида и 7,0 г (0,1 моль)253-ного водного аммиака растворяютв 25 мл этанола и кипятят в течениеб ч. После охлаждения выделяют 9,3 г(457) светло-желтого кристаллическоого вещества, т.пл. 126-128 С (изэтанола),Полученное соединение устойчивов обычных условиях хранения,Исследование действия 2,6-диметил 3,5-бис-(1 - адамантилоксикарбонил) в 4(2-дифторметоксифенил)-1,4-дигидропиридина (1) иа сердечно-сосудистуюсистему проведено в опытах на кошках,крысах и мышах. Изучено его специфическое (антиангинальное и гипотензивное) действие и острая токсичность, Для сравнения использовалиизвестное гипотензивное и антиангинальное средство - нифедипин,а также нитроглицерин,В опытах на наркотизированныхкошках (90 мг/кг глюко-хпоралозывнутрибрюшинно) установлено, что соединение 1 обладает выраженным коронародилатирующим действием, но поактивности несколько уступает нифедипину, Однако в эквиактивных дозахоно действует в два раза более длительно. В отличие от нифедипина соединение 1 оказывает положительный эффект на коронарное кровообращение в большом диапазоне доз (0,05- 3 мг/кг), не вызывая нежелательных эффектов - резкого падения артериального давления, выраженного умень- шения артериального кровотока, увеличения центрального венозного давления (см. таблицу).Дополнительные исследования для проверки антиангинального действия показали, что соединение 1 в диапазоне доз 0,1-2,0 мг/кг повышает содержание кислорода в венозной крови, оттекающей из коронарного синуса сердца, что свидетельствует о более экономичной работе сердца.Внутривенное введение его в до- зах 0,1 - 1,0 мг/кг значительно уменьшает, а в нескольких случаях даже полностью предупреждает подъем сег-мента БТ на эпикардиальных отведениях электрокардиограммы от очага ишемии во время наложения сердцу искусственного ритма. При этом эффект от введения соединения 1 почти в два раза более выражен и продолжителен, чем после введения нитро - глицерина в дозе 0,05 мг/кг. Внутри- венное введение нифедипина в дозах 0,01-0,05 мг/кг не вызывало значительного защитного эффекта, а в нескольких случаях, судя по эпикардиальной электрокардиограмме, даже увеличивало степень ишемии в центре очага.В опытах на спонтанно гипертензивных крысах (СГК) при пероральном введении соединения 1 и нифедипина в дозах 10 мг/кг понижение систолического артериального давления через 1 ч после введения составляет 31,5 мм рт. ст. и 51,7 мм рт.ст. соотве тственно, Таким образом, соединение 1 несколько в меньшей степениуменьшает артериальное давление,однако в отличие от нифедипина не вызывает при этом такикардии (см. таблицу) .При изучении острой токсичности 10 установлено, что соединение 1 малотоксично. 1,Рзо соединения 1 при внутрибрюшинном введении белым мьшам8400 мг/кг, в то время как ЕРо нифедипина 190 мг/кг.15 На основании полученных данныхможно выделить ряд преимуществ предлагаемого соединения по сравнениюс известными препаратами: низкаятоксичность (в 44 раза меньше, чем 20 у нифедипина); более широкий диапазон терапевтического действия; положительное влияние на коронарноекровообращение в большем диапазонедоз и более чем в два раза пролои гированное действиепо сравнениюс нифедипином при отсутствии нежелательных эффектов; соединение 1 более эффективно, чем нифедипин и даже нитроглицерин предупреждает ишемические изменения в миокарде причастичной окклюзии коронарной артерии и одновременного наложения сердцу высокого искусственного ритма;соединение 1 в отличие от нифедипинане вызывает тахикардии. Все это указывает на возможностьпрактического использования 2,б-диметил,5-бис-(1-адамантилоксикарбо нил) - 4-(2-дифторметоксифенил)-1,4 дигидропиридина в медицине для лечения ишемической болезни сердца,1044001 Результаты изучения фармакологического действия 2,6-диметил,5-бис(1-адамантилоксикарбонил)-4-(2-дифторметоксифенил)-1,4-дигидропиридина (1) Изменение величины Доза, мг/кг онижение це нтр ального венозно олжительность, мин авления 5+60 0 Составитель Ж.СергееваРедактор Л,Письман ТехредМ.Гергель. Корректор С,Шекмар Заказ 4496/3Тираж 384 Подписно ВНИИПИ Государственного комитета СССР по делам изобретений и открытий 113035, Москва, Ж, Раушская наб., д. 4/Филиал ППП "Патент", г.Ужгород, ул.Проектная Увеличение объемной скорости коронарного кровотока 0,095 12 0,2 70 0,06 130 артериального давления, 7. Изменениевеличиныкровотокааорты, 7
СмотретьЗаявка
3415357, 30.03.1982
ОРДЕНА ТРУДОВОГО КРАСНОГО ЗНАМЕНИ ИНСТИТУТ ОРГАНИЧЕСКОГО СИНТЕЗА АН ЛАТВССР
БИСЕНИЕКС Э. А, ВЕВЕРИС М. М, ДУБУР Г. Я, ПОЛИС Я. Ю, УЛДРИКИС Я. Р, БАРМЕНКОВА Н. В, КИМЕНИС А. А
МПК / Метки
МПК: A61K 31/4422, A61P 9/10, C07D 211/86
Метки: 4-дигидропиридин, 5-бис-(1-адамантилоксикарбонил)-4-(2, 6-диметил-3, антиангинальным, действием, дифторметоксифенил)-1, обладающий
Опубликовано: 30.06.1985
Код ссылки
<a href="https://patents.su/4-1044001-2-6-dimetil-3-5-bis-1-adamantiloksikarbonil-4-2-diftormetoksifenil-1-4-digidropiridin-obladayushhijj-antianginalnym-dejjstviem.html" target="_blank" rel="follow" title="База патентов СССР">2, 6-диметил-3, 5-бис-(1-адамантилоксикарбонил)-4-(2 дифторметоксифенил)-1, 4-дигидропиридин, обладающий антиангинальным действием</a>
Предыдущий патент: Способ фотохимического окисления двуокиси серы
Следующий патент: Способ формирования субмикросекундных импульсов лазерного излучения
Случайный патент: Отстойник для взвешенных смесей