Способ получения пиразолов
Похожие патенты | МПК / Метки | Текст | Заявка | Код ссылки
Номер патента: 645566
Автор: Мюррей
Текст
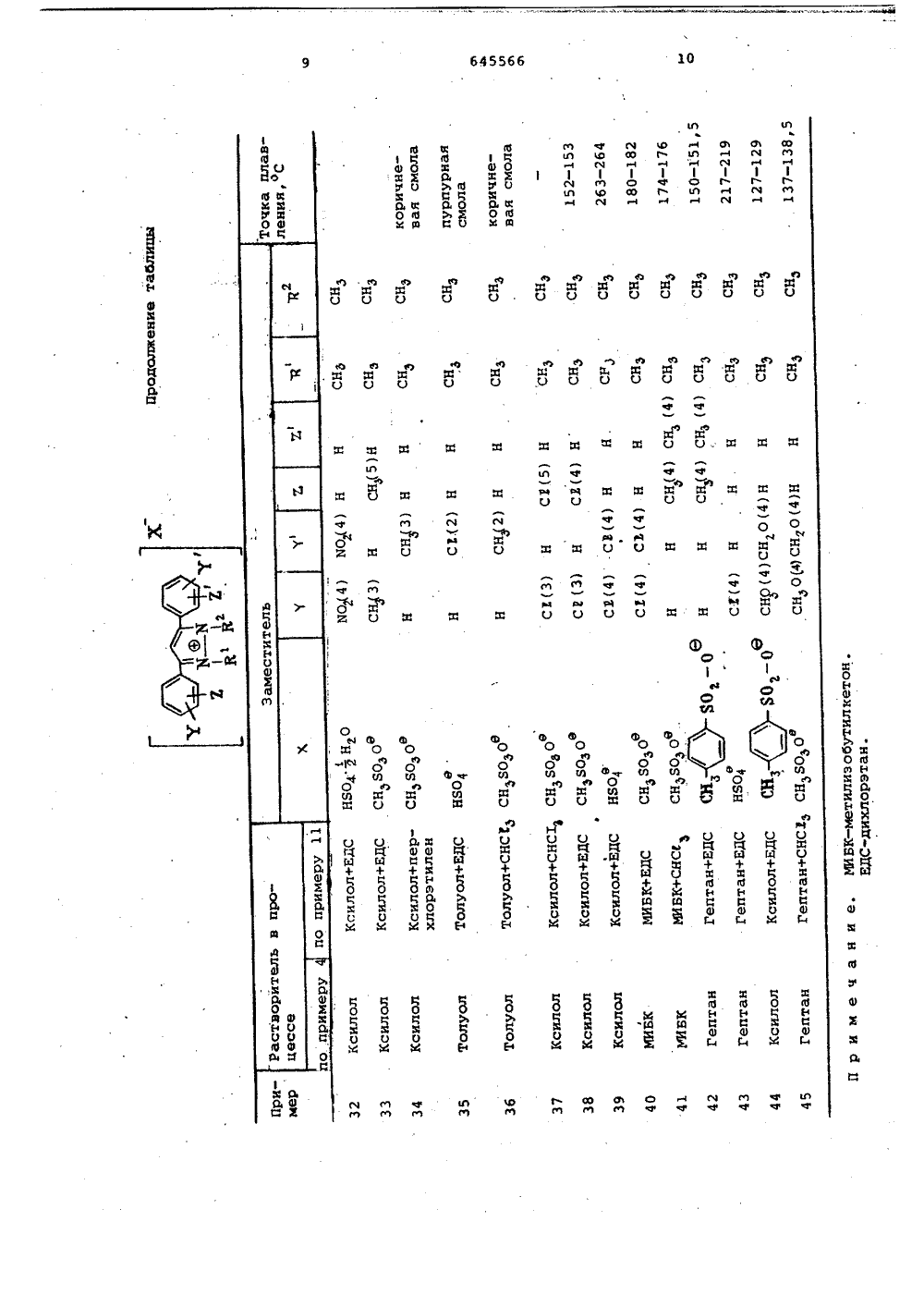
И Е ОП И 1 ц 645566 Союз Советских Социалистических Республик(33) США ииый иоиитСРизобретенийкрытийсуларс лел иЛата опублнк 30.0 17 описан 2) Авт.ор, изобретен Иностранец мюррей Гарбер(США) 1) Заявитель 154) СПОСОБ ПОЛУЧЕНИЯ ПИРАЗОЛО Изобретение отнспособу получения ится к новомураэолов формул Недоста является н продукта,Цель нзобре хода целевого Это достига собом получени заключается в пираэол .Формултком и евысок вестного спосой выход целево тения - повышенпродукта.ется предлагаея пиразолов, котом, что 3,5-диф в мым споорый енил" М - алкил с 1 мами углеро а 12 и Е каждый означает ода, нитрогруппу, галоид, 4 атомами углерода, галоид атомами углерода и с ами или алкоксигруппу, являются промежуточными в синтезе 1,2-диалкил,5- раэолиевых солей, обладаюической. активностью.н способ получения Пираэо" ной обцей формулы, заклютом, что кетон формулы1",Х и Е иалкилируютлента алкили де У, ения, квива ормул ло ча й-3 атомами угльфонат или ф имеет укаостаток ай как хлоульфат, кльфонат,1-4 атомальфон с-толуолсу сульалкил леро- осфат ал идразином в среде растворителяри температуре от 70 до 150 С 1атом водо алкил с 1 алкил с 1 1-4 галоид которые продуктами-дифенилпи щих биолог Известе в указан юцийся вмеют укаэанные знапри помоци 1-1,5рующего агентаалкансульфонат с 1-4 атомами углерода;й 1 - целое число от 1 до 3,в присутствии твердого безводногооснования щелочного металла в безводном инертном органической растворителе при температуре от 80 до 175 С.В качестве основания применяютпреимущественно твердую безводнуюгидроокись" натрия, гидроокись калия, карбонат натрия или карбонаткалия..Процесс проводят преимущественнопри температуре от 85 до 120 С.оВ случае, если М означает метил,У,Ъ,Х и Е каждый означает во дород, то в качестве алкилирующегоагента применяют диметилсульфат и вкачестве растворителя применяют ксилол.,В качестве растворителя применяют"преймущественно ароматический углеводород, алифатический углеводород,высший ароматический растворитель,которые имеют смешанную анилиновуюточку -1 фС и 35 С и содержат ароматического компонента от 60 до 100с удельной плотностью 0,88-1,5 при 60.оС, алифатические кетоны С,(-С, али";фатические спирты С-С 8, дихлор- .Э 1 ИЛЕН, ПЕРХЛОРЭтИЛЕН, ДйПОЛЯРНЫй,апротонный растворитель, простойциклический эфир" и алкоксиалкиловыйпростой эфир.П р и м е р 1, Получение 1-метил,5-дифенйлпйразола.5,0 г (0,023 моль) 3,5-дифенил " пиразола растворяют в 40 мл метилизобутилкетОна. Прибавляют 3,76 г(0,027 моль) твердого безводного карбоната калия и смесь нагревают до90 фС. Прибавляют 3,43 г"диметилсульфата и смесь нагревают 1,5 ч при112-115 С. Через 1,5 ч не оотаетсянепрореагиройавшего. 3,5-дифенилпиразола. РеакциоййУю смесь охлаждают до 50 оС, органическую фазу, содержащую некоторое количество нерастворимьФ "твердых соединений (водораствориМых), промывают 10 мл разбавлен йМб"едкого натра. Органический слойдважды промывают 10 мл воды. Для-3,5-дифенилпираэола.5,0 г (0,023 моль 3,5-дифенилпиразола растворяют в 25 мл метилизобутилкетона. Прибавляют 1,1 г твердой безводной гидроокиси натрия.гидроокиси натрия. Органический слойдважды" промывают 30 мл воды. Для определения выхода удаляют в вакууме метилизобутилкетон и получают 4,95 г6 (выход 93 сырого)масла, котороекристаллизуется при охлаждении втвердый продукт с т.пл. 52-53 С.П р и м е р 3. Получение 1-метил,5-дифенилпираэола10 10,0 г (0,0454 моль) 3,5-дифенилпиразола растворяют в 50 мл ксилола,содержащего 2,62 г (0,0655 моль)твердой безводной гидроокиси натрия.Реакционную смесь нагревают до 110 Со 15 и прибавляют 6,9 г (0,0547 моль) диметилсульфата, смесь нагревают при107-1150 С. После 30 мин кийячения собратным холодильником реакционнуюсмесь охлаждают до 60 С и прибавляют25 мл воды, Устанавливают рН 1011 5 мл 25-ного водного растворагидроокиси натрия. Органический слойдважды промывают 25 мл воды. Для определениявыхода ксилол отгоняют ввакууме и получают 9,65 г масла,кристаллизующегося при посеве(т.пл. 53-56 С). Анализ показывает96,6-ную чистоту продукта. Выходсоставляет 87,5.П р и м е р 4. Получение 1-метил,5-дифенилпиразола.20,0 г (0,0908 моль) 3,5-дифенилпиразола растворяют в 100 мл ксило"ла, содержащего 7,26 г (0,1816 моль)твердой безводной гидроокиси натрия. М Реакционную смесь нагревают до 120 Сои прибавдяют 13,8 г (0,109 моль) диметилсульфата. Кипятят с обратнымхолодильниксм при 95 С и через 15 минв смеси не остаеТся непрореагировав шего 3,5-дифейилниРазола.ЧерезЗОмин реакционную смесь охлаждаютдо 800 С и прибавляют 50 мл воды.Прибавляют 50-ный раствор едкогонатра для установления рН воднойфазы 10-11. Органический слой дваждыпромывают 50 мл воды. Для определейия"выхода Ксилол отгоняют в вакуумеи получают 19,7 г масла, котороекристаллизуется, Анализ показывает98,5-нуФ чистоту продукта. Выход50 составляет 91,6;П р и м е р ы 5-10. Получение1-метил,5-дифенилпираэола, Опытыбеэ использования безводного основания щелочного металла и неводного 55 растворителя приводят в результатек смесям "непрореагировавшего 3,5 дифенилпиразола и 1-метил,5-дифенилпиразола.Процесс проводят по примеру 4.60 Во всех примерах был использован диметилсульфат, но твердую безводнуюгидроокись натрия заменяют на разные основания. В некоторых случаяхксилол заменяют различными раствори- , 65 телями.64 Результаты Приьзер 5 Водная )(аОН (25-ная) в ксилоле в результате приводит кнепрореагировавшему 3,5-дифенилпираэолу.6 Водная ИаОАс (10-ная) вксилоле в результате приводитк непрореагировавшему 3,5-дифенилпираэолу.7 Основания не прибавляют, врезультате получают непрореагировавший 3,5-дифенилпираэол.8 Водный БаНСОприводит в результате к непрореагировавшему 3,5"дифенилпираэолу.9 Водный БаСО приводит в результате к непрореагировавшему 3,5-дифенилпиразолу,10 Метилат натрия при кипячениис обратным холодильником всреде метанола приводит кнепрореагировавшему 3,5-дифеннлпиразолу,П р и м е р 11. Получение 12-диметил,5-дифенилпиразолийметилсуль"фата,1-Метил,5-дифенилпиразол(1,0 моль), полученный по примеру 4,смешанный с ксилолом, разбавляют равным объемом дихлорэтана. Реакцион"ную смесь нагревают до 50 - 55 С иоприбавляют эквимолекулярное количест"во или небольшой избыток (1,05 моль)диметилсульата. Смесь нагреваютпри 105-110 С в течение 4 ч. Затемреакционную смесь охлаждают до 15 Си продукт, выпавший в осадок, отфильтровывают. Влажный осадок нафильтре промывают ксилолом, затемацетоном и сушат.Выход продукта составляет 93,Повторяют указанный процесс, нопосле алкилирования смесь охлаждаютдо 50 С и прибавляют к ней небольшоеколичество триэтиламина, смесь нагревают при 50 фС в течение 30 мин иохлаждают. В этой реакции разрушаютизбыточное количестьо диметилсульфата, что увеличивает безопасностьработы. Выход продукта составляет90-92,Указанную реакцию алкилированияповторяют, заменив триэтиламин напиридин и получают те же результаты.П р и м е р 12. Получение 1,2-диметил,5-дифенилпиразолийметилсульфата.1-метил,5-днфенилпиразол(1,0 моль) получают по примеру 4,но удаляют ксилол. Реакционнуй смесьнагревают до 60 С и прибавляют 5566 61,05 моль диметилсульфата, затемсмесь нагревают до 105-110 Си выдерживают при этой температуре 8 ч.Смесь охлаждают до комнатной температуры, затем отфильтровывают выпав.ший в осадок продукт, промывают кси-лолом, затем ацетоном и сушат.Выход продукта составляет 83.Повторяют укаэанную реакцию, нопосле алкилирования к реакционнойсмеси прибавляют при 50 С триэтилфамин, смесь нагревают 30 мин при10 этой температуре для удаления избытка диметилсульфата. Выход продуктане меняется,При замене в реакции алКилированиятриэтиламина на пиридин и триметиламин получают хорошие результаты,П р и м е р 13, Получение 1,2-диметил,5-дифенилпираэолийметилсульФата.,1-Метил,5-дифенилпиразол(1,0 моль) получают по примеру 4, ноне удаляют ксилол, использованный впримере 4. Около 75 ксилола теперьотгоняют и прибавляют дихлорэтан вколичестве, эквивалентном количествуксилола, оставшегося в реакционной25 смеси Охлаждают реакционную смесьдо 60 С и затем прибавляют 1,05 моль6диметилсульфата, смесь нагревают до105-110 фС и выдерживают при этойтемпературе 4 ч. Смесь охлаждают до30 50 ОС и прибавляют триэтиламин в ко"личестве, равном 8 мол. от использованного диметилсульфата. Реакционную смесь перемешивают 30,мин при,50"С, Затем реакционную смесь охлажЗ 5 дают до комнатной температуры ифильтруют. Влажный осадок на фильтрепромывают ксилолом, затем ацетономи продукт сушат.Выход продукта составляет 90-92.П р и м е р 14. Получение 1,240.45 фпол чают 1-алкил,5-дифенил (заме"щенный или незамещенный) пиразол.Затем полученное такиМ образом соединение превращают в пираэолиевуюсоль общей Формулы 1 по примерам11 и 12 или 13, применяя выбранный"0 растворитель или смесь растворителей,приведенных в таблице.Выходы продуктов обычно находятсяв интервале 78-83, когда используютодин растворитель в окончательномалкилировании, в то время как, ис-пользуя систему растворителей в окончательном алкилировании, достигаютвыходов на 5-10 выше.6455 бб О1 въ юэ сб Ю х х х х х х О О О О О О Юф йфЭ х х о о х о х" о х" о х х о о хж о оЮ Ф иЙ х во р, х И ю о И Ц Я ао а и ою ио ыщ м Р М Ю .1 СЧ 1 1 сч м ОЪ 0 т 1 (Ч12 6455 бб 4 атомами углероВ - алкил где да;У, водоро кил с кил с лоидам ч а ю повыш 3,5-д Составитель Т. Якунинаольская Техоед И. Асталош КорректТираж 512 ПодписиНИИПИ Государственного комитета СССРпо делам изобретений-и открытий35 Москва ИРаушская наб. д. ор Л, Веселовское4 5 едактор Т. Ни Заказ 385/ 1 П Патентф, г. Ужгород, ул, Проектная филиал П формула изобретения 1, Способ получения пиразолов формулы 2 и Е каждый означает атом да, нитрогруппу, галоид, ал 1-4 атомами углерода, галоидал-4 атомами углерода и с 1-4 гаи или алкоксигруппу, о т л и- щ и й с я тем, что, с целью, ния выхода целевого продукта, фенилпираэол формулы 2Н где У, У, Е и Е имеют указанные эна 1чения, алкилируют при помощи 1-1,5 эквивалента алкилирующего агентаформулы гдеЙ -" имеетуказанное -"значение;О - остаток алкилирующего агентЪ, такой как хлорид, бромид или йодид, сульфат, кислый сульфат, бен"эолсульфонат, алкоксибенэолсульфонат с 1-4 атомами углерода, алкилбензолсульфон с 1-3 атомами углерода, и -толуолсульфонат или фосфат,алкансульфонат с 1-4 атомамн углерода;щ - целое число с 1 до 3,в присутствии твердого безводногооснования щелочного металла в безводном инертном органическом растворителе при температуре от 80 до 175 С2, Способ по п.1, о т л и ч а ющ и й с я тем, что в качестве основания применяют твердую безводнуюгидроокись натрия, гидроокись калия,карбонат натрия или карбонат калия.3, Способ по п.1, о т л и ч а ющ и й с я тем, что процесс проводят при температуре от 85 до 120 фС.4. Способ по п.1, о т л и ч а ющ и й с я тем, что в случае, еслик означает метил, У, У, Е и 2каждый означает водород, то в качестве алкилирующего агента применяютдиметилсульфат и в качестве растворителя применяют ксилол.Источники информации, принятыево вниманиепри экспертизе1. Патент СССР, кл. С 07 О 231/1207.07.77.
СмотретьЗаявка
2038201, 17.06.1974
Иностранная фирма "Американ Цианамид Компани
МЮРРЕЙ ГЕРБЕР
МПК / Метки
МПК: C07D 231/12
Метки: пиразолов
Опубликовано: 30.01.1979
Код ссылки
<a href="https://patents.su/6-645566-sposob-polucheniya-pirazolov.html" target="_blank" rel="follow" title="База патентов СССР">Способ получения пиразолов</a>
Предыдущий патент: Способ получения производных пиридина
Следующий патент: Способ получения 3, 5-дизамещенных пиразолов
Случайный патент: Кулачок к трехкулачковому самоцентрирующему патрону