Способ получения тризамещенных имидазолов или их солей
Похожие патенты | МПК / Метки | Текст | Заявка | Код ссылки
Номер патента: 1235454
Автор: Альфред
Текст
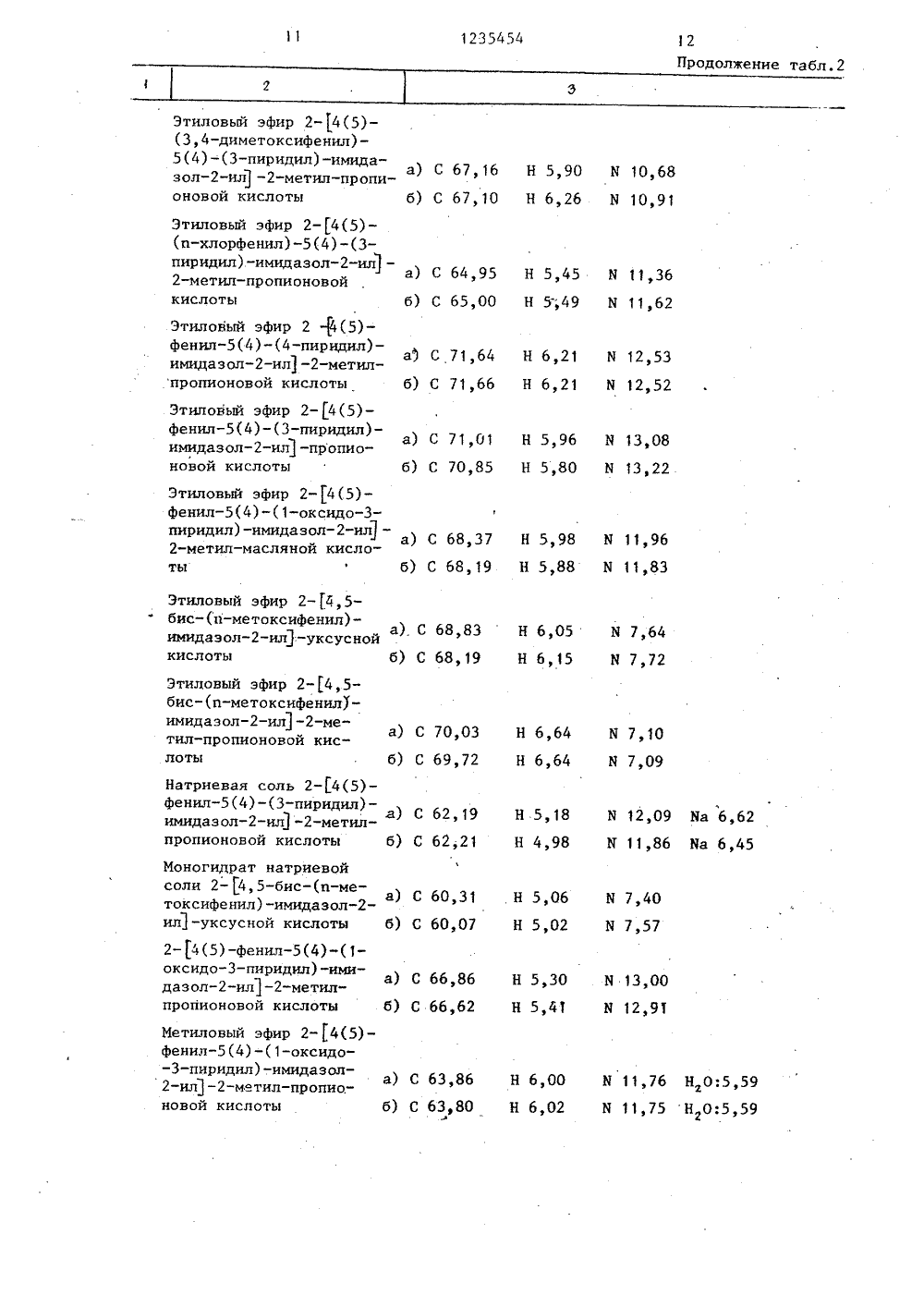
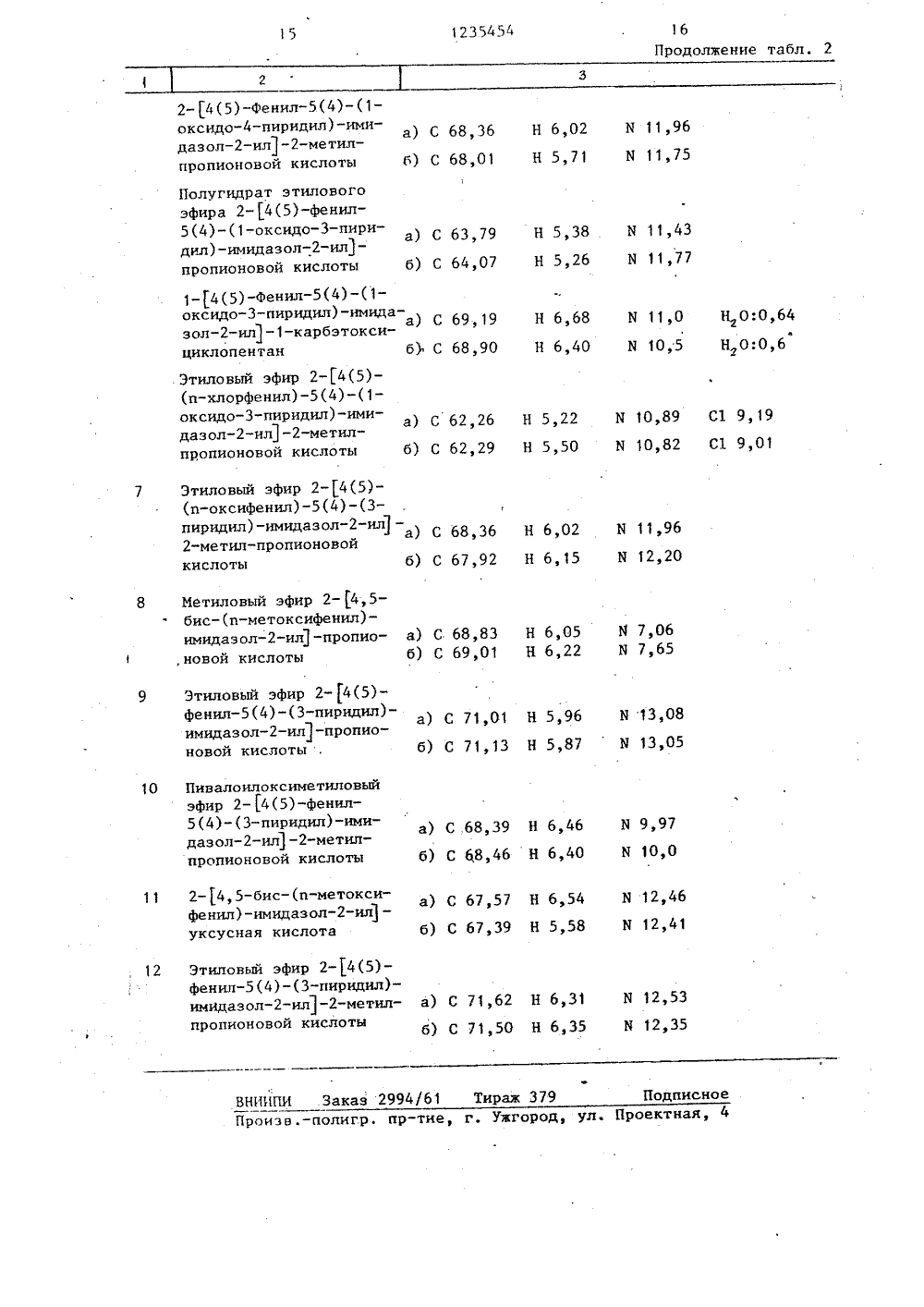
) 4 С 07 В 233/20 ОСУДАРСТ 8 ЕННЫИ НОМИТЕТ СССРПО ДЕЛАМ ИЗОБРЕТЕНИЙ И ОТКРЫТИЙ ИСАНИЕ ИЭОПАТЕН ший алкокзший алий алкоккарбокси, н сикарбонил,каноилоксинсикарбонил ил кар юл. 9 20(СН)анн (СН)7(088.8)ГетероциклИ.: ИЛ, 196 условием их солеи и илидентатка К о означаден и К ческие этит моил, оба остодновременно мет с я кси енил чт%1 А-В2 М К -С=О г где 2 - при необходимости реакцноспособный этерифицированный всложный эфир гидрокси, или его сподвергают реакции с соединениемформулы (111) нК - фенил и/или замещенный г низшим алкокси фенил,е или один из остатков К, и К - пиридил или1-оксидопиридил, а другой - фенил, замещенный низшим алкокси, окси и/или галогеном фенил или тиенил;низший алкилен, низшийалкилиден, низший алкенилиден и лимоноциклический 3-8-членный цикКз где 2 -амидинкар бок или его соль,-остатоилат,или аммони сли необ редством, ах темпе продукт карбоно эфира, ам одимо сотдающиматур 20 -формулы (1)ой кислоты,ида или пири и ако А амм предел елевой 153 С ивыделяюсоли, сл в видожногосида. ил-К-о алкилиден;. соединения, т. 5, с. 177. (54) СПОСОБ ПОЛУЧЕИИИДАЗОЛОВ ИЛИ ИХ (57) Способ получ ных имидазолов общ НИЯ ТРИЗАМЕШЕННЫХ ОЛЕЙния тризамещенй формулы (1) ЕНИЯ /",А - метиленсикарбонил,могут одноври, если Аси или карбаКг не могутфенил или ич а ю щ и йформулы (11) что если К - эток "Кг ь фенил, - карбоктка К, и значать о т л и- соединениеИзобретение относится к способу получения новых тризамещенных имидазолов,общей Формулы (1)где К и К - Фенил и/или замещенный2низшим алкокси фенил,или один из остатков К,и К - пиридил или 1-ок -сидопиридил, а другой -фенил, замещенный низшималкокси, окси и/или галогеном фенил или тиенил,А - низший алкилен, низшийалкилиден низший алкенилицен или моноциклический 3-8-членный циклоалкилиден,К - карбокси, низший алкоксикарбонил, низший алканоилоксинизший алкоксикарбонил или карбамоили их солей с тем условием, что, еслиА - метилен или этилиден и К - этоксикарбонил, оба остатка К,и К немогут одновременно означать фенил, ЗОи, если А - этилиден и К - карбокси или карбамоил, оба остатка не могут одновременно означать фенил илип-метоксифенил,Цель изобретения - синтез новыхсоединений, обладающих ценными Фармакологическими свойствами.Изобретение иллюстрируется следующими примерами.П р и м е р 1. Смесь 7, 14 г гидробромида о -бром-(3-пиридил)-бензилкетона и 19,56 г аммониевой соли этилового эфира метилмалоновой кислоты в30 мл безводного диметилформамидапри перемешивании и пропускании азоота нагревается в течение 5 ч до 100 СЗатем охлаждают и концентрируют прио11 торр при температуре бани 70 С досухого остатка, Остаток смешивают с300 мл этилацетата и 200 мл воды,рН 8-9 смеси устанавливают с помощьюконцентрированного водного аммиачного раствора. Органическую Фазу отделяют,дважды промывают водой по 50 мл,сушат над сульфатом магния и упаривают при 11 торр до сухого остатка.Остаток хроматографируют на 100 гсиликагеля, Фракции 1-8 элюированные с 600 мл хлороформа каждая, выбрасываются Фракции 9-16, элюированные смесью 600 мл хлороформ - метанол (99:1) каждая, объединяются ипри 11 торр упариваются до сухого остатка. Остаток - этиловый эфир 2- 4(5)-фенил(4)-(3-пиридил)-имидазол-ил пропионовой кислоты, желтое:масло, т. пл. 131-133 С,Аналогично получают:этиловый эфир 2- (4(5)-фенил(4) -(1-оксидо-пнридил)-имидазол-ил 12-метил-масляной кислоты, исходя изм-бром-оксидо-пиридил бензилкетона н аммониевой соли моноэтилового эфира 2-этилв метил в малонкислоты;этиловый эфир 2-4(5)-Фенил(4) -(из эфира), исходя из, -бром-(3-пиридил)-бензил-кетона и аммониевойсоли моноэтилового эфира диметилмалоновой кислоты.Исходное вещество получается следующим .образом.Раствор 42,5 г бензил-(3-пиридил)кетона в 400 мл этиленхлорида нагреовают до 50 С. При этой температуреприкапывают раствор 36,2 г брома в30 мл этиленхлорида, Суспензию перефомешивают в течение 15 ч при 50 С,затем охлаждают и фильтруют. Отфильтрованные кристаллы трижды промываютэтиленхлоридом по 30 мл и сушатпри 0,1 торр и при 50 С, ГидробромидК-бром-бензил-(3-пиридин) в ,кетона плавится при 218-219,5 С;П р и м е р 2Аналогично примеру 1 получают:1-14(5)-Фенил(4)-(3-пиридил)имидазол-ил 1 - 1-карбэтоксициклопентан, т.пл, 115-117 С;этиловый эфир 2-4(5) -(и-метоксиФенил)-5(4)-(3-пиридил)-амидазолил 1-2-метил-пропионовой кислоты,т.пл. 126-128 С;этиловый эфир 4(5)-фенил(4)(1-оксидо-пиридил)-имидазол-ил 2-метил-пропионовой кислоты; тпл,82-85 С;.гемигидрат этилового эфира 2-14(5)фенил(4)-(3-пиридил)-имидазолил 1-пропионовой кислоты, т.п, 131133 С;этиловый эфир 2-14(5)-Фенил(4)(3-пиридил)-имидазол-ил-уксуснойокислоты, т.пл. 126-129 С;,этиловый эфир 2- 4(5)-(п-хлорфенил)-5(4)-(3-пиридил)-имидазол- ил -2-метил-пропионовой кислотыоЭ т.пл. 161-163 С; 15этиловый эфир 1-4(5)-фенил(4)- -(4-пиридил) -имидаз ол-ил 1 -метило пропионовой кислоты, т,пл.210-212 С;этиловый эфир 2- 4(5)-фенил(4)- в (3-пиридил)-имидазол-ил 3 -пропионо О вой кислоты, т.пл. 131-133 С;этиловый эфир 2-4(5)-фенин(4)- -(1-оксидо-пиридил)-имидазол-илов 2-метил-масляной кислоты, т.пл.101-104 С;25этиловый эфир 2-4,5-бис-(п-метоксифенил)-ииидаеол-ил 1-уксусной кислоты, т.пл. 131-132 С;этиловый эфир 2-14,5-бис-(п-метоксифенил) -нмидазол-ил 1-2-метил-проо пионовой кислоты, т.пл. 128-132 С;натриевая соль 2-14(5)-фенил-;5(4)- (3-пиридил)-имидазол-ил-метилпропионовой кислоты, в виде гидрата, т,пл. 273-276 Сумоногидрат натриевой соли 2-4,5- бис-(п-метоксифенил)-имидазол-кфо уксусной кислоты, т.пл, 187-190 С;2-14(5)-фенил(4)-(1-оксидо- пиридил)-имидазол-ил 1 -2-метил-про-. щоо пионовой кислоты, т.пл, 178-180 С;метиловый эфир 2-14(5)-фенил(4)" (1-оксидо-пиридил) имидазол-ил 1 - 2-метил-пропионовой кислоты в видеомоногидрата, т. пл. 96-98 С; 45этиловый эфир 2-4(5)-фенил(4)- (1-оксидо-пиридил)-имидазол-ил-метил-пропионовой кислоты, т.пл.164-166 С;гемигидрат этилового эфира 2-14(5)У 50 фенил(4) в (1-оксида-пиридил)-имидазол-ил -пропионовой кислоты, т, т.пл. 145-148 С;1-14(5)-фенил(4)-(1-оксидо- пиридил)-имидазол-ил 1-1-карбэтокси- .5оу циклопентан, т.пл, 153-156 С;этиловый эфир 2-14(5)-(п-хлорфенил)-5(4) в (1-оксидо-пиридил)-имидазол-ил -2-метил-лропионовой кислоты, т.пл. 137-140 С;этиловый эфир 2-4(5)-(и-оксифенил)-5(4)-(3-пиридил)-имидазол-ил - 2-метил-пропионовой кислоты, т.пл.186-187 С;метиловый эфир 2- 4,5-бис-(п-метоксифенил)-имидазол-ил -пропионоа вой кислоты, т,пл. 124-127 С;метиловый эфир 2- 14(5)-фенил(4)- (3-пиридил)-имидазол-ил-метилО пропионовой кислоты, т,пл. 158-162 С;метиловый эфир 2-14(5) -фенил(4) - (3-пиридил)-имидазол-илметилпроо пионовой кислоты, т.пл. 143-145 С;2-425-бис-(и-метоксифенил)-имидазол-ил 1 -уксусную кислоту, ИК (КВг) 3500 (шир), 1760 см у. т.пл. 159 - 161 С;амид 2-14,5-бис-(п-метоксифенил) - имидазол-ил -уксусной кислоты, ИК (КВг): 1670 см , т.пл. 119-121 С;2-14(5)-фенил(4)-(3-пиридил)- иющазол-ил 1 -уксусную кислоту, масло, ИК (КВг): 3500 (шир.), 1740 см т.пл, 129-131 С;амид 1-4 у 5-бис-(и-метоксифенил)- имидазол-ил)-2-метилпропионовой кислоты, ИК (КВг): 1670 см , т.пл.128-130 С;этиповый эфир 2-4(5)-тиенил(4)- (3-пиридил)-имидазол-ил 1-метил-пропионовой кислоты, т.пл. 134-150 С.оП р и м е р 3. Аналогично примеру 1 получают".2-Г 4(5)-фенил(4)-(3-пиридил)- имидазол-ил - уксусную кислоту, масло, т.пл. 129-131 С, ИК (КВг): 3500 (шир.), 1740 смамид 24,5-дис-(п-метоксифенил) - имидазол-ил -2-метилпропионовой кислоты, ИК (КВг): 1660 см , т.пл.128-130 С;этиловый эфир 2- 4(5)-(2-тиенил)-5(4)-(3"пиридил)-имндазол-ил 1- 2-метил-пропионовой кислоты, т.пл.134-135 С.П р и м е р 4. Раствор этилового эфира 2-4(5)-фенил(4)-(3-пиридил)-имидазол-ил 1-2-метил-пропионовой кислоты (3,32 г) в 20 мл метанола смешивается с 40 мл 0,5 н.раствора натриевой щелочи. Раствор перемешивают 4 ч при комнатной температуре и упаривают при пониженном давлении и при 40 С. Остаток смешиовают с 50 мл метиленхлорида и отфильтровывают желтоватые кристаллы.Натриевая соль 2- 4 (5) -Фенил(4)(3-пиридип)-имидазол-ил -2-метилпропионовой кислоты (как гидрат) плавится при 273-276 С,5Аналогичным образом получают: моногидрат натриевой соли 2- 4,5-(пметоксифенил)-имидазол-ил 1-уксусной кислоты, т.пл. 187-190 С, исходяиз этилового эфира 2-4,5-бис-(пметоксифенил)-имидазол-ил -уксусной кислоты,П р и м е р 5. Раствор 0,9 гэтилового эфира 2-Г 4(5)-Фенил(4) -(1-оксидо-пиридил)-2-ил 1-2-метилпропионовой кислоты в 10 мл метанолапри перемешивании смешивают с 3,0 мл1 н, раствора натриевой щелочи, Раствор в течение 15 ч перемешивают прикомнатной температуре и при 11 торр 20ои при 40 С освобождают от метанола.,Остаток смешивают с 20 мл воды и желтый раствор экстрагируют с 20 мл хлороформа. Затем отделяют водную фазуи при 0 С подкисляют с 2 н, раствором 25осоляной кислоты. Прозрачный раствореще раз экстрагируют с. 10 мл хлороформа, Затем водную Фазу при 11 торри при 40 С упаривают до сухого ос-,татка. Белый кристаллический остаток З 0сушат при 0,1 торр и комнатной температуре в течение 20 ч2- 4(5)-Фенил(4)-(1-оксидо-пиридил)-имидазол-ил-метил-пропионовая кисолота плавится при 178-180 С,35 П р и м е р 6, Раствор 5,9 г этилового эфира 2- 4(5)-фенил(4)-(3- пиридил)-имидазол-ил -2"метил-пропионовой кислоты в 120 мл метиленхло орида охлаждают до 0-5 и смешивают с3,5 г м-хлор-пербензойной кислоты. Смесь перемешивают при комнатной температуре в течение 24 ч, Затем желтый раствор дважды промывают 2 н, раствором бикарбоната калия по 20 мл и с 30 мл воды, сушат над сульфатомф омагния и при 40 С и пониженном давлении сгущают. Остаток растворяется в небольшом количестве метанола.Пос ле добавления воды кристаллизуется этиловый эфир 2- 4(5)-фенил(4)-(1- оксидо-пиридил)-имидаэол-ил -2- метил-пропионовой кислоты в виде монои гидрата, точка плавления 82-85 С. 55Аналогичным образом получают:метиловый эфир 2- 4(5)-(2-тиенил) - 5(4)-(1-оксидо-пиридил)-имидазол 2-ил 1-2-метил-пропионовой кислоты, т,пл, 134-135 С;моногидрат метилового эфира 2- 4(5)-Фенил(4)-(1-оксидо-пиридил)- имидазол-ил-метил-пропионовойокислоты, т.пл. 96-98 С (из смеси метанол - вода);2-4(5) -Фенил(4)-(1-оксидо- пирицил)-имидазол-ил 1 -2-метил-проо пионовой кислоты, т.пл. 164-166 С (из этил:ацетата), исходя из этилового эфира 2- 4(5)-Фенил(4)-(4-пиридил)-имццазол-ил-метил-пропионовой кислоты;полугидрат этилового эфира 2- 4(5)- фенил(4)-(1-оксида-пиридил)-имидазол-ил 1 -пропионовой кислоты, масло, т.пл. 145-148 С, исходя из этилового эфира 2-4(5)-Фенил(4)-(3- пиридип)-имидазол-ил 1-пропионовой кислоты"1" "4(5)"Фенил(4) в (1-оксидо-пиридил)-имидазол-ил 1-карбэтокси-цико лопентан, масло, т.пл, 153-156 С, исходя из 1-4(5)-Фенил(4)-(3-пиридил)-имидазол-ил-карбэтокси-циклопентан;этиловый эфир 2- 4(5)-(и-хлорфенил)-5(4)-(1-оксидо-пиридил)-имидазол-ил -2-метил-пропионовой кисОлоты т.пл. 137-140 С (из смеси метиленхлорид - петролейный эФир), исходя из 2-4(5)-(и-хлорфенил)-5(4)-(3- пиридил)и;:идазол-ил -2-метил-пропионовой кислоты.П р и м е р 7. Раствор 1,3 г этилового эфира 2-4(5)-(и-метоксифенил)- 5(4)-3-пиридил)-имидазол-ил 1-2-метил-пропиоиовой кислоты в 50 мл метиленхлорида в атмосфере азота приоперемешивании и при -70 С, прикапывая в течение 3 мин, смешивают с раствором 47 г бортрибромида в 20 мл метиленхлорида. Смесь перемешивают при -О С в течение 30 мин, Затемоудаляют охлаждающую баню и перемешивают до тех пор, пока температура не достигает 25 С. После этого белую суспензию выпивают на 50 мл смеси льда с водой и перемешивают. Водную Фазу отделяют, дважды экстрагируют метипенхлоридом по 20 мл и с 2 н,раствором карбоната натрия, при этом рН 8. Выпавшие в осадок кристаллы дважды экстрагируют этилацетатом по 30 мл. Объединенные этилацетатные фазы сушат над сульфатом магния ипри пониженном давлении упаривают до сухого остатка. Остаток кристаллизуют из смеси этилацетат - эфир.Этиловый эфир 2-4(5)-(р-гидроксифенил)-5(4)-(3-пиридил)-имидазол- 5 ил -2-метил-пропионовой кислоты плавится при 186-187"С.П р и м е р 8. 100 мл насыщенного газообразным хлористым водородом безводного метанола смешивают с 5,0 г 2- 4,5-бис-(р-метоксифенил)-имидазол- -2-ил -пропионовой кислоты. Смесь нагревают 15 ч с обратной флегмой, охлаждаются и при пониженном давлении упаривают до сухого остатка. Остаток смешивают с 10 мл воды и с помощью водного концентрированного аммиачного раствора делают щелочным. Экстрагируют дважды этилацетатом по 40 мл и органическую фазу при 5 С промывают 2 Оо с 20 мл 2 н. раствора бикарбоната калия и с 20 мл воды, сушат ее над сульсульфатом магния и концентрируют при пониженном давлении до сухого остатка, Метиловый эфир 2 -14,5-бис-(р-мет оксифенил)-имидазол-ил-пропионовой кислоты кристаллизуют из смеси эфир - петролейный эфир, т.пл, 124- 127 С.П р и м е р 9. Раствор 3,52 г ЗО калиевой соли 2-4(5)-Фенил(4)- (3-пиридил)-имидазол-ил-пропионовой кислоты в 30 мл безводного димеотилформамида при 80 С и при перемешивании смешивают с 3,0 г диэтилсуль-З 5 фата, Смесь при 80 С перемешивают 15 мин, охлаждают и выливают на смесь льда с водой. Масло растворяют в этилацетате и органическую фазу дважды экстрагируют с 2 н. раствором 4 О бикарбоната. калия, сушат над сульфатом магния и при пониженном давлении упаривают до сухого остатка. Этиловый эфир 2-4(5)-фенил(4)-(3-пнридил)- имидазол-ил -пропионовой кислоты 45 кристаллизуют из эфира, т.пл, 158- ,162 С.П р и м е р 10. Суспензию 3,5 г моногидрата натриевой соли 2-4(5)- -фенил(4)-(3-пиридил)-имидазол- ил-метил-пропионвой кислоты в 50 мл безводного диметилформамида при пропускании азота и перемешиванни при комнатной температуре капельным образом смешивают с 2,5 г пивалоилоксиметилиодидом. Смесь перемешивают 15 ч при комнатной температуре затем при 11 торр упаривают до сухого остатка. Остаток распределяют между 20 мл воды и 50 мл этилацетата. Органическуюфазу отделяют, сушат над сульфатоммагния и при 11 торр сгущают до сухого остатка, Остаток хроматографируют на 300 г силикагеля. ФракцииГ1-15, элюированные смесью хлороформэтилацетат (95:5) по 300 мл, выбрасываются, Фракции 16-26, элюированные смесью хлороформ - этилацетат(80:20) по 300 мл, объединяются и при11 торр упариваютдо сухого остатка. Остаток крйсталлизуют из смесиэфир - петролейный эфир, Пивалоилоксиметиловый эфир 2-4(5)-фенил(4)(3-пиридил)-имидазол-ил-метил-пропионовой кислоты плавится нри143-145 С.П р и м е р 11. Раствор 5 0 гамида 2-4,5-бис-(р-метоксифенил)имидазол-ил -уксусной кислоты и5,0 г гидроксида калия в 100 мл н -бутанола нагревают 8 ч с обратной флегмой, Затеи охлаждают и при О, 1 торро,и 50 С упаривают до сухого остатка,Остаток растворяют в 200 мл воды.Раствор фильтруют и фильтрат подкисляют концентрированной соляной кислотой. Выпавшие в осадок кристаллы 2- 4,5-бис-(р-метоксифенил)-имидазол-нл-уксусной кислоты отфильтровывают, ИК (КВг): 3500 (шир,), 760 смт.пл. 159-161 С.П р и м е р 12. Смесь из 3,35 г(0,025 моль) карбоната калия в 100 млацетонитриала 60 ч перемешивают ватмосфере азота прн комнатной температуре (20 С), Смесь Фильтруют, остаток смешивают с водой, смешиваютс 50 мл ледяной уксусной кислотыои 96 ч перемешивают при 20 С, Смесьзатем выливают на 100 г льда, дваждыэкстрагируют этилацетатом, соединенные органические фазы промывают донейтральной реакции, сушат над сульфатом натрия н упаривают досуха при40 С при 11 торр. Остаток перекрисоталлизовывают из эфира, получая этиловый эфир 2-4,5-бис-(п-метоксифенил)-имидазол-ил-метил-пропионовой кислоты, т.пл, 128-129 С,Аналогично превращение можно осужствлять в среде кипящего диметилформамида.1235454 10Продолжение табл, 1 Результаты испытаний сведены втабл, 1 и 2,Пример Выход Т а б л и ц а 1 Выходт теория, 7. Пример 0,3 2,7 1,1 о 910 79 25 2,4 60 3,0 91 0,75 64 2,0 12 Таблица 2 Элементарный анализ,а - вычислено, б - найдено Соединение Пример а) С 68,36 Н 6,02 Н 11,96 б) С 68,01 Н 5,7.1 И 11,75 а) С 63, 79 Н,5,38 И 11,43 б) С 6407 Н 526 Н 1177 а) С 69,19 Н 6,68 М 11,0 Н О:0,64 Х 11,5 Н О 0,6 б) С 68,9 Н 6,40 а) С 62,26 Н 5,22 И 10,89 О 12,44 С 1 9,19 б) С 62,29 Н 5,50 Н 10,82 О 12,85 С 1 9,01 Этиловый эфир 2-4(5) -фенил(4) - (3-пиридил)имидазол-ил-уксуснойкислоты а) С 70,34 б) С 70,00 И 13,6И 13,8 Н 5,58Н 5,8 а) С 72,60 Н 6,09 Н 12,09 б) С 72,49 И 12,18 Н 6,05о а) С б) С 1 Этиловый эфир 2 ф(5)- фенил(4)-(1-оксидопиридил)-имидазол-ил -2-метилпропионовой кис- лоты Этиловый эфир 2-4(5)-фенил(4) - (1-оксидопиридил)-имидазол-иловпропионовой кислоты 2 1- 4(5) -Фенил(4) -(1 оксидо-пиридил)-имидазол-ил -1-карбэтокси- циклопентан Этиловый эфир 2-4(5)- (и-хлорфенил) -5 (4) -(1- оксидо-пиридил)-имидазол-ил 1 -2-метил-пропионовой кислоты Этиловый эфир 2-14 (5)- фенил(4)-(3-пиридил)- имидазол-ил 1-2-аллилуксусной кислоты Метиловый эфир 2- 4(5)- (м-метоксифенил) -5 (4) - (З-пиридил)-имида.зол- ил-метил-пропионовой кислоты 69,02 Н 6,35 М 11,50 69,22 Н 6,55 М 11,68(3,4-диметоксифенил)- 5(4)-(3-пиридил)-имидазол-ил -2-метил-пропионовой кислоты б) С 67,10 Н 5,90 К 10,68 Н 6,26 К 10,91 Этиловый эФир 2-4(5)- (и-хлорфенил)-5(4)-(3 пиридил)-имидазол-ил - ) С 64 95 2-метил-пропионовойкислоты б) С 65,00 Н 5,45 К 11,36 Н 5",49 К 11,62 а 5 С 71,64 Н 6,21 К 12,53 б) С 71,66 Н 6,21 К 12,52 Этиловый эфир 2-4(5)- фенил(4)-(3-пиридил)имидазол-ил -пропионовой кислоты б) С 0,85 Н 5,96 К 13,08 Н 5,80 К 13,22 Этиловый эфир 2-4(5)- фенил(4)-(1-оксидопиридил)-имидазол-ил - ) С 68 37 2-метил-масляной кислотыб) С 68,19 К 11,96К 11,83 Н 5,98 Н 5,88 Этиловый эфир 2-4,5- бис-(и-метоксифенил)- а) имидаэол-ил 1-уксусной кислоты б) К 7,64 Н 6,05 С 68,83 а) б) Натриевая соль 2-4(5)- фенил(4)-(3-пиридил)- а) имидаз ол-ил 1-2-метилпропионовой кислоты б) К 12,09 Ка 6,62 С 62,19 Н 5,18 Моногидрат натриевой соли 2- 4 5-бис-(и-меФа) токсифенил)-имидазол- ил 1-уксусной кислоты б) 2-(4(5)-вменил(4)-(1- оксидо- пиридил) -имиа) дазол-ил-метилпропионовой кислоты 6) Метиловый эфир 2- 4(5)- фенил(4) - (1-оксидо- -3-пиридил) -имидазола) 2-ил-метил-пропио. - новой кислоты б) К 13,00 С 66,86 Н 5,30 Н 5,41 К 12,91 С 66,62 Н 0:5,59Н 0:5,59 С 63,80 Н 6,02 К 11,75 Этиловый эфир 2 -4(5)фенил(4)-(4-пиридил)имидазол-ил 1 -2-метилпропионовой кислоты Этиловый эфир 2-4,5- бис-(и-метоксифенил)- имидазол-ил 1-2-метил-пропионовой кис- лоты С 68,19 Н 6,15 К 7,72 С 70,03 Н 6,64 К 7,10 С 69,72 Н 6,64 К 7,09 С 62,2 1 Н 4,98 К 11,86 Ка 6,45 С 60,31 Н 5,06 К 7,40 С 60,07 Н 5,02 К 7,57 С 63,86 Н 6,00 К 11,76,02 Этиловый эфир 2-4(5)фенил(4) в (1-оксидо 4-пиридил)-имидазолил -2-метил-пропионовойкислоты 2- 3, 4-бис- (и-Иетоксифенил) -имидазол-ил 1 уксусная кислота Амид 2- 4,5-бис-(п-метоксифенил)-имидазолил-уксусной кислоты2- 4 (5) -фенил(4) - (3 пиридил) -имидазолил -уксусная кислота Амид 2- 4,5-бис-(п-метоксифенил)-имидазол 2-ил-метил-пропионовой кислоты Этиловыи эфир 2- (2-тиенил)-5(4) - ридил)-имидазол-метил-пропионо кислотыНатриевая соль 2 фенил(4)-(3-пи имидазол-илпропионовой кисл Натриевая сольбис-(и-метоксифимидаз ол-ил - ной кислоты 2-4(5)-Фенил(4) в (1- оксидо-пиридил)-имидаэ ол-ил -2-метилпропионовая кислота Этиловый эфир 2-4(5)- фенил(4) в (1-оксидо-пиридил)-имидазол-ил 1-2-метил-пропионовой кислотыЭтиловый эфир 2-4(5)- (2-тиенил)-5(4)-(1-оксидо-пиридил)-имида" зол-ил-метил-пропионовой кислоты Метиловый эфир 2-4(5) Фенил(4) в (1-оксидо-пиридил)-имидазол- ил 1-2-метил-пропионовой кислоты 14Прсдолжение табл, 2. 5,98 Н 11,9 5,87 Н 11,7 11,38 Н 20:4,8 11,7 1 ИО:4,21235454 16Продолжение табл. 2 2- 4 (5) -Фенил(4)- (1 оксидо-пиридил)-имидазол-ил-метилпропионовой кислоты Я 11,96 М 11,75 Н 6,02 а) С 68,36 б) С 6801 Н 5 71 М 11,43 М 11,77 Н 5,38 С 63,79 С 64,07 Н 5,26 Н О:0,64Н О:0,6 Н 6,68 М 11,0 С 69,19 М 10,5 С 68,90 Н 6,40 Метиловый эфир 2- 4,5 бис- (и-метоксифенил) -имидазол-ил 1-пропио,новой кислоты М 7,06 М 7,65 а) С 68,83 б) С 69,01 Н 6,05 Н 6,22 Этиловый эфир 2- 4(5)- фенил(4)-(3-пиридил)имидазол-ил-пропионовой кислоты б) С 71,13 Н 5,96 Я 13,08 Н 5,87 М 13,05 Пивалоилоксиметиловый эфир 2 - 4(5)-фенил (4) - (3-пиридил) -имидаз ол-ил 1-2-метиппропионовой кислоты а) б) Этиловый эфир 2-4(5)- фенил(4)-(3-пиридил)- имидазол-ил 1-2-метилпропионовой кислоты а) С 71,62 Н 6,31 б) С 71,50 Н 6,35 Я 12,53М 12,35 ВНИИПИ .Заказ 2994/61 Тираж 379 Подписное Произв,-полигр. пр-тие, г. Ужгород, ул. Проектная, 4 11 олугидрат этилового эфира 2-14(5)-фенил(4)-(1-оксидо-пириа) дил) -имидазол-ил- пропионовой кислоты б) 1-4(5)-Фенил(4)-(1 - оксидо-пиридил)-имидаа) зол-ил-карбэтоксициклопентан б) . Этиловый эфир 2-4(5)- (и-хлорфенил) -5 (4) - (1- оксидо-пиридил)-имиа) дазол-ил 1-2-метилпропионовой кислоты б) Этиловый эфир 2-4(5)- (и-оксифенил)-5(4)-(3- пиридил)-имидазол-илова) 2-метил-пропионовой кислоты б) 2-14 5-бис-(и-метоксиУа)фенил) -имидазол-ил -уксусная кислота б) С 62,26 Н 5,22 Я 10,89 С 1 9,19 С 62,29 Н 5,50 М 10,82 С 1 9,01 С 68,36 Н 6,02 М 11,96 С 67,92 Н 6,15 Я 12,20 С .68,39 Н 6,46 М 9,97 С 8,46 Н 6,40 М 10,0 С 67,57 Н 6,54 Я 12,46 С 67,39 Н 5,58 Я 12,41
СмотретьЗаявка
3317053, 24.07.1981
Циба-Гейги АГ
АЛЬФРЕД САЛЛМАНН
МПК / Метки
МПК: C07D 233/20
Метки: имидазолов, солей, тризамещенных
Опубликовано: 30.05.1986
Код ссылки
<a href="https://patents.su/9-1235454-sposob-polucheniya-trizameshhennykh-imidazolov-ili-ikh-solejj.html" target="_blank" rel="follow" title="База патентов СССР">Способ получения тризамещенных имидазолов или их солей</a>
Предыдущий патент: Пресс с коробчатым корпусом
Следующий патент: Зажимной челнок ткацкого станка
Случайный патент: Установка для окраски изделий