Способ получения гидрохлоридов замещенных 2 4-окси-4-(п фторфенил)бутил -4а, 9в-транс-2, 3, 4, 4а, 5, 9в-гексагидро-1н пиридо4, 3виндолов
Похожие патенты | МПК / Метки | Текст | Заявка | Код ссылки
Номер патента: 1333239
Автор: Виллард
Текст
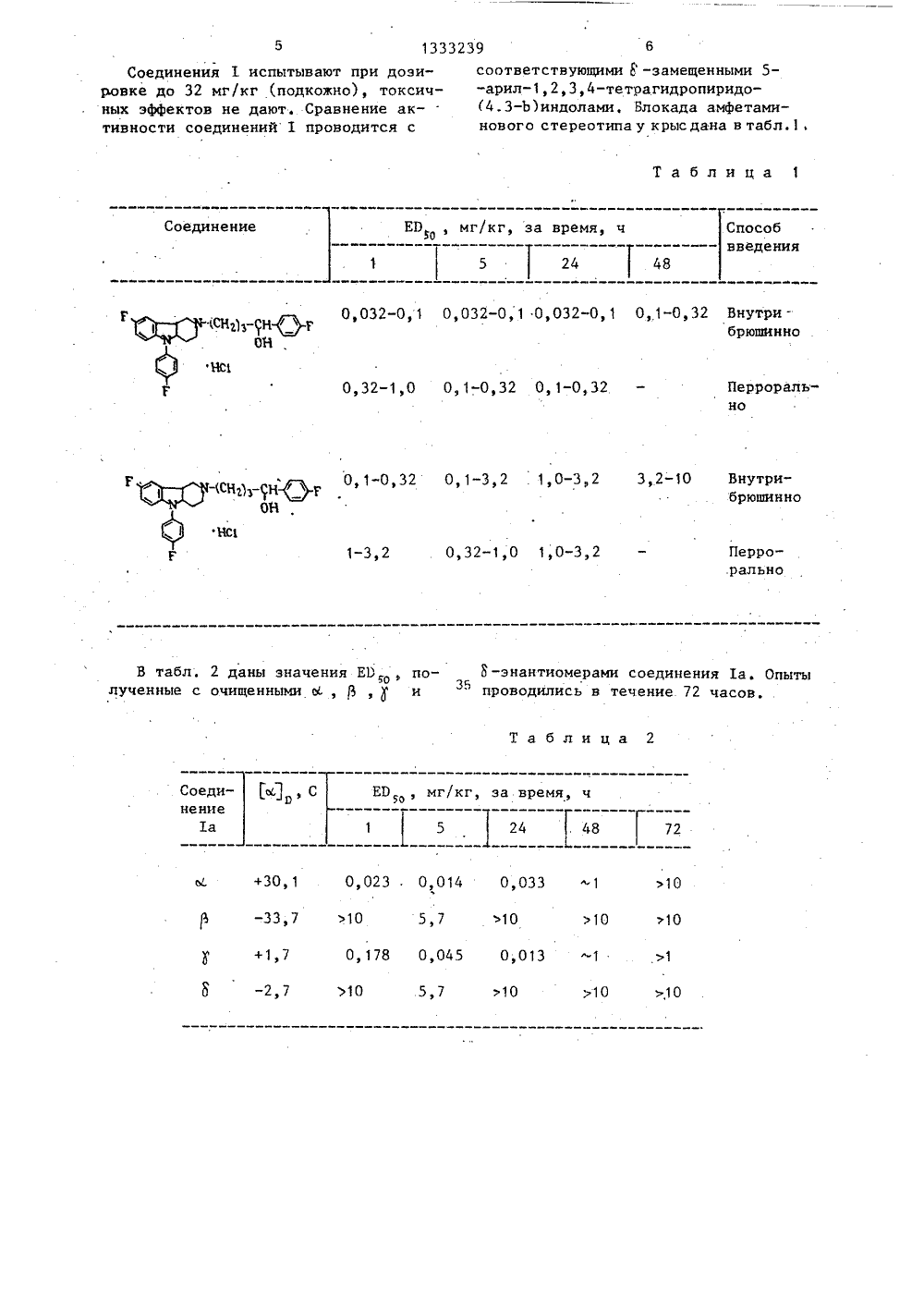
СОЮЗ СО 8 ЕТСНИХСОЦИАЛИСТИЧЕСКИХРЕСПУБЛИК ЗСЕСЯОЗИ Яз И 1 НГН 9 П Хэйолф4 11 11 ЮТЮА ОПИСАНИЕ ИЗОБРЕТЕНИЯН ПАТЕНТУ(ф 4 ГОСУДАРСТ 8 ЕКНЫЙ КОМИТЕТ СССРПО ДЕЛАМ ИЗОБРЕТЕНИЙ И ОТКРЫТИЙ(72) Виллард Маккован Велч (младший)(54) СПОСОБ ПОЛУЧЕНИЯ ГИДРОХЛОРИДОВЗАМЕЦ 1 ЕННЫХ 2- 4-ОКСИ-(п-ФТОРФЕНИЛ) -БУТИЛ 1-4 А,9 В-ТРАНС,3,4,4 А,5,9 В-ГЕКСАГИДРОН-ПИРИДО(4,3-В)ИНДОЛОВ(57) Изобретение касается замещенныхиндола, в частности гидрохлоридов2- 4-окси-фенил (или п-фторфенил)бутила,9 Ь-транс,3,4,4 а,5,9 Ь-гексагидроН-пиридо (4,3-Ь)индолов,801333239 А 3 51 4 С 07 Э 471/04, А 61 К 31/395 которые проявляют транквилиэирующеедействие и могут быть использованы вмедицине, Цель - создание активныхвеществ указанного класса. Получениенового индола ведут из соответствующего (+) или (+) амина и эквимолярного количества 5-(п-фторфенил)-2-окситетрагидрофурана в среде реакционно-инертного растворителя в присутствии эквивалентного количествацианоборгидрида натрия или водородаи каталитического количества палладия в качестве восстановителя прикомнатной температуре, О -Энантиомер получают с 97,5%-ной чистотой,т. пл, 248-252 С, м= (+) 30,1 С(-) 33,7 С,-энантиомер - с чистотой 98%, т. пл. 254-256 С,- (+) 1,7 С, 3 -энантиомер - с чистотой 98%, т, пл, 257-260 С и ы. в- (-) 2,7 С. В сравнении с известными 3 -замещенными 5-арил,2,3,4-тетрагидро-(4,3-Ь)индолами новые вещества в отношении действия амфетамина проявляют лучшую активность.2 табл, 133Изобретение относится к способу получения новых химических соединений ряда-карболина, а именно гидрохлоридов замещенных 2- 4-окси- -(п-фторфенил)бутил -4 а,9 Ь-транс- -2,3,4,4 а,5,9 Ь-гексагидроН-пиридо(4,3-Ъ)индолов общей формулы32392 5 10 костной хроматографии при высоком давлении чистота 97,5%.-Энантиомер. К раствору 53 мг (0,95 ммоль) .гйдроксида калия в 50 мл метанола добавляют в атмосфере азота 613 мл (1,9 ммоль) левовращающего хлористоводороднсго 8-фтор-(п-фторфенил)-2,3,4,4 а,5,9 Ь-гексагидроН-пиридо(4,3-Ь)индола,а(-) 40,9 (метанол), и смесь пере" мешивают до полного растворения. К раствору добавляют 346 мг (1,90 ммоль) левовращающего 5-(и-фторфенил)-2-ок15 20 25 30 40 45 50 где Х и У - водород или фтор,которые проявляют транквилизирующеедействие и могут найти применениев медицине,Цель изобретения - разработка наоснове известного метода способа получения новых соединений, обладающихценными фармацевтическими свойствами.П р и м е р 1, Хиральный синтезэнантиомеров 8"фтор-(п-фторфенил)-2-4-окси-(п-фторфенил)бутил,3,4,4 а,5,9 Ь-гексагидроН-пиридо(4,3-Ь)индола гидрохлорида (1 а),Ы-Энантиомер. 5-(п-Фторфенил)-2-окситетрагидрофуран 230 мг растворяют в 30 мл метанола, добавляют свободное основание правовращающего 8-фтор-(п-фторфенил)-2,3,4,4 а,5,9 Ь-гексагидроН-пиридо(4,3-Ь)индола404 мг (1,25 ммоль), смесь перемешивают 15 мин, добавляют 150 мг катализатора 10%-ного палладия на углеи перемешанную смесь гидрируют приатмосферном давлении, После прекращения поглощения водородакатализатор удаляют фильтрованием и растворитель выпаривают в вакууме. Остаток распределяют между этилацетатоми 10%-ным водным раствором гидроксида натрия. Водный слой экстрагируют опять этилацетатом, соединенные экстракты высушивают (М 8804) ивыпаривают досуха. Остаток хроматографируют на 20 г силикагеляи элюируют этилацетатом. Фракции, содержащие требуемый продукт, соединяют,выпаривают досуха, растворяют в этиловом эфире и превращают в хлористоводородную соль путем добавленияэфирного раствора хлористого водорода, Выход 144 мг, т. пл. 248252 С,сс = (+) 30,1 С (метанол),По результатам анализа методом жидситетрагидрофурана, растворяют в небольшом объеме метанола, и полученный раствор перемешивают 15 мин при комнатной температуре. Раствороохлаждают до 5 С и добавляют в течение 20 мин 120 мг (1,90 ммоль) цианоборгидрида натрия в небольшом количестве метанола. Реакционную смесь перемешивают при комнатной температуре 45 мин, затем добавляют 250 мг гидроксида калия и перемешивают до растворения, Растворитель выдерживают в вакууме, и остаток распределяют между этилацетатом и водой.После повторной экстракции водной фазы соединенные органические экстракты сушат (М 8804), ыпаривают в вакууме и получают 1,014 г масла, Его хроматографируют на 30 г силикагеля, и получают 653 мг требуемого продукта в виде масла. Масло превращают в хлористоводородную соль и получают 400 мг, Т. пл, 252-257 С (разлагается), ос= -33, 7 С (метанол) .Найдено, что продукт представляет собой-энантиомер чистотой 99%. После обработки маточного раствора получают еще 80 мг продукта. Т. пл, 254 о258 С (разлагается)Суммарный выход 56%.-Энантиомер. В 25 мл метанола растворяют 2,07 мг (6,4 ммоль) хлористоводородного д (+)-8-фтор-(п-фторфенил)-2,3,4,4 а,5,9 Ь-гексагидроН- -пиридо(4,3-Ь)индола, Я(+) 39 С, и 1,3 г (7,1 ммоль) левовращающего 5-(и-фторфенил)-2-окситетрагидрофурана, и раствор перемешивают в атмосфере азота при комнатной температуре 15 мин, Добавляют 300 мг катализатора 5%-ного палладияна угле и смесь гидрируют при атмосферном давлении 3 ч. Реакционнуюсмесь обрабатывают, как указано для4-энантиомера, и получают 2,4 г не3133 очищенного продукта в виде желтой пены. Пену растворяют в 40 мл ацетона, и полученный раствор добавляют к 20 мл этилового эфира, насыщенно го хлористым водородом. После стояния при комнатной температуре в течение 2 ч смесь фильтруют и получают 980 мг хлористоводородной соли, Фильтрат выпаривают и получают 1,7 г пены, Ее хроматографйруют отдельно на силикагеле, полученные фракции опять обрабатывают хлористым водородом и получают соответственно 140 мг, ор .= (+) 1,4 С (метанол) и 800 мг Ы = (+) 1,7 С (метанол). Оба продукта имеют температуру плавления 254-256 С. Методом жидкостной хроматографии при высоком давлении установлено, что каждый из них представляет собой -энантиомер чистотой 987. 3 -Энантиомер. К хлористоводородному 1 (-)-8-фтор-(п-фторфенил)-2,3,4,4 а,5,9 Ь-гексагидроН-пири-.до(4,3-Ь)индолуо = (-) 40 9 ОС(968 мг, 3,0 ммоль, растворенномув минимальном количестве этанола, добавляют эквимолярное количество правовращающего, 5-(п-фторфенил)-2-окситетрагидрофурана. Смесь нагревают напаровой бане, добавляя дополнительное количество этанола до образования гомогенного раствора. Раствор оставляют охлаждаться до комнатной температуры и получают 1300 мг неочи -щенного оо-энантиомера в виде бледножелтой смолы. Смолу превращают в хлористоводородную соль, 835 мг (573) .Т. пл. 240-250 С. Ее хроматографируют на 30 г силикагеля, и фракцииэлюированного продукта выпаривают,снова обрабатывают эфирным растворомхлористого водорода и получают 610 мг .Т.Пл, 257-260 С. оь = (-) 2,7 С(метанол), чистота которого 987 (пожидкостной хроматографии при высокомдавлении),П р и м е р 2, д 1-8-Фтор-фенил-(4-гидрокси-(п-фторфенил)-бутил,3,4,4 а,5,9 Ь-гексагидроН-пиридо(4,3-Ь)индола гидрохлорида.Смесь 300 мг й 1-8-фтор-фенил,3,4,4 а,5,9 Ъ-гексагидроН-пиридо(4,3-Ь)индола гидрохлорида, 10 мпэтилацетата, 10 мл насыщенного раствора карбоната натрия встряхивают,слои разделяют, и к органическому 3239слою добавляют 45 мг катализатора(57-ный палладий на угле) и 273 мг1-5-(п-фторфенил)-2-гидрокситетрагидрофурана. Эту смесь встряхивают55 ч при 50 С под давлением водородао1 атм. Результирующую смесь фильтруют, к фильтрату добавляют 1, 1 мольэквивалента хлористого водорода вэтилацетате, и результирующую смесьперемешивают при 20 С 1 ч для гранулирования осадка. Продукт собираютфильтрованиемпромывают этилацетатом и сушат при 40 С на протяженииночи с получением 146 мг (327) продукта, т. пл. 199"201 С.П р и м е р 3, Л"(п-Фторфенил)-2-(4-гидрокси-(п-фторфенил)- -бутил,3,4,4 а,5,9 Ь-гексагидроН-(897) неочищенного продукта, т. пл.188-191 С. Очистка с использованиемохроматографии на силикагеле, элюирование смесью 1: 1 гексан/этилацетат,ЗО дают 29 мг чистого целевого соединения, т. пл, 208-210 С.Действие соединений 1 на заметные,вызванные амфетамином симптомы, исследуют на крысах, Группы из пятикрыс помещают в закрытую пластмассовую клетку размерами приблизительно26 х 42 х 16 см, После непродолжительного периода акклиматизации вклетке крысам каждой группы вводят40 нодкожно испытуемое соединение, Затем спустя 1,5 и 24 ч им дают нитраперитонально Й-амфетаминсульфат,5 мг/кг. Через час после введенияамфетамина каждую крысу наблюдают с 45 целью характеристик ее поведениявызванного амфетамином, которое состоит в движении по клетке, На основании данных о поведении после амфетамина с учетом дозы можно определить эффективную дозу испытуемогосоединения, необходимую для подведения или брокирования характерногоамфетаминного поведения - движенияпо клетке - для 507. подопытных крыс55 ( 50)фВыбранное время оценки совпадаетс пиковым действием амфетамина, составляющим 60-80 мин после введенияэтого средства,1333239 Соединения 1 испытывают при дозировке до 32 мг/кг (подкожно) токсичных эффектов не дают. Сравнение активности соединений 1 проводится с Таблица 1 ЕР , мг/кг за время ч Соединение Способвведения 5 24 48 0,032-0,1 0,032-0,1 0,032-0,1 0,1-0,32 Внутри -брюшинно 0,32-1,0 О, 1-0,32 О, 1-0,32 Перрорально О 1 032 01 32 10 32 0,32-1,0 1,0-3,2 Перро.рально 1-3, 2 В табл. 2 даны значения ЕВ , по -энантиомерами соединения 1 а. Опытылученные с очищенными о,и проводились в течение 72 часов.ЗБ Таблица 2 ЕП , мг/кг за время, ч 1 5 24 . 48 72Соеди- М , Снение1 а соответствующими 1 -замещенными 5-арил,2,3,4-тетрагидропиридо(4.3-Ъ)индолами, Блокада амфетаминового стереотипа у крыс дана в табл.1,3,2-10 Внутрибрюшинно1333239формула изобретения Способ получения гидрохлоридов замещеннь 1 х 2-4-окси-(п-фторфенил)- .5 бутил -4 а,9 Ь-транс,3,4,4 а,5,9 Ь- -гексагидроН-пиридо(4,3-Ъ)индолов общей формулы где Х и У имеют указанные значения, О (подвергают взаимодействию с эквимолярным количеством 5-(п-фторфенил)- 1-2-окситетрагидрофурана в среде реакционно-инертного органического растворителя в присутствии эквивалент ного количества цианоборгидрида иат"рия Или водорода и каталитического количества палладия в качестве восстановителя при комнатной темпера.туре. Х- водород или фтор, а ю щ и й с я тем, что, ющий или рацемический амин мулы где Х ио тлиправовращобщей фо Составитель В,Теренинктор И,Горная Техред Л.Сердюкова Корректор Н.Король Подп комитета СССР открытий ская наб., д.аказ 3853/58 Тираж 37 1 ВНИИПИ Государственного по делам изобретений 113035, Москва, Ж, Рау
СмотретьЗаявка
3233012, 26.01.1981
Пфайзер Инк
ВИЛЛАРД МАККОВАН ВЕЛЧ
МПК / Метки
МПК: A61K 31/437, A61P 25/22, C07D 471/04
Метки: 3виндолов, 4-окси-4-(п, 4а, 9в-гексагидро-1н, 9в-транс-2, гидрохлоридов, замещенных, пиридо4, фторфенил)бутил
Опубликовано: 23.08.1987
Код ссылки
<a href="https://patents.su/5-1333239-sposob-polucheniya-gidrokhloridov-zameshhennykh-2-4-oksi-4-p-ftorfenilbutil-4a-9v-trans-2-3-4-4a-5-9v-geksagidro-1n-pirido4-3vindolov.html" target="_blank" rel="follow" title="База патентов СССР">Способ получения гидрохлоридов замещенных 2 4-окси-4-(п фторфенил)бутил -4а, 9в-транс-2, 3, 4, 4а, 5, 9в-гексагидро-1н пиридо4, 3виндолов</a>
Предыдущий патент: Способ получения производных 2, 6-пиперидиндиона
Следующий патент: Способ получения производных метилендифосфоновой кислоты
Случайный патент: Способ получения полиэфирных слюл