3 -хлор-4 b -окси-24s-этил-5 b -холестан-6-он, обладающий фиторостостимулирующей активностью, и способ его получения
Формула | Описание | Похожие патенты | МПК / Метки | Текст | Заявка | Код ссылки
Номер патента: 1371003
Авторы: Борисова, Быховец, Ковганко, Стрельцова, Хрипач
Формула
1. 3 ![]() -Хлор- 4
-Хлор- 4 ![]() -окси-24S-этил- 5
-окси-24S-этил- 5 ![]() -холестан-6-он формулы
-холестан-6-он формулы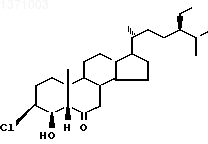
обладающий фиторостостимулирующей активностью.
2. Способ получения 3 ![]() -хлор- 4
-хлор- 4 ![]() -окси-24S-этил- 5
-окси-24S-этил- 5 ![]() -холестан-6-она, заключающийся во взаимодействии 3
-холестан-6-она, заключающийся во взаимодействии 3 ![]() -хлор-24S-этилхолест-5-ена с двуокисью селена при кипячении в диоксане и последующей обработке полученного 3
-хлор-24S-этилхолест-5-ена с двуокисью селена при кипячении в диоксане и последующей обработке полученного 3 ![]() -хлор-24S-этилхолест-5-ен-4
-хлор-24S-этилхолест-5-ен-4 ![]() -ола трифторнадуксусной кислотой в метиленхлориде при комнатной температуре.
-ола трифторнадуксусной кислотой в метиленхлориде при комнатной температуре.
3. Способ по п. 2, отличающийся тем, что процесс проводят при соотношении 3 ![]() -хлор-24S-этилхолест-5-ена и двуокиси селена 1: 1,8, а 3
-хлор-24S-этилхолест-5-ена и двуокиси селена 1: 1,8, а 3 ![]() -хлор-24S-этилхолест-5-ен-4
-хлор-24S-этилхолест-5-ен-4 ![]() -ола и трифторнадуксусной кислоты 1 : 8,8.
-ола и трифторнадуксусной кислоты 1 : 8,8.
Описание
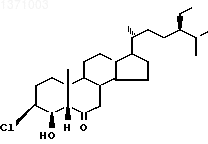 и способу его получения. Соединение (I) проявляет фиторостостимулирующую активность и может быть использовано в практике сельского хозяйства в качестве регулятора роста растений.
и способу его получения. Соединение (I) проявляет фиторостостимулирующую активность и может быть использовано в практике сельского хозяйства в качестве регулятора роста растений.Целью изобретения является получение нового производного
Соединение (I) получают в результате взаимодействия 3
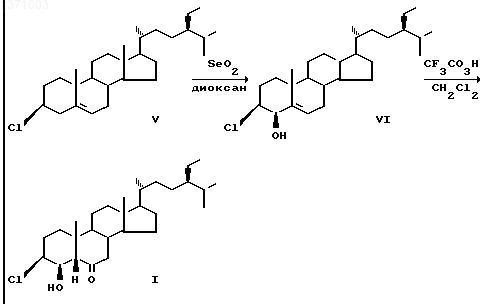
П р и м е р. К раствору 8,5 г (19,6 ммоль) 3 -хлор-24S-этилхолест-5-ена в 250 мл диоксана прибавляют 4,0 г (36 ммоль) двуокиси селена. Реакционную смесь кипятят с обратным холодильником в течение 3,5 ч, после охлаждения до комнатной температуры фильтруют через окись алюминия.
Фильтрат упаривают в вакууме и остаток подвергают колоночной хроматографии на силикагеле, алюируя смесью гексана с эфиром (25: 1). Получают 3,35 г (7,46 ммоль, 38% ) 3
Найдено, % : С 77,58; Н 11,17; Сl 7,60.
C29H49OCl
Вычислено, % : С 77,55; Н 11,00; Cl 7,89.
М. м. 449, y. e.
ИК-спектр (KBr), см-1: 3550 (OH).
Спектр ПМР (100 МГц, CDCl3,
К раствору 0,78 г (1,7 ммоль) 3
Найдено, % : C 74,90; Н 10,60; Cl 7,80.
С29Н49O2Cl
Вычислено, % : C 74,88; Н 10,62; Cl 7,62.
М. м. 465,16 y. e.
ИК-спектр (KBr), см-1: 3550 (OH), 1712 (C= O).
Спектр ПМР (360 МГц, CDCl3,
Изучение биологической активности 3
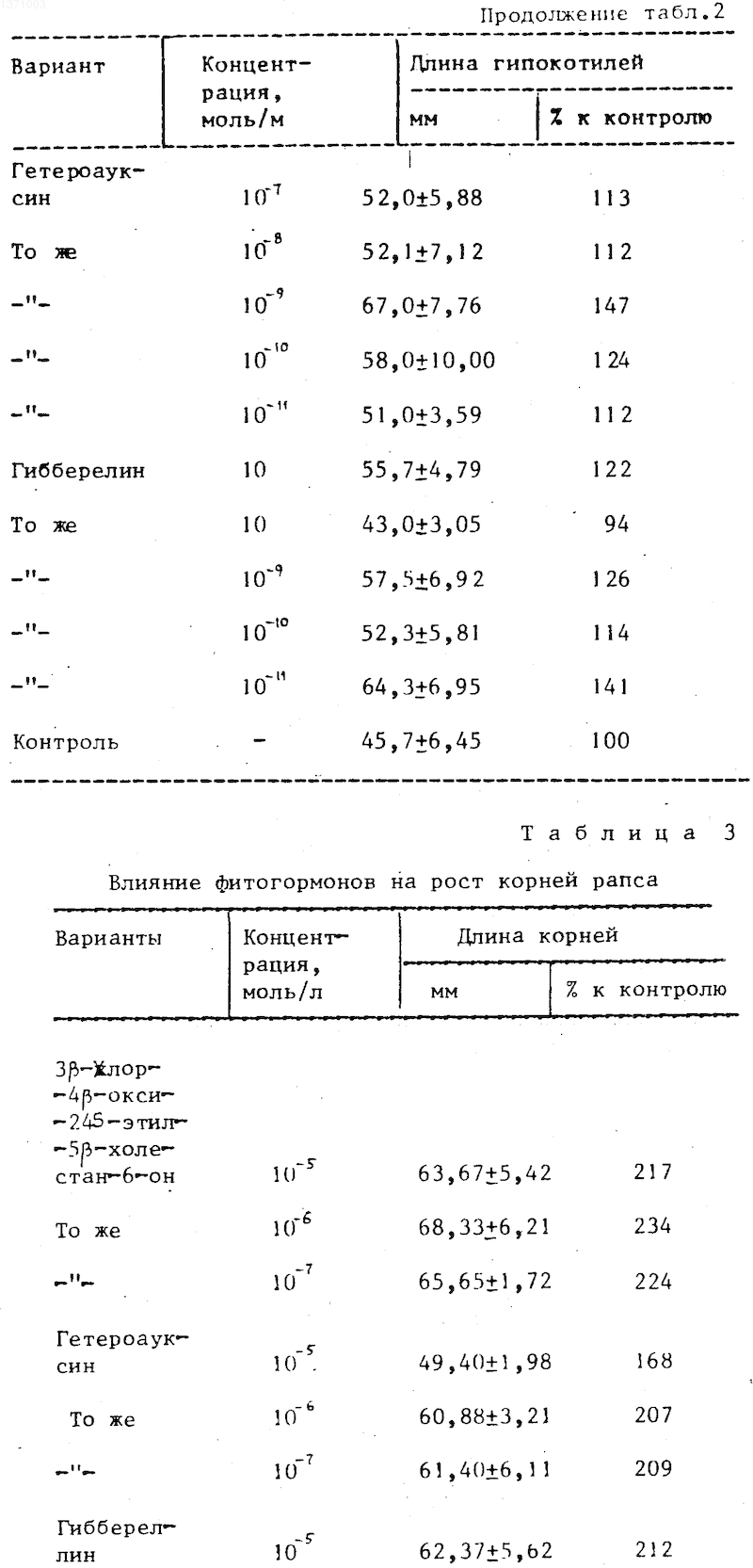
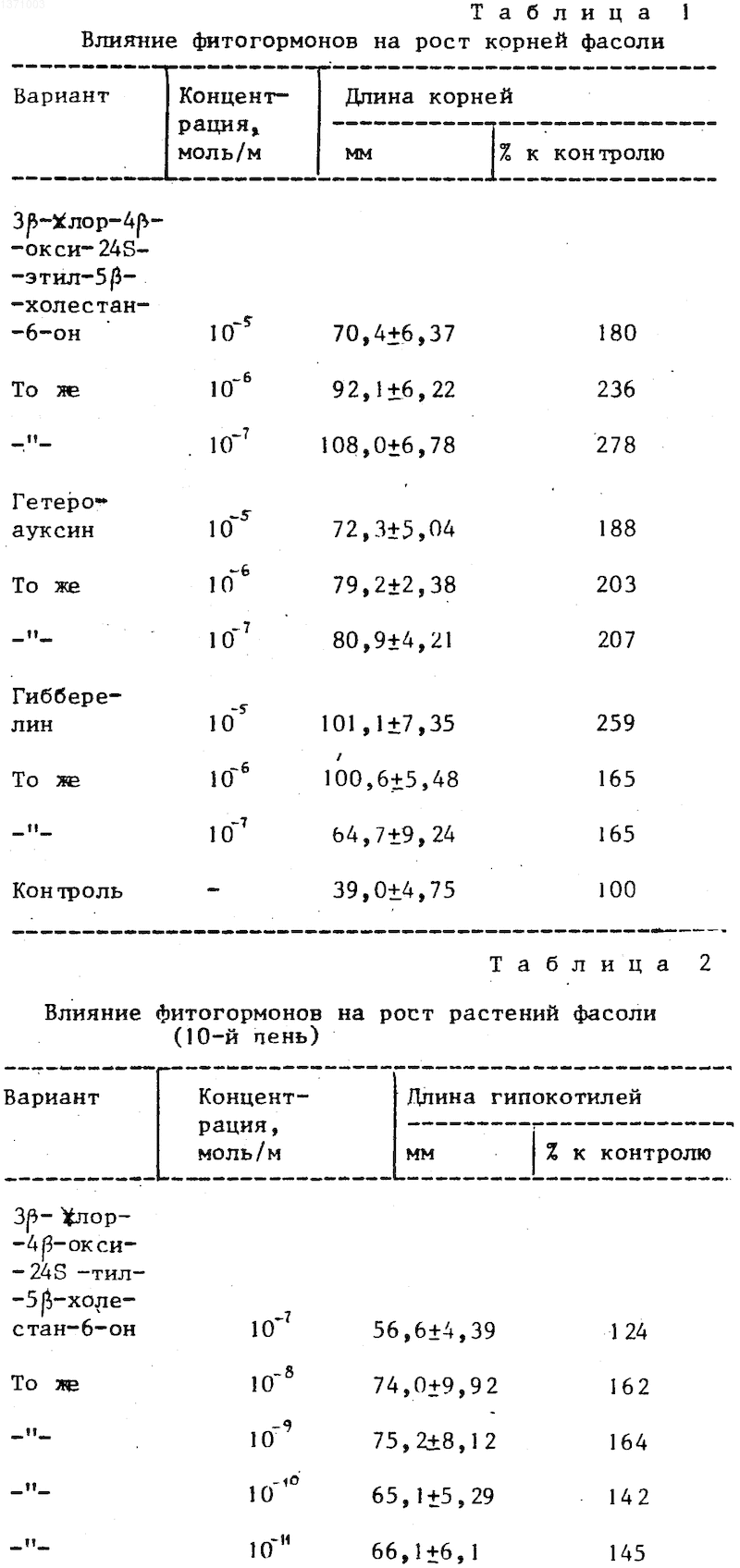
Рост корней фасоли. По 10 семян фасоли помещали в чашки Петри и приливали по 10 мл раствора с исследуемыми веществами. Закрытые чашки помещали в темноту при 24оС на 7 дней. По истечении этого срока измерили длину корней фасоли. Результаты испытаний приведены в табл. 1.
Рост фасоли. По 10 семян фасоли помещали в чашки Петри и приливали по 10 мл раствора, содержащего исследуемые вещества. Чашки ставили на сутки в темноту, затем замоченные семена высаживались по три в стаканчики с почвой. Дальнейшее прорастание и рост проростков проходили при 12-часовом фотопериоде при искусственном освещении в течение 10 суток. Измеряли длину гипокотилей фасоли. Результаты приведены в табл. 2.
Тест с растениями рапса. Использовали рапс сорта Ольга. Семена проращивали двое суток в темноте, затем переносили в чашки Петри с растворами исследуемых соединений. Вносили по 2 мл раствора и по 10 семян рапса в чашку диаметром 4 см. Дальнейший рост проходил на свету в течение 3 суток. Измеряли длину корней рапса. Результаты измерений приведены в табл. 3.
Как видно из представленных в табл. 1-3 данных, описываемое соединение 3
3
Описываемый способ позволяет получить новое производное
Carlisle D. B. , Osborne D. J. , Ellis P. E. , Moorhouse J. E. Reciprocal effect of insect and plant growth substances. - Nature, 1963, v. 200, N 4912, p. 1230.
Мельников Н. Н. и др. Справочник по пестицидам. М. : Химия, 1985, с. 36.
Sharplees K. B. , Michaelson R. C. Higt stereo and regioselectivities in the transition metal catalyzed epoxidation of olefinic alcohols by tert-butyl hydroperoxide. - J. Am Chem. Soc. , 1973, v. 95, N 18, p. 6136-6137.
Shoppee C. W. Steroids and Walden intersion; IV, Derivatives of 6-Ketositostane and 6: 17-diketoandroctane. - J. Chem. Soc. , 1948, N 7, p. 1043-1045.
Изобретение касается замещенных стероидов, в частности получения 3b-хлор- 5b-окси-24S-этил-5b- холестан-6-она (ХН), который обладает фиторостостимулирующей активностью и может быть использовано в сельском хозяйстве. Цель изобретения - создание нового более активного соединения указанного класса. Синтез ХН ведут окислением 3b-хлор-24S- этилхолест-5-ена (I) двуокисью селена (II) при кипячении в среде диоксана с последующей обработкой трифторнадуксусной кислотой (III) в среде метиленхлорида при комнатной температуре. Целесообразно использовать соотношение I и II, равное 1: 1,8, а соединение III использовать в 8,8-кратном избытке по отношению к промежуточному продукту окисления. Выход ХН 65% , т. пл. 194 - 196С (гексан), брутто ф-ла C29H49O2Cl. ХН проявляет активность в отношении роста фасоли, рапса, аналогичную гиббереллину A3 и гетероауксину IV, но в 10 раз лучше известного
Рисунки
Заявка
4007020/04, 10.01.1986
Институт биоорганической химии АН БССР
Хрипач В. А, Ковганко Н. В, Быховец А. И, Борисова М. П, Стрельцова В. А
МПК / Метки
МПК: A01N 29/00, C07J 9/00
Метки: активностью, обладающий, окси-24s-этил-5, фиторостостимулирующей, хлор-4, холестан-6-он
Опубликовано: 30.01.1994
Код ссылки
<a href="https://patents.su/0-1371003-3-khlor-4-b-oksi-24s-ehtil-5-b-kholestan-6-on-obladayushhijj-fitorostostimuliruyushhejj-aktivnostyu-i-sposob-ego-polucheniya.html" target="_blank" rel="follow" title="База патентов СССР">3 -хлор-4 b -окси-24s-этил-5 b -холестан-6-он, обладающий фиторостостимулирующей активностью, и способ его получения</a>
Предыдущий патент: Устройство для измерения параметров движения воздушного потока
Следующий патент: Свч-логическое устройство
Случайный патент: Натяжная звездочка для цепной передачи