Способ получения замещенных дибензиловыхэфиров или их кислотно-аддитивных солей
Похожие патенты | МПК / Метки | Текст | Заявка | Код ссылки
Текст
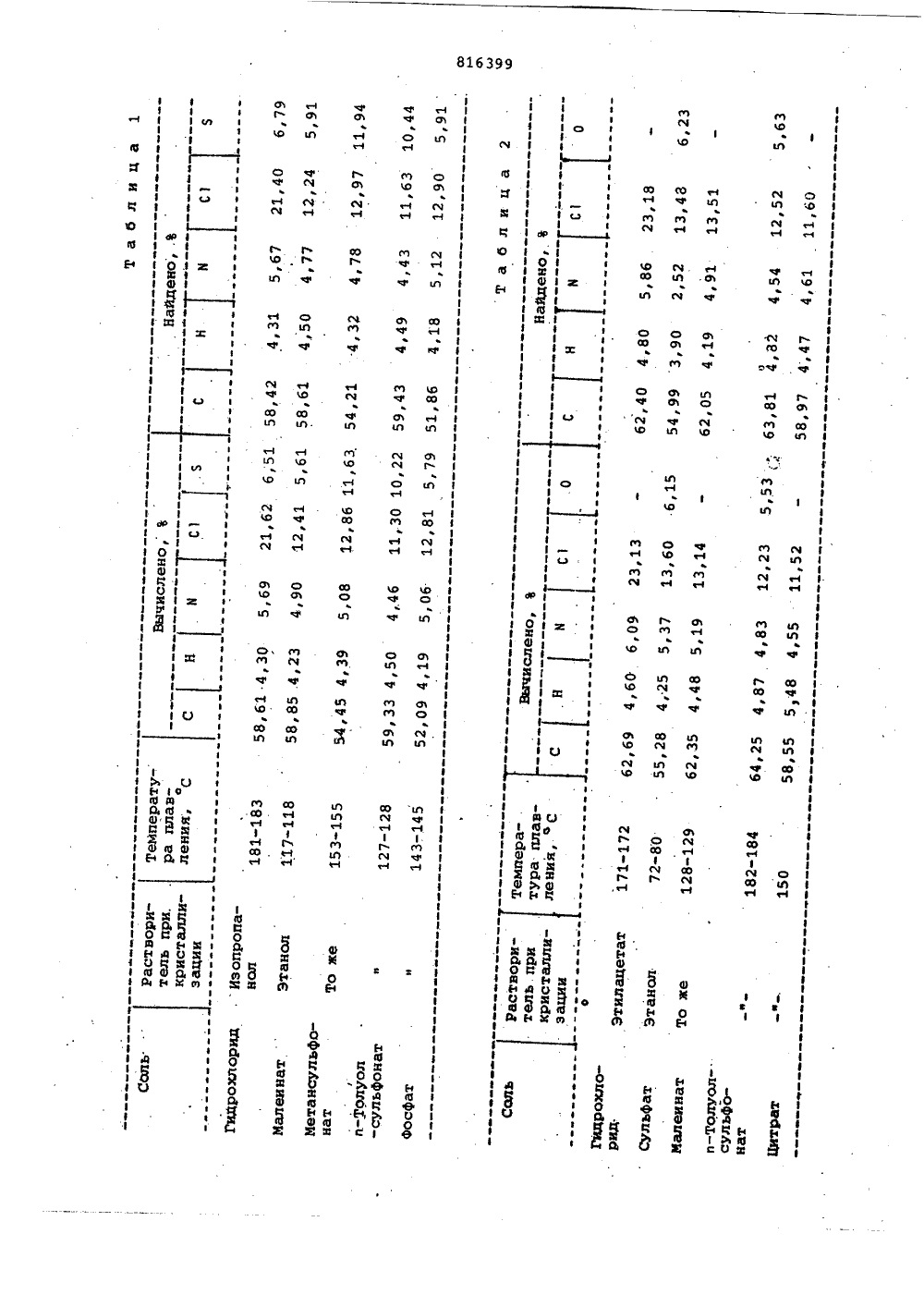
ОПИСАНИЕИЗОБРЕТЕНИЯК ПАТЕНТУ он 816399 Союз Советских Социалистических Республик(23) Приоритет - (32) 18. 05, 78 Государственный комитет СССР но делам изобретений и открытийДата опубликования описания 230381 Иностранцы Нарди, Елена Массарани, Альберто и Марио Веронезе(72) Авторы изобретени ан 3 с.к Коьщани Иностранная Фирма и С.А Кемккал энд ФармасьюРе 1) Заявитель СПОСОБ ПОЛУЧЕНИЯЗАМЕЩЕННЫХ ДИБЕНЗИЛОВЫХ ЭФИРОВ ИЛИ ИХ КИСЛОТНО-АДДИТИВНЫХ СОЛЕЙ 2) -этанол подвергаюгалондбензилом Фор ондены относится к способу х эамещенных дибензили их кислотно- орые могут найти стве физиологичес нений, обладающих й активностью, в промышленности.й способ получения зазиловых эфиров осноой реакции конденсаких оксисоединений с н переводе их иэвестсоли.тения - разработка ния эфиров или их солилме сацни аддитивпри- ки- ан- Фарспособа полу лей.Поставлен что в спосо дибензиловых достигается тем,ения эамещенныхобщей формулы я це пол фиросн-о-сн .СР Ц 25 ли СЬНВЪ, о-аддитивных солей,рфенил)"2-(й-имидазо г Сб Нб кисло4 -дихл Изобретение получения новы ловых эфиров и ных солей, кот менение в каче активных соеди тибактериально мацевтической Предлагаемы мещенных дибен ван на известн ции ароматичес галоидбензилом ным способом в Цель изобре чегде йС Н Х и С 1, Вг в среде карСбоксамида в присутствии гидрида щелочного металла, или в среде алифатического спиРта Сз-Сб в пРисУтствии алкоголята щелочного металла с выделением целевого продукта в виде ос" нований или их солей.В качестве карбоксамидов используют днметилформамид, гексаметнлфосфорамид, но конденсация протекает более полно, если используют диметилсульфоксид. Это приводит к более высокому выходу и к получению более чистого продукта. Полученное при кондея" сацин основание не подвергают очистке хроматографией, потому что очистка является необходимой только прк применении в качестве растворителей днметилформамкда или гексаметилфосфорамида. Фильтрование раствора основания через колонку с силикагелем приводит к задержанию неболыаих количеств примесей. В случае соединенияв котором аимвол и представляет816399собой фенильную группу, Фильтрование тилформамид Са. месь нагревают доне является необходимям и кристалли-120 С и выдерживают при этойзация нитрата приводит к получению температурере в течение 20 мин, и поспродукта, достаточно чистого для фар- ле последующегоего охлаждения до 40 С,4мацевтических целей. При применении при энергичнгичном перемешивании прибав 5описанных апротонных растворителей ляют 2500 млмл ледяной воды, Продукт,употребляют гидрид щелочного металла, осадившийсяся при перемешивании в течекоторый способен образовывать соль с ние периодапериода времени около 2-х ч осгидроксильной группой производного вобождают от ве хнют от верхнего слоя жидкости,который декантируют, прибавляют ещеРастворитель, используемый при 2500 мл водымл воды и, после выдержки, смеськонденсации, представляет собой али- " фильтруют. П олученный осадок сушатфатический спирт, содержащий от 3о 6и кристалс аллизуют из толуола. Придо углеродных атомов, такой, кактетбтнэтом получают 170ают г целевого продуктрет- утанол,и в этом случае гидрид та, плавящегося при 134-135 С.щелочного металла заменяют алкоголя- Найдено Ъ: С 51 62том щелочного металла, например, трет й 10,73, С 27,76.Н 3,80,бутилатом калия, С Н С й 0Кислотно-аддитивные соли замещен- Вычислено,Ъ: С 51,38, Н 3,92,10.ных дибензиловых эфиров получают из- й 10,89, С 27,58.вестным способом, например путем при- П р и м е р э. 2,4"Дихлор",фебавления к основанию эквимолекуляр нилтио- -(й-ими аного количества кислоты с после юнилтио- - й-имидазолилметил) -дибенты с последую- зиловый простой эфир (1:й =: СН 5щей кристаллизацией полученной таким аствор 2,57 г 1-(2 ,4 - иобразом соли из подходящего раство- ф )- -((, -дихлоррителя , ,1енил -2- й-имидазол) -этанола вР10 мл гексаметилфосфорамида прибавИсходных 1-(2 ,4 -дихлорфенил)-2-(й-имидазолил)-этанол получают .ляют по каплям, при 25 ф С к сч ют из зии 0,52 г гидрида нат ия (50 р ф , к суспен 1-хлорацетил,4-дихлорбензола путем раствор в масле) в 5 мл гексаметивосстановления последнего боргидри- осуорамида. После прекращения вы е- аметилдом натрия и последующей конденсаци- ления водо о а обей с имидазолилом.и- ления водорода, образование соли завершают путем нагревания в течениер и м е р 1. 1-(2 ,4 -Дихлор ч при 50 С. После офенил)-2-хлорэтанол.осле охлаждения до49,5 г боргидрида натрия медлен 25 С, прибавляют 2,58 г 1-4- е-хлорметилно прибавляют небольшими порциями к-Фенилтиобензола. Темпе тратуру посуспензии 233 г 1-(1 -окси-хлорок вышают до 50 С и смесь в еыд рживаютэтил)-2,4-дихлорбензола в 1 л метано- Ыпри этой температ е вур течение 12 ч.ла, перемешиваемого при комнатнойПо завершении реак иир ц и, смесь выливатемпературе. Полученный раствор пе еют в 200 мл во ы п од , р дукт экстрагимешивают при комнатной температуреере- руют диэтиловым эфи омр , раствориеще 2 ч и после этого в 1тель выпа ив тр аю и остаток дважды очиыливают в л щают на колонке силикаг5 н. соляной кислоты, охлажденной 40 е силикагеля, с испольльдом. После экстракции этила етато зованием в качестве элюента этилацеили хлороформом, экстракт промываютразличных фракцийводой, 1 н. раствором гидрата окисиметодом тонкослойной х оматр ографии.натрия и снова водой до нейтральнойРастворитель выпа ивают изреакции, и наконец, насыщенным растФракций, для получения 2 4 гния ., г целевовоРом хлористого натрия, Экстрактл го основания в о мф р е желтоватого масла, дающего одно пятно на тонкослойсушат, растворитель выпаривают и получают 220 г ма лной хроматограмме.г масла. Масло застывает Найдено,%: С 63,86, Н 4,24,й б 41при выдержке и полученное твердоевещество плавится при 48-51 О С.С 47,43.Найдено,Ъ: С 42,75, Н 3,19, ВйчислейоС 63 30Н 4,44,й 6 13, С 15 57, 5 7048 "7 3Вычислено,В: С 42,61, Н 3,13,П р и м е р 4. 2,4-Дихлор- С 47,17.-(- -ю из , г третмл трет-бутанола885 ги30 г натрия прибавляют к раствору готовят при 20-25 С в атмосферепосле этогог имидаэола и 600 мл метанола, азота. Прибавляют 3 86 1- (раатворитель выпарива- -дихлорфенил) -2- ( й-иг -2,4ют. Остаток растворяют в 300 в . 60т в мл ди-. ла. Раствор нагревают п и теметилформамида и нагревают до 115- ре кипения с об атн120 С. К полученному растворе кипения с обратным холодильникомму раствору при- в течение 1 ч и затем охла а тбавляют по каплям и при перемешива онии, раствор 225 г 1-(2С. П ибавляри авляют 3,03 г 4-хлормефенил)-2-хлороэтанола в 400г - ,4 -дихлор- тилбифенила и аствор ор снова нагревамл диме ют при температуре кипения с обратным холодильником в течение 5 ч После охлаждения до 20-25 С смесь выливают в воду и основание экстрагируют этилацетатом, Экстракт промывают диэтиловым эфиром и растворитель выпаривают. Остаток растворяют в диэтиловом эфире (80 мл) и оставляют на ночь. НераствориЬие вещества отфильтровывают и фильтрат обрабвйывают азотной кислотой, растворенной в диэтиловом эфире. При этом получа" ют масло, застывающее нри выдержке.Остаток, состоящий из нитрата 2.,4- -дихлор-фенил-с 4-(М-имидазолил-метил)-дибензилового эфира, кристаллизуют из этанола или этилацетата.Продукт (4,3 г) является чистым, что до-казывается методом тонкослойной хроматографии и плавится при 140"141 С.Найдено,: С 59,17, Н 4,14,й 8,61, С) 14,46.СЙ Н С)ОНио ., 2 ОВычислено,%3 С 59 у 25Н 4,35 ф й 8,64, С) 14,57.П р и м е р 5. К раствору 3,86 г 1-(2 ,4 -дихлорфенил)-2-(М-имидазолил)-этанола в 15 мп диметилсульфоксида (высушенного над гидридом кальция ) прибавляют 0,66 г гидрида натрия в атмосфере азота, при 20-25 С.Смесь нагревают при 50-60 С до прекращения выделения газа. После этого смесь охлаждают до 20-25 С, прибав" ляют 0,5 г.иодистого калия и раствор 3,03 г 4"хлорметилбифенила в 7 мп диметилсульфоксида (высушенного над гидридом кальция), вводимый по каплям. Смесь перемешивают примерно в течение 20 ч при 20-25 С и после этого выливают в воду. Продукт экстрагируют этилацетатом и после этого обрабатывают, как описано,Выход составляет 4,6 г.Соли 2,4-дихлор-фенилтио-о- -(Й-имидазолнл-метил-дибензилового простого эфира получают путем взаимодействия свободного основания, растворенного в этаноле, со спиртовым раствором желательной. кислоты с последукщей кристаллизацией полученной соли в подходящем растворителе. Сво- бодное основание готовят в соответствии с примером 3В табл. 1 приведены растворители, используемые для кристаллизацин,данные элементарного анализа и температуры плавления некоторых солей соединений формулыгде В -5 С Н,В табл. 2 приведены некоторыеФ данные для рада солей 2,4-дихлор-фенил-о-(й-имидазолил-метил)-дибензилового простого эфира, полученных в соответствии с приведенными примерами., й) ГдЕ й - СН- илн С Н Ьили их кислотно-аддйтйвных солей, о т л и ч а ю щ и й с я тем, чтоСоставитель В. МеркуловаРедактор С. Патрушева Техред Т.Маточка Корректор М. Демчик Заказ 1058/94 Тираж 443 Подписное ВНИИПИ Государственного комитета СССР по делам изобретений и открытий 113035, Москва, Ж, Раушская наб.; д. 4/5филиал ППП Патент", г. Ужгород, ул. Проектная, 4Способ получения замещенных дибензиловых эфиров общей формулысРси- о-сй 5И ) й)30 1-(2,4 -дихлорфенил)2-(й-имидазолилчметил)-этанол подвергают конденсации с галондбензилом формулы где й. СИ, 4;ВМ 5 Х С 1, Вг,в среде карбоксамида в присутствиигидрида щелочного металла или всреде алифатичесмого спирта С -С 4 вприсутствии,алкоголятащелочногометалла с выделением целевого продукта в виде оснований или солей.
СмотретьЗаявка
2771698, 17.05.1979
ДАНТЕ НАРДИ, ЕЛЕНА МАССАРАНИ, АЛЬБЕРТО ТАЙАНА, МАРИО ВЕРОНЕЗЕ
МПК / Метки
МПК: C07D 233/60
Метки: дибензиловыхэфиров, замещенных, кислотно-аддитивных, солей
Опубликовано: 23.03.1981
Код ссылки
<a href="https://patents.su/5-816399-sposob-polucheniya-zameshhennykh-dibenzilovykhehfirov-ili-ikh-kislotno-additivnykh-solejj.html" target="_blank" rel="follow" title="База патентов СССР">Способ получения замещенных дибензиловыхэфиров или их кислотно-аддитивных солей</a>
Предыдущий патент: Способ получения 4-2-(пиразол-1-карбонамид)-этил бензолсульфонил-мочевин
Следующий патент: Способ получения производныхтиазолидинкарбоновых кислот
Случайный патент: Устройство для отключения цепей постоянного тока