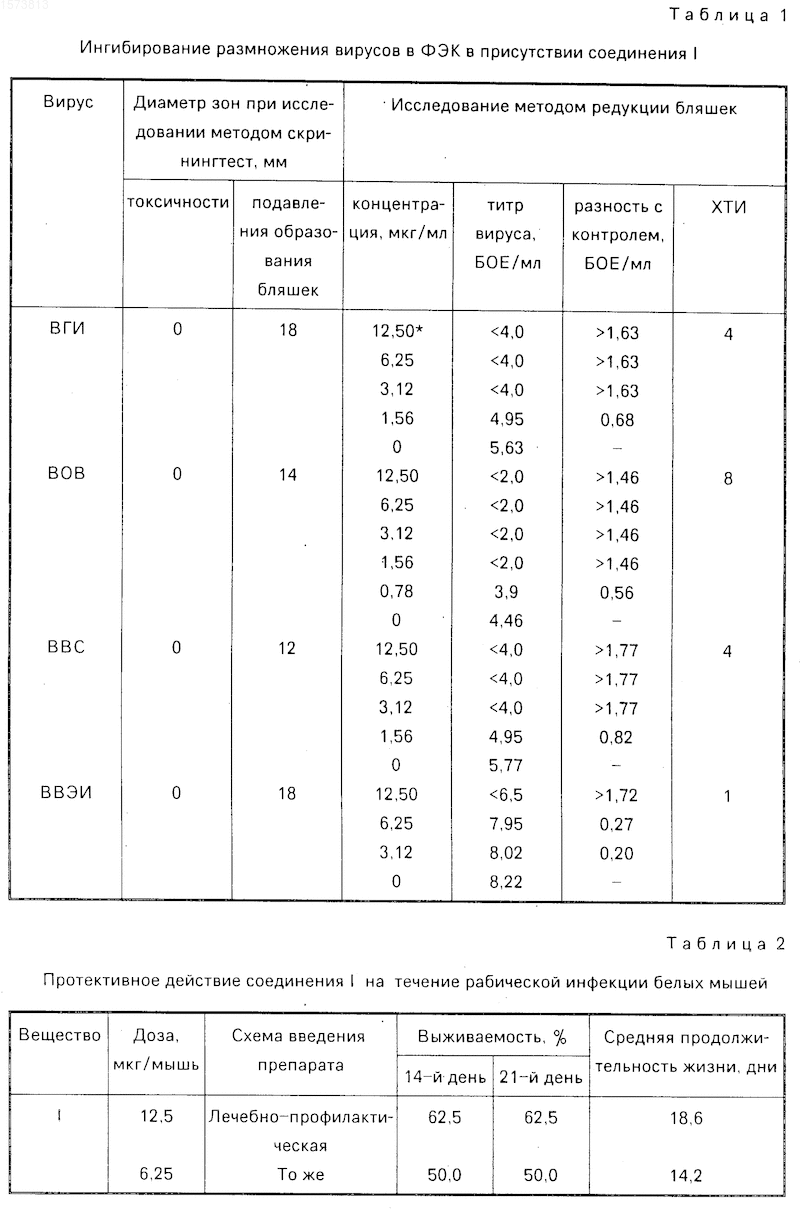
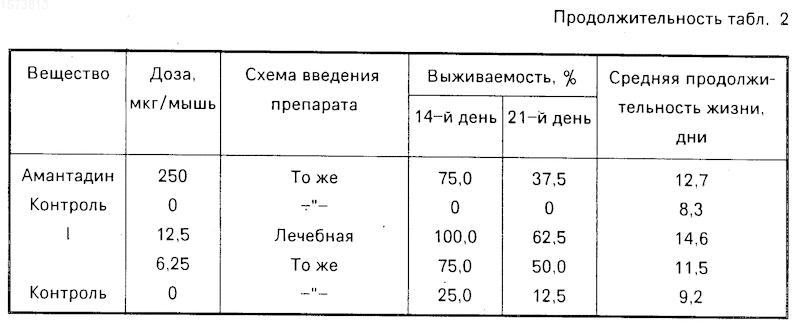
1-фенил-3-окси-4-этоксикарбонил-5-п-бромфенил-2, 5 дигидропиррол-2-он, проявляющий противовирусную активность
Формула | Описание | Похожие патенты | МПК / Метки | Текст | Заявка | Код ссылки
Номер патента: 1573813
Авторы: Андрейчиков, Бореко, Владыко, Вотяков, Гейн, Згировская, Зубович, Коробченко, Мишаева, Тарасенко, Шумиловских
Формула
1-Фенил-3-окси-4- этоксикарбонил-5-п-бромфенил -2,5-дигидропиррол-2-он формулы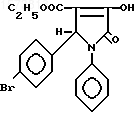
проявляющий противовирусную активность.
Описание
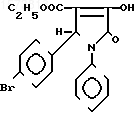 которое проявляет противовирусную активность и может быть использовано в медицине.
которое проявляет противовирусную активность и может быть использовано в медицине.Целью изобретения является поиск в ряду пирролонов новых соединений, обладающих широким спектром высокой противовирусной активности, превосходящей активность известных противовирусных препаратов.
П р и м е р. 1-Фенил-3-окси-4-этоксикарбонил-5-n-бромфенил-2,5-дигидропиррол-2-он (I).
К раствору 3,0 г (0,0159 моль) диэтилового эфира щавелевоуксусной кислоты в 5 мл этанола прибавляют смесь из 2,95 г (0,0159 моль) n-бромбензальдегида и 1,45 мл (0,0159 моль) анилина в 10 мл этанола. Реакционную смесь выдерживают при 20оС в течение 24 ч, выпавший осадок отфильтровывают, перекристаллизовывают из толуола и получают 3,2 г (50%) целевого продукта. Т. пл. 191-193оС.
Найдено, С 56,84; Н 3,98; Br 19,61; N 3,31.
С19Н16BrNO4
Вычислено, С 56,72; Н 4,01; Br 19,83; N 3,48.
В ИК-спектре соединения I, снятом в вазелиновом масле, присутствуют полоса поглощения С=С-двойной связи при 1655 см-1, полосы поглощения лактамного карбонила при 1680 см-1, сложноэфирного карбонила при 1705 см-1 и енольного гидроксида при 3312 см-1.
В ПМР-спектре, снятом в CDCl3, присутствуют триплет и квадруплет протонов этоксигруппы при 1,15 и 4,07 м.д. синглет протона в положении 5 гетероцикла при 5,43 м.д. и мультиплет ароматических протонов при 7,25 м.д.
Соединение I испытывали на противовирусную активность в отношении вирусов везикулярного стоматита, герпеса простого, осповакцины, венесуэльского энцефаломиелита лошадей, бешенства и клещевого энцефалита.
При проведении испытаний использовали тканевую культуру первично-трипсинизированных фибробластов эмбрионов кур (ФЭК) производства отдела культур клеток БелНИИЭМ, выращенную на 5%-ном гемогидролизате, беспородных белых мышей-сосунков обоего пола, вирусы осповакцины (ВОВ), герпеса простого I типа (ВГП), везикулярного стоматита (ВВС), венесуэльского энцефаломиелита лошадей (ВВЭЛ), вакцинного бешенства, клещевого энцефалита (КЭ), клещей.
Культуры ФЭК, выращенные на чашках Петри и дне пенициллиновых флаконов, отмывали от ростовой среды средой 199, наносили 0,00002 БОЕ/клетка ВОВ, ВГП, ВВС и ВВЭЛ в среде 199. После часового контакта вируссодержащую жидкость удаляли и наносили покрытие на основе среды 199, включающее 1% бактоагара; 0,005 нейтрального красного, антибиотики. Для культур, выращенных на дне пенициллиновых флаконов, в состав покрытия добавляли соединение I с тем, чтобы его конечная концентрация составила 12,50 мкг/мл и менее (метод редукции бляшек). После застывания агарового покрытия на чашках Петри вырезали лунки на всю глубину слоя. В лунки устанавливали мерные (0,05 мл) отрезки стеклянной трубки, заполненные взвесью излучаемого вещества (скрининг-тест). После 48-часовой инкубации культур сосчитывали количество бляшек (при исследовании методом редукции бляшек) или измеряли диаметр концентрических зон токсичности и подавления образования бляшек (при исследовании методом скрининг-теста). Титр вируса рассчитывали, исходя из количества бляшек.
Токсические свойства соединения I для ФЭК исследовали на культурах, выращенных на боковой стенке флаконов из-под антибиотиков. Вещество разводили на среде 199 с добавлением 1% диметилсульфоксида и наносили на отмытые от ростовой среды клетки. Инкубацию вели 96 ч, после чего регистрировали цитопатическое действие изучаемого соединения при малом увеличении микроскопа. Затем в поддерживающую среду добавляли 0,1 мл 0,1%-ного водного раствора нейтрального красного на 1 ч, клетки трижды отмывали раствором Хенкса без фенолового красного, заливали на 1 ч этанолом и оценивали степень поглощения нейтрального красного клетками по оптической плотности. Последнюю измеряли на СФ-26 при 510 нм. Максимальной толерантной концентрацией (МТД) считали наивысшую дозу соединения I, не вызывающую изменений клеточной морфологии и нарушения поглощения красителя.
Критерием антивирусного действия служили наличие и величина зоны подавления образования бляшек, снижение титра вирусов в присутствии различных концентраций соединения. Минимальной активной концентрацией (МАК) считали дозу, в присутствии которой регистрировалось снижение титра вируса на величину, соответствующую не менее 1,25 lg БОЕ/мл. Химиотерапевтический индекс (ХТИ) высчитывали как отношение МТД/МАК.
В экспериментах на животных использовали дозу вируса КЭ и бешенства, соответствующую 10 LD50/0,25 мл. Инфицирование проводили подкожно, суспензию вируса готовили на среде 199. Раствор соединения I на бидистиллированной воде с добавлением 25%-ного диметилсульфоксида вводили мышам подкожно в дозах 12,5 и 6,25 мкг/жи- вотное за 24 и 1 ч до заражения и еще в течение трех дней после него один раз в день (лечебно-профилактическая схема) или в течение 5 дней по одному разу в день, начиная с дня инфицирования (лечебная схема).
Наблюдение за мышами вели в течение 21 дня. Об эффективности соединения судили по увеличению выживаемости в сравнении с контрольной группой. Животным контрольной группы вводили растворитель.
Исследования на животных выполняли одновременно с известным противовирусным препаратом амантадином. Оба вещества исследовали в каждом эксперименте параллельно. Использовали водный раствор амантадина.
В экспериментах на тканевой культуре установлено, что соединение I обладает способностью подавлять размножение ВГП, ВОВ, ВВС и ВВЭЛ (см. табл.1).
При этом в отношении ВОВ он проявляет высокую активность, в отношении ВГП и ВВС среднюю. Значимое снижение титра ВВЭЛ отмечено только в присутствии соединения в концентрации, соответствующей МТД.
В опытах на животных соединение I обеспечивает высокий защитный эффект, достигающий 62,5% снижения летальности мышей и увеличения продолжительности их жизни до 5,4-10,3 дней (см. табл.2).
В экспериментах на белых мышах, зараженных вирусом КЭ, соединение I также проявило четко выраженное протективное действие. Выживаемость животных на 7 сутки составила 87,5% при 100% гибели контроля, продолжительность жизни возросла в 1,5 раза.
В крови белых мышей, получавших 1-фенол-3-окси-4-этоксикарбонил-5-n-бромфе- нил-2,5-дигидропиррол-2-он (I), подавлялось размножение вируса КЭ более чем в 100 раз. Если в контроле у животных развивалась напряженная вирусемия (4,25 lg LD50/0,03 мл), то у подопытных животных титр вируса в крови был 2,0 lg DD50. Известно, что при арбовирусных инфекциях, таких как КЭ, при низком уровне вирусемии преpывается диссеминация возбудителя через питающихся иксодовых клещей, которые являются переносчиками и длительными хранителями вируса КЭ. В экспериментах, где на зараженных вирусом КЭ животных, получивших соединение I, подсаживали для питания личинки иксодовых клещей, последние получали ничтожную дозу вируса, на 2,25 lg LD50 меньшую, чем в контроле. Более того, под влиянием соединения I сами клещи погибали в 68,8% случаев. Следовательно, соединение I не только ингибирует вирус КЭ в организме животных, но и подавляет интенсивность циркуляции названного арбовируса между позвоночными животными и переносчиками кровососущими членистоногими.
Таким образом, соединение I обладает способностью подавлять размножение вирусов простого герпеса, осповакцины, везикулярного стоматита, венесуэльского энцефаломиелита лошадей. Оно высокоэффективно ингибирует указанные вирусы, ХТИ для вируса осповакцины составляет 8, а для вирусов простого герпеса и везикулярного стоматита 4. Активность соединения I превосходит активность известного препарата амантадина в 4 раза.
Кроме того, соединение I эффективно защищает лабораторные животные от инфекции, вызванной вирусом бешенства. На 100 62,5% снижается летальность животных и увеличивается продолжительность их жизни до 5,4-10,3 дней.
Изобретение относится к гетероциклическим соединениям, в частности к 1-фенил-3-окси -4-этоксикарбонил-5-n-бромфенил - 2,5-дигидропиррол -2-ону, который проявляет противовирусную активность и может быть использован в медицине. Цель - выявление более активных соединений указанного класса. Получение ведут реакцией диэтилового эфира щавелевоуксусной кислоты со смесью n-бромбензальдегида и анилина в спирте при комнатной температуре. Выход 50%, т. пл. 191 - 193oС. Брутто-ф-ла C19 h16 BrNO4. Новое соединение подавляет размножение вирусов простого герпеса, осповакцины, везикулярного стоматита, венесуэльского энцефаломиелита лошадей. Активность превосходит активность амантадина в 4 раза. Кроме того, новое соединение защищает лабораторных животных от инфекции, вызванной вирусом бешенства. Защитный эффект при лечении соединением состоит из 100 - 62,5% снижения летальности животных и увеличения продолжительности их жизни до 5,4 - 10,3 дней. 2 табл.
Рисунки
Заявка
4495712/04, 17.10.1988
Пермский фармацевтический институт, Белорусский научно-исследовательский институт эпидемиологии и микробиологии, Пермский государственный университет им. М. Горького
Андрейчиков Ю. С, Гейн В. Л, Шумиловских Е. В, Владыко Г. В, Бореко Е. И, Мишаева Н. П, Зубович И. К, Вотяков В. И, Коробченко Л. В, Згировская А. А, Тарасенко А. Б
МПК / Метки
МПК: A61K 31/40, C07D 207/38
Метки: 1-фенил-3-окси-4-этоксикарбонил-5-п-бромфенил-2, активность, дигидропиррол-2-он, противовирусную, проявляющий
Опубликовано: 27.05.1996
Код ссылки
<a href="https://patents.su/0-1573813-1-fenil-3-oksi-4-ehtoksikarbonil-5-p-bromfenil-2-5-digidropirrol-2-on-proyavlyayushhijj-protivovirusnuyu-aktivnost.html" target="_blank" rel="follow" title="База патентов СССР">1-фенил-3-окси-4-этоксикарбонил-5-п-бромфенил-2, 5 дигидропиррол-2-он, проявляющий противовирусную активность</a>
Предыдущий патент: Способ определения амплитудно-временных параметров однократного электрического импульса
Следующий патент: Способ определения электромагнитных параметров вещества
Случайный патент: Жатка