Способ получения 4-замещенныхимидазо1, 2-a-хиноксалинов илиих солей
Похожие патенты | МПК / Метки | Текст | Заявка | Код ссылки
Текст
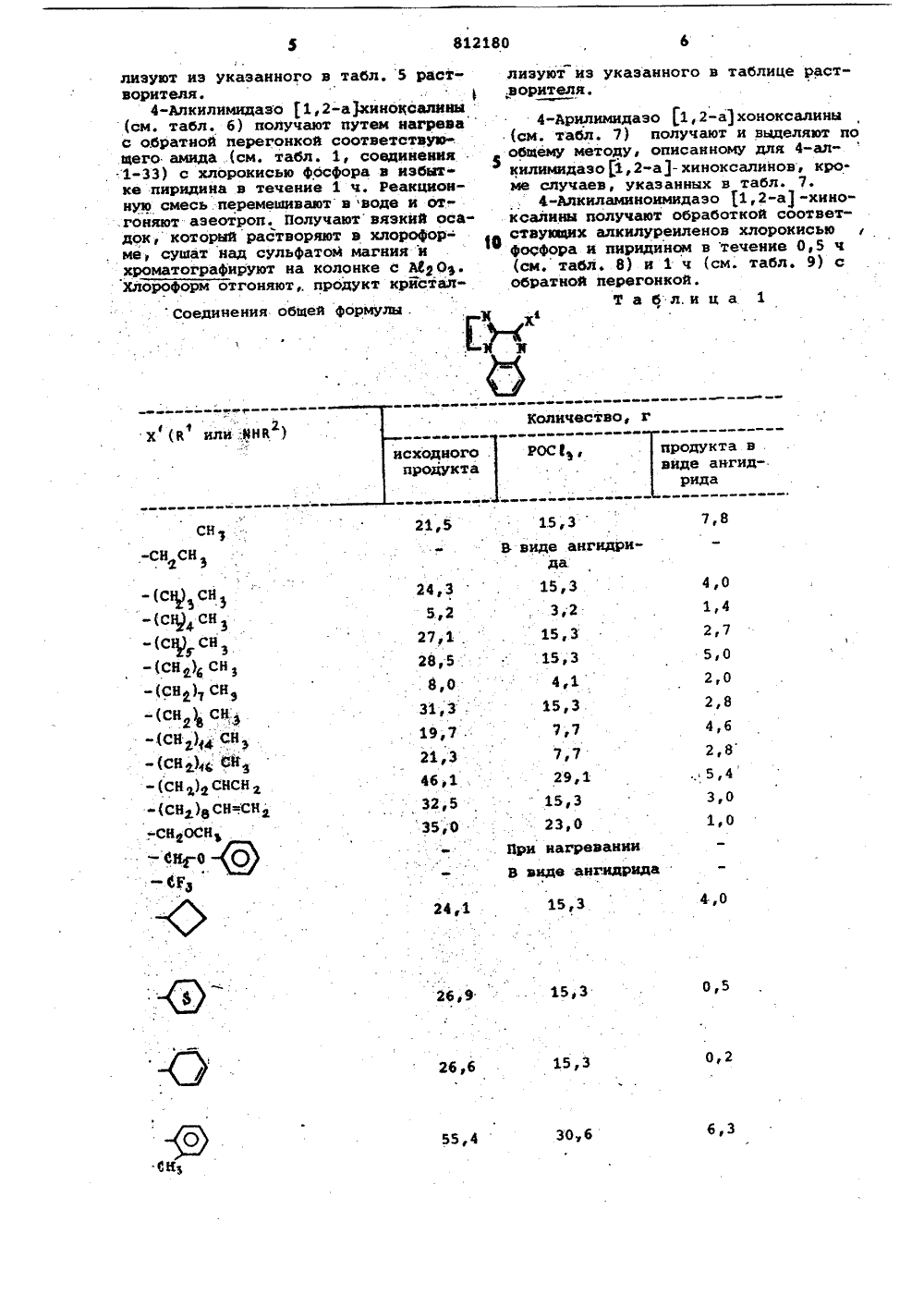
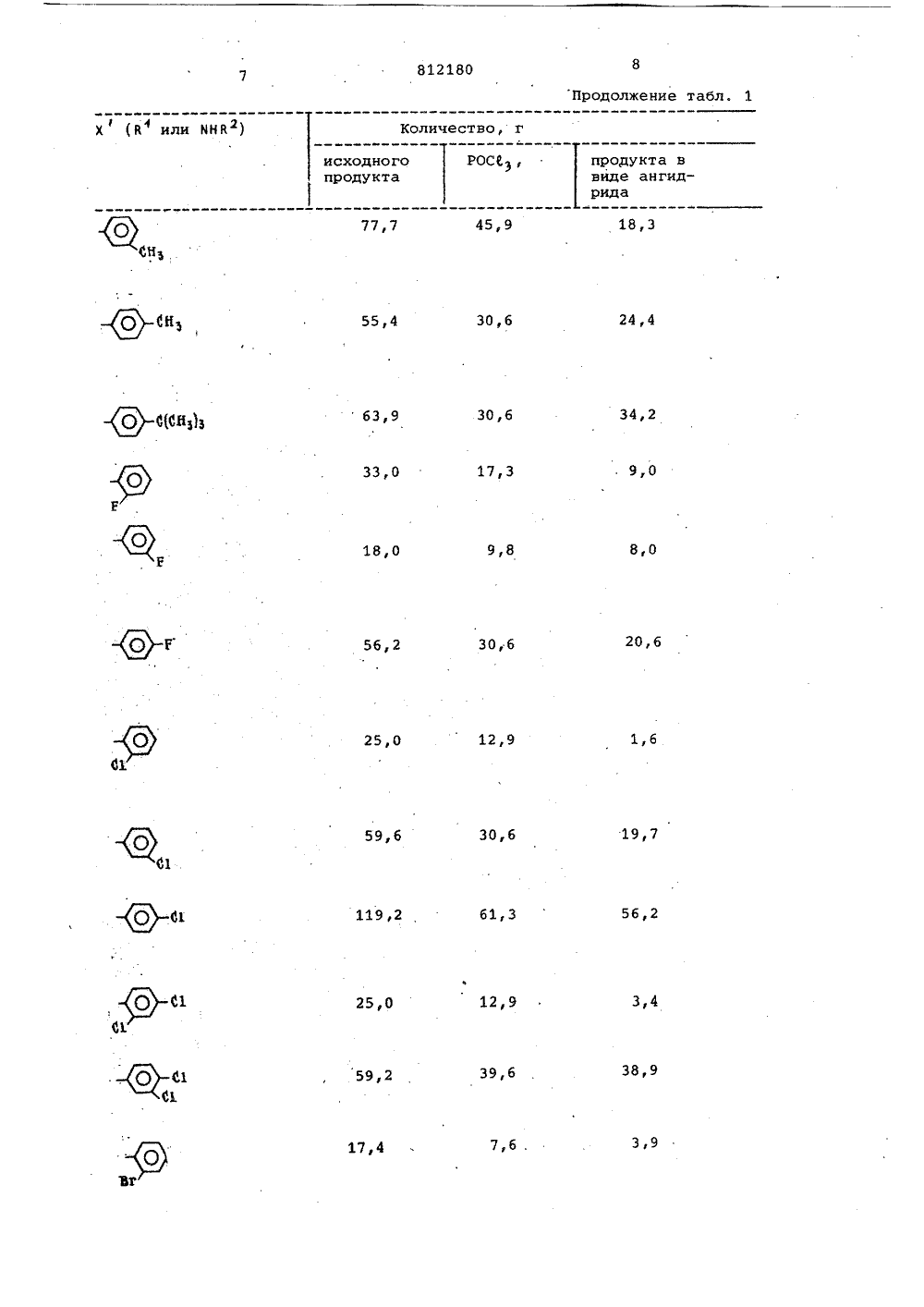
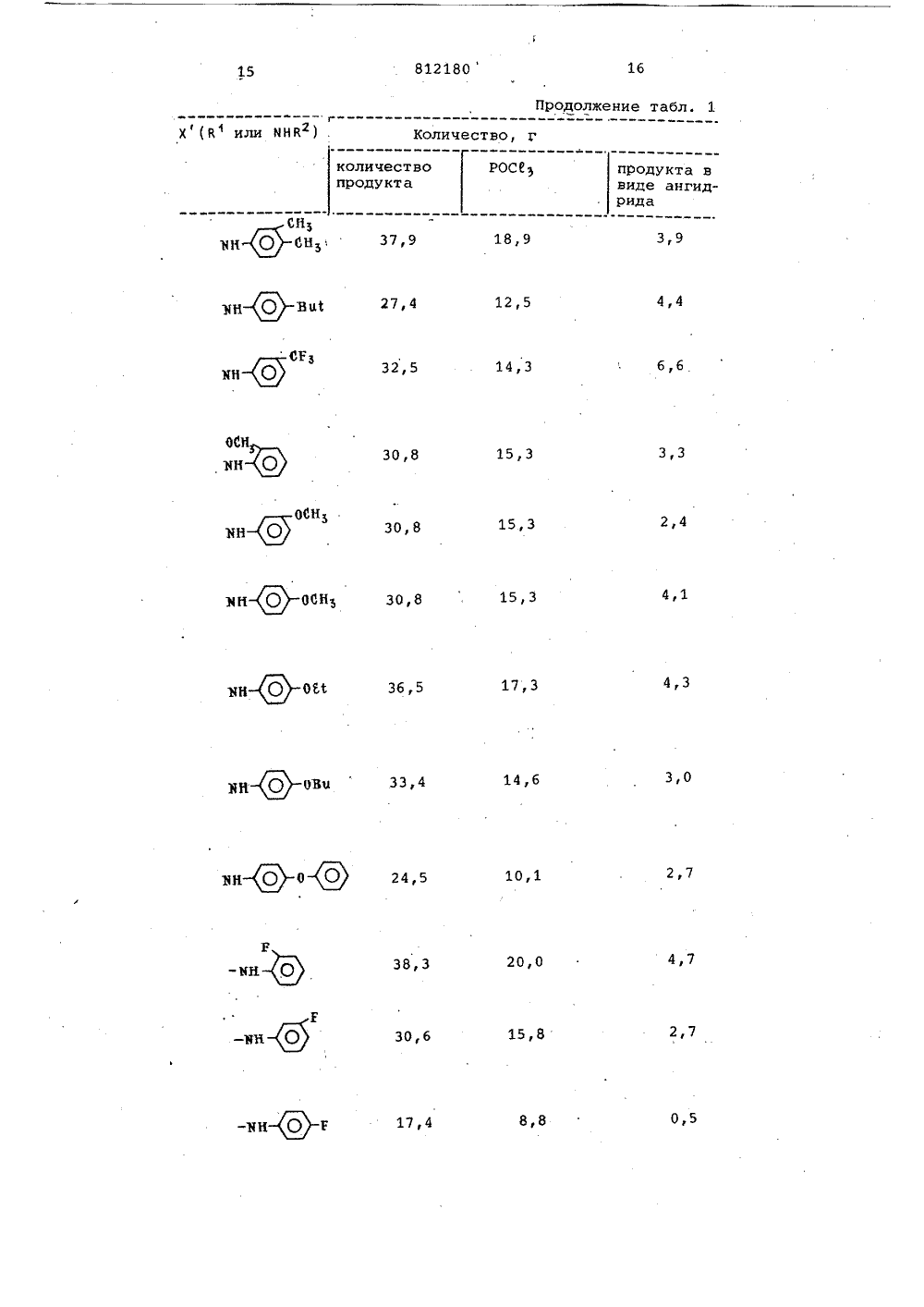
ОПИСАНИЕ ИЗОБРЕТЕНИЯ Союз Советских Социалистических Республик(23) Приоритет - (32) Государственный комитет СССР по делам изобретений и открытий(53) УДК 547,781. . 78507 (088, 8) Дата опубликования описания 070381Заявитель ОСОБ ПОЛУЧЕНИЯ 4-ЗАМЕЩЕННЫХЭО 1,2-а 1-ХИНОКСАЛИНОБ ИЛИ ИХ СОЛ И хинаэолины, облай активностью илиочными продуктамически активных эобре чения 1 2-а ение относитс новых 4-замещ -хиноксалинов к способуных имндабщей формуС интез новых адают биоло- и могут быть промежуточза соединени й активносО стигаетс олучения формулы лы о 0 1 нс-х,едста В и де Х пр вНВ, гдеые выше,. Виклоалифатичесамещенный фени В или ия указа кая или фенил,сированныйляет собомеет эначеалифатиче кая групп л, сконде или их солей,где х 1- В 1 или йНВ , В присоединен к кольцевому углеродному атому углерод-углеродной связью и представляет собой алифатический или циклоали фатический радикал, замещенный фенил, сконденсированный бициклический арил или алифатическую группу, заме- ,щенную моноциклическими арилом; В присоединен с атому азота углерод 2азотной связью и представляет собой алифатическую, циклоалифатическую группу, феннл, замещенный фенил, сконденсированный бициклический арил; или алифатическую группу, замещенную 25 моноциклическим арилом, обладающих биологической активностью и являющихся промежуточными продуктами для синтеза биологически активных соединений. 30 Известны имидазодающие биологическоявляющиеся промежутдля синтеза биологисоедИнений 1 1.Цель изобретения -соединений, которые облгической активностью илиспользованы в качественых продуктов для синтобладающих биологическтью.Поставленная цель дпредлагаемым способомдинений указанной общезаключающимся в том, чаминофенил)-имидазол о20 812180 19 Продолжение табл. 1 Количество, г росе количествопродукта ЮК 0 30 32 3 10,1 15,3 тн-ЯО -ВСЕЬ за,а 2,6 15,3 1 В О С М 46,3 2,6 23,3 4,5 14,6 31,2 2,0 23,0 50,7 0,6 9,3 20,7 6,6 12,3 21,0МИ О С 1 1,5 8,5 6,4 13,8 1,5 Х (й или МНВ С 1мн 0 СЦ Офмн 0 си,М 02юц 0 02 О 41. 98-100 80 юб СН (СН )Соединения общей формулы СН (СН )- В Ъ СНЗ (СН ) - А СН (СН)7 - А 63,3 Вода Толуол-гек-125 сан Изопропило-105 вый эфир- трихлорэти- лен Н 6,59й 18,33С 69,11Н 7,04й 17,27С 70,01Н7,44й 16,33С 70,82Н 7,80й 15,48С 71,55Н 8,12й 14,72С 72.,21Н 8,42й 14,08С 72,81Н 8,68й 13,41С 75,52Н 9,89й 10,57С 76,19Н 10,18й 9,87 64,26 4, 7 ь 22,30 65,69 5,52 20,84 67,26 6,15 19,40 67,956,52 18,25 69,14 7,00 17,17 70,31 7,45 16,26 70,79 7,74 15,23 71,67 8,05 14,65 72,24 8,41 13,92 78,38 8,85. 13,02 75,12 9,76 10,38 76,57 10,289,79(сн ) С 69,11 Н 7,04 М 17,27 С 69,40 Н 6,66 й 17,34 102-104 48,8 13 Бензол 128-г 20 25,4 14 с 71,55 Н. 8,12 й 14,72 С 73,81 Н 8,36 М 12,91 71,867,84 14,95 74,268,50 12,30 125-127 32,8 92-94 76,8 Изопропиловый эфир гексан 73-76 3,6Сн 145-147 205-207 Диэтиловый эфир 7,7 161-164 Сн осц 136, 5138,5 2324 ( 207-209 го,г Изопропа- нол 151-153 142,5145 67,3,5,59Получено из уксусномуравьийого ангидрида по Джонсу. После отгонкн избытка растворителя остаток растворяют в воде и нейтрализуют йаОН для получения сырого продукта.Получено через ангидрид.Не кристаллизуется, очищают хроматографнчески на окиси алюминия, элюирование ведут зтилацетатом. Таблица 3 Соединения общей формулы нНС-Аф ТИетод выде- ления Температура мфК плавле- ( Ония,ф С Выход, РастворнтельЪ для кристал- лизации Анализ, В Номерсоеди- д,нения вычис- найделено ноРастворительдля кристаллизации Метод выде- ления емпера.уралавлеия, С омер оеди ения ычис- найде но н 57,б С 73,63 73,2Н 545 52 й 15,15 15,2 4346,5 С 61,63 Н 3,65 53 153 нзол 9 (скз)сО 23920,4 9 13,37 13,332 812180 31 ПРодолжение табл. 3 Номер соеди нения Метод выде- ления Анализ, Ъ Растворительдля кристаллизации Температураплавления,С Выход,В,8 Этанол А 5,3712,68 3,00 ачительного УФ выход. е позволяют определ нения общей формул ц а 4 Т Соед 1НС - МНИ Растворкристаллции 2 Метод Вых К выде- Ъ ления(Е) ель эанализ, В Номер соеди- нения йден вычислно 41,6 Этан 94-196 240 С 61,60,6 Изопропано 7 .СН СН СН СН В 15-116,5 Н 7,0 й 21,6 21,78 67,60 .7,08 164-166 0 64 Диметилфор 68 4112,200) 67,58 7,0919,70 мамид- вода,4 Соединение поглощает слишком мало для ф Выделено в виде полугидрата. Частичные потери н и 278(1,20242812180 зз 34 Таблица Соединения общей формулыМ и нСорит ель аллиза- ции ых омер .бедиения йден 69,13 5,15 20,16 69,85 0120 б б б анолРастэорителькристаллизаЦИИ Выхдд, Ф Теипература плааления, С Номер соеди нения Анализ,найдено вычислено С 195. 259(30,210) 211,5214,5 62, 3 Диметил- формамид- мода 96 / Р1 З (С 1 252(25,230) 75,9 То же 198210 258(32,380) 232,5234 64,8бициклическии арил. нлн замещеннаямоноциклическим арилом алифатическаягруппа, присоединенная к карбониль.ному атому углерода углерод-углеродной связью,подвергают циклизации в присутствиихлорокиси Фосфора с выделением целевого продукта в свободном виде илив виде солей.П р и м е р 1. Получейие 4-(3-трифторметилфенил)имидазо 1,2-а )хиноксалина,Раствор 16, 3 г (0,11 моль) хлорокиси фосфора в 100 мл сухого пиридина обрабатывают 35,2 г (0,11 моль)1- 2-(3-трифторметилбензамидо)-Фенил 1имидаэола, нагревают раствор на паровой бане в течение 2 ч, охлаждаюти перемешивают в 1 л воды. Образующийся при этом осадок отфильтровывают, промывают водой и растворяют в50 мл хлороформа. После осушки надбезводным сульфатом магния растворхроматографируют на колонке диаметром 6 см, содержащей 350 г окисиалюминия, с использованием в качестве растворителя хлороформа, Послеэлюирования компонентов с наименьшим временем удерживания и отгонкирастворителя получают твердое вещество, которое кристаллизуют из изооктана. Таким способом получают 16,2 гпродукта, имеющего т, пл, 112-113 С.П р и м е р 2. Получение 4-бутилимидазо 1,2-а 1-хиноксалина.Раствор 15 3 г (0,1 моль) хлор-.окиси фосфора в 75 мл сухого пиридина обрабатывают 24,3 г (01 моль)1-(2-валерамидофенил)-имицазола.Раствор нагревают с обратным холодильником в течение 1 ч, после чегоохлаждают и после перемешивания с400 мл воды отгоняют примерно половину растворителей при пониженномдавлении, В результате получают осадок, который отфильтровывают, промывают водой, растворяют в 200 млхлороформа и сушат над безводнымсульфатом магчия, Вещество хроматографируют на колонке диаметром б см,содержащей 350 г окиси алюминия, сиспользованием в качестве растворителя хлороформа, собирая при этомкомпонент, обладающий наименьшимвременем удержания. После отгонкирастворителя и кристаллизации остатка,.из гексана получают 4,0 г (17,8)желтых игл, имеющих т. пл. 92-93 ОС.П р и м е р 3. Получение 4-(4-хлораиилин)имидазо 1,2-а)хиноксалина.Раствор 15,3 г (0,1 моль) хлорокиси фосфора в 75 мл сухого пиридина обрабатывают 31,3 г (0,1 моль)1- 2-(4-хлорфенилурилен)фенил-имидаэола, нагревают полученный раствор с обратным холодильником в течение 0,5 ч и охлаждают его. Вязкуюсмесь Фильтруют через Фильтр из.:.л-реформа и сушат охлажденный раст-.вор над безводным сульфатом магния.Раствор хроматографируют на колонке;ачестве,растворителя хлороформа, собирая при этом компонент обладающ й наименьшим временем удерживания,После отгонки растворителя и обра;утки остатка этиловым зфирои полу=ают твердый остаток, который отФильтровывают и кристаллизуют изсмеси метанол; хлороформ (10:1)Таким способом получают 4.0 г про-1 дукта, т. пл. 176,5-178 СОстальные примеры приведены втабл., 1,. В табл. 2 показано получеге ал"Фатичесхих, циклоалифатических и за,".ещенных моноциклических арилом алифатических амидофенилимидазолов поизобретению. В табл, 3 показано полу.-ение арил (включая сконденсирован ное арильное кольцо) - амидофенилими-.дазолов по изобретению.В табл, 2 и 3 применены следующиеметоды выделения;твердое вещество, прямаякристаллизация из растворителя. указанного в таблице.В - масло, растворение с минимальном количестве хлороформа и пропусканне через колонку с А 2 03,. коли.честно которой примерно в 20 раз вышевеса сырого твердого вещества элюирование хлороформом, отгонка хлороформа и кристаллизация из раство.-.ителя указанНого в таблице.С есл раствор в смеси с ледя"- 1 Р4 ной водой,. то азеотропная отгонкапиридин - вода, остаток сырогопродукта обрабатывают по методу В.Алкил-(1-имидазолил) -Фенилуреилены (см. табл, 4) получают пО реак ции эквимолярных количеств аминоФеййлимидазола и соответствующегоизоцианата в толуольном растворе притемпературе паровой бани в течение2-3 ч. После охлаждения сырой про- аО дукт собирают фильтрованием и обрабатывают по одному из следующих методов:А. Прямая кристаллизация иэ соответствующего растворителя;Б. Растворение в горячем диметилФормамиде и осаждение водой с последующей, кристаллизацией.Арил-(1-имидаэолил)-фенилуреилены (см. табл. 5) получают по реак-ции эквимолярных количеств аминофо фенилимидазола и соответствующегоарилизоцианата в сухом толуоле в течение 3 ч при температуре паровойбани. Реакционную смесь охлаждаюти сырой продукт отделяют Фильтрова нием его промывают эфиром и кристал,52 2 Т лица Соедине общей формулы алиэ, В Т ату- Двле ФоксВыход,Растворитель для Ъ кристаллизации Номер соеди кения иоле- найдено 316 (10,900)312(11;200) ублим б 00 С 72,11 Н 4,95 и 22,93 С 73,07. Н 5,62 и 21,30 10 й 134 опропил СН Гексан 4-115 311812180 41 42 Продолжение табл. б Выход,Номерсоединения Анализ, В ычи на ено СН (СН ) 26,щ,9 ексан 8 5 18,7 276 Н=6 Н,2 Растворитель для Температу кристаллизации ра плавле ния, ф С/0,15 мм рт.ст.84 фС/0,40 ж рт.ст. Температура плавления этого(литературные данные).фф Очищено сублимацией при 90Очищено перегонкой при 174 Продолжение т,абл. б Акали э, Ъвычисле- найденолоС ЧИ Г Е м в ч гсч) М сФ сут.3 с О с Оф С, О (Ч (ЧО сЧ СЧ сФ сс с с с с Ю (Ч Ю М 1 Л М Сс В СЧ ф тЧ) гЧ сЗС ес бмюС ее ФчщФ м м еч 1.о. ф 111о 1 щ. с ф 1 щ М й ф щщ Ф, ф М Мсс сф м Ф ф м е Ч) е М 0 еР ЕЧ Р еЧ Ю щ Лфефюафв с с Ссс со ч м о ч м фг 4 Ю г Ю аЧ й е вв ." ф Р е ф М е ф М Яс сс сс Е е Ч М еЧ СЧ М Е е Ю еЮ е- й о1е 1 Й Ю1СО о с Гщъ а 0 ОЪ М Ю СО М ГЧ СР М М О "О О "с СЗЪ ОЪ СО 01 а СО а а "ГЧ У М ГЧ 3 фс,с с с,с сс сс сГч Гч м а о м э а м с а м 33 ъ ч3 щ Н Гщ, Н Гс ГЧ О Н 1 Ю м а Г"Ъ С 0 0 асм э нГЧ м а с н ГЧ ь м а Ю м с ОЪ -1 м а ф 0 с с м э Н ОЪ ф Ю ГЧа с ОЪ ОЪ 1 С 0 ОЪ м м н 1 о м н И ОЪ 1 Ю ОЪа СО н 1 м н а СО ГЧСО ГЧ 1. аа с с Ю 3 ГЧ ГЧ ГЧ (3 а аГс ОЪ аа ГЧ 3 Ч Е й О Я 3 Х Н Ц 0 3; 0Х Ц Х 1 1 Й С 1 1 С 1 Н 1 Х Ц 1 С 30 Н 1 300Н Х ОЙ 1 С 1 О Ц 0 ГС С О й И О Ж Ф", 0 Х Г Н Х. О О Н ОЪ 1 1О МЭ ОДНй СХ Х0: Б- СО с о н СОЛ ъ м с с О ф СО Ч Ю М 3 МЧ Лн 3 ОЪ 3 СОс с3ОЪ М Ч Н ОЪ.О ОЪ М с с с с СО 3 3 Н О Н Гщ 1 1 1 Э 1, я 1 б Ож х 3 О б 3 1 11 1 1 Э 1 Ч ф Л м 3 Фсс ф 3 СЧ4 сч м сч " СЧ Ч 3 СЧ Л " С- Мс с с 3 Ъ 3 Н СЧ Н сдам НЛ фм лсЮ фщ 3 н с н н Л м н о с с Л " н о н ОЪ с ф б н О с ссЧ Л СЧ Сс Н 3 СО Ч Л О СЧ М СО с с с с л н Р м и Г" н 1 Н ОЪСО,0с сСО 3О х Э И Ц о Х 1 1 б 1 Х Х 1-и Г -б 3 б о я оо8 31Х 1 Е о е о й о 1 о х б 1 Ъ В1 1--- , 11 с3 Ц1. О1 Хе ь СО с ОЪ СЧ СЧ с 00.фч . ч, чФ ы ооЭЬ.ФМь о.о О. 1, 1 3 1ц ц 1 е а 1 рЕО Н 1 1 1Э 11 1640,г ---1 ВИ1 В,1 Ю1 М 1 Во щ 1 ЮО 1 М и э м ф ч ф М Ри ъс чу г сч ю ч Гнн ф 4Ю Ю ОО 1" О Н Н м Ю Ю О 1 н м и м щ Ю ОО Ф (ч н М ъ 1 моыф %1 ффГж до йхо 1 Ф Ц 1 СИЫЕ ФФХ 1 Эй 3 Л н Ю н 3 Л Ь СО О 1 О н 1 ГЧ Ю н 1Р 4812180 1лизуют иэ укаэанного в табл. 5 растворителя.4-Алкнлимидазо ( 1,2-а)хинохсалины (см. табл. 6) получают путем нагрева с обратной перегонкой соответствую. щего амида (см. табл, 1, соединения .1-33) с хлорокисью фосфора в избытке пиридина в течение 1 ч, Реакционную смесь. перемешивают в воде и от,гоняют аэеотроп. Получают вязкий осадок, который растворяют в хлороформе, сушат над сульфатом магния и хроматографируют на колонке с Му Оз. Хлороформ отгоняют продукт крйсталли.;МНУ ) ееай Ю М ю ю ае сходно г продукт 8 1.5 , 3В виде анг 24,3 5,2 27,1 28,5 .(СН)8 СН=СН -СНзОСН лиэуют из укаэанного в таблице раст.,ворителя. 4-Арилимидаэо 1,2-а)хоноксалины (см. табл. 7) получают и выделяют по общему методу, описанному для 4-алкилимидаэо 1,2-а- хиноксалинов, кроме случаев, указанных в табл. 7,4-Алкиламиноимидаэо 1,2-а 1 -хиноксалины получают обработкой соответ ствующих алкилуреиленов хлорокисью фосфора и пиридином в течение 0,5 ч (см. табл. 8) и 1 ч (см. табл. 9) с обратной перегонкой.Таблица 1 М Количество, г Фв РОС Й продукта в виде ангидрида 7,729,115,323,0При нагреванииВ виде ангидрид(О г.( ф гГ ОЪОЪс сО . (ч сгн сч о ОЪ О с с СО СГ Ю ф ф сч РЪ Ъ ф Ю г(сс ф СО Е О тЧ (О СЧ СЧ (Чс с(Л ф О ОЪс ОЪ РЪ (О(О ( (О СЧ (О М а ОЪ (ГЪ ф РЬ ОЪ с с с с ф ОЪ М Ь т.Ч (О (Ч к о хо х Ц 1 -----О 1 Ю.сЧ СО (Л а-( м (ч РЪ с Ю %-( сУс ю Ч (О СЧ м Ю РЪс (+. гЧ су (Ч ГЪ с ь РЪ ос т СО м н о РЪ счс мо сф гч М с,Ю О (ъ сг (Ч (Ч мЮ г-( фс РЪ к-( РЪ с. О о (О м оъФ г( РЪсЕ 1 й цо ое хо (б О но812180 . 6364. Ъ ф . Ф 01 0 РЪ с 01 ф емовасфсф С,с с сс с м а о се а Оъ м а фч ЕФЕСЕ.ИЧЕЧЭ 0 с с Ф О ЧЭ Осс с с с ссб ч ч Ръ ч а чФ аЧ 0 .Чефвнфе вочфаэс с с с. с о во съ науч а" 0 Ч Юа ю м а Ръ ю 01 Ю 01 01 0 ОЪсс с Ю И Ч Ч РЪ 4 Ч Ю Ч Ю СЧ 0 ъ ф Э ФЪ а 61 а 01 фФ с 4 сс сс ае ааЧ с Ойй.О ВЗОфйОВЗОВЗОЖйОй йОйй о о сР а с о о о ф с Фф оофс Ч Ю Юо с, фе о,фвч 01 ф .ч 4 О б ф 4 ММЧ Сф щщ СЪ сг 11 1 аа ф с1 фа н ЧВЮ фс М 1 Ф: 01 чФ чЧ с .0Мф ос с Ю ф ф о УЕ 1 оъ 15 1 аО 1зз Ч е 1 Ц 1 юс 1. еЧсасф юЪ й ф Ф ф1 01 а сУ ся сФ а 01 фЪ е И ф а н с с4 ф) а ю с Г 3812180 66 О Ю 3 ф Ю Ф Ю Ф а а ф а м тР ьь сь с л а ча 1 н мл Н Ю Н 1 О Н 0 СЧ 1 с со 1" с с ь а сч а а н О ф 1сч моь ьСЧ М 1"0 Н в ф а сч л уО 1 ч а а нс О Ф д о о а сР а Ч Ч мь ф о о м ло Ф Ч м сг Ю о 3 НО фФ сч м юг о о О ьв Ф н м сФ о о, мс оо Ф Ч М ь о о Ч (Ч фФ су сч М ьщф о о счс а м СО (Ч мм сч н а с о сч н о н 1 а с сч Ю н а н в 1 а ь в ф л Гч н 1 а сУ сч о м н.й о 01 1 л сО н аа ьфв нн Ц о 3й.с фМ1 11 101 Н ЦОа айте. "1 И Й 11 ИХХ, 1ен йх1АЦ (с 11 Ф с 1х1 й ИО О Х1л Х 1чО 11 Ц Х 1ДЬ Х 11 11 1ь 1Ц 1о1 С дйВ 11 11 111 чФ " СЧ Ф Л СЧ СО 1 Ч СО СЧ СЧ НЧ Ю чУ н ч о н р о а а а м м О а м ь ь ь с с ьь ь ь ь с ь с а ва в О ч л ф а л н м Л НН ОЮм н м м н м в О о в а ф о ф л ф сч сч од а ч со асч а ф вф сч м о а ч) оь ь ь ь ь ь с с ь с ь ь с ьь (О а в сО а в ю э л сб а л сч м л аФ сОн л н л и чР н чР н ю н О ж л О ж и О ж ж О х м ц жио .овн фФ Сч м сег о о.10Ь 10 В ЯС4 м о о мЬ фм С М,4 о о вВ а. чЮ СЧ мо. о Сч . С СЧ МФ СЧ м щф. о о СЧф в и СЧ ео 1 ааЬВе 4 а 10 ,Сч СЧ 1 аа % Ь СЧМ Сь Сс % 4 %щ 4 1 3 Цф в 1В фФ о м ф4 а ю 4 ФС ЮГЮЭ О:е 4 СЧ т 4 СЧ СЧ Сч СЧ в1 ф311 й 11 1ц" э 1 ф фФ 1 юч11 1 ГТГЬь ЭеахЕО .йо 3 аО 4 РЪ В4 ф, 1 О, 1 вфаффСЧ40 Сч а а ч 3ае 4 ю. цахцщ 11; СЧ1 а .1 4 Р 1 4 1 м 1, Ф11, 1 .м.3 АЙЗ 1 О 0 МВЧО 4 СЧф ф ф ч В ф СчЬ ЬСф ЩР М ф О, М с 4 Е . 4 а.ц ж х цФо с- а4 О Е о.-.ма м сч ф а .о сч в оЪ.Ь Ь Ь, Ь0 е 4 М ф ф М с 4 СЧ ч 3Е . 44 а. СЧ ф Ф а сч сч сфъ м) а ч сч в 40 е 4 , С Ь Ь04, М Сф фс 4 ЮсЧ а хцщхца 9 р.812180 72 71 формула изобретения й 0 Нейскфили ННОЕ где Х представляет собой й.илн3йНЙ , где к имеет значения, укаэан 2ные выше,или ихгде х В присоединен к кольцевому углеродному атому углерод-углероднойсвязью .и представляют собой алифатнческий или циклоалифатический радикал, замещенный феиил, сконденсированный бициклический арил илиалифатическую группу, заиещеннуюмоноциклическим арилом,й ф присоединен к атому азотауглерод-азотной связью и представляет собой алифатическую, циклоалифатическую группу, феиил, замещенныйфенил, сконденсированный бициклический арнл или алифатическую группу,замещенную моноцлклическим арилом, 25о т л и ч а ю щ и й с я тем, что Составитель Г, ЖуковаРедактОр Л. ушакова Техред Н.Бабурка Корректор Г, Решетннк 51 б/4 Тираж 443ВНИИПИ Государственного компо делам изобретений и от 13035, Москва, Ж, Раушская сн Потета СССРрытий,наб., д. ак илиал ППП фПатентф, г. Ужгород, ул. Проектна Способ получения 4-эамещенных. имндазо ф,.2-а 1-хиноксалинов общей формулыХ 1-(2 ф-ациламинофенил) -имидазол общей формулы й э - алифатическая илн циклоалнфатическая группа, фенил, замещенный фенил, сконденсированный бициклический арил или эамещенная мсцюциклическим арилом алифатическаягруппа, присоединенная к карбонильному атому углерода углерод-углеродной связью,подвергают циклизации в присутствиихлорокиси фосфора, с выделением целевого продукта в свободном виде илив виде соли.Источники информации,принятые во внимание при экспертизе "1. Ъвторское свидетельство СССРР 405895, кл. С 07 О 487/04, 1971.,2 12 р 9 5,0 389 Х (В или КНВ ) Я-б(Ср 11 ф Колихество р Г ИСХОДНОГО РОСпродукта Продолжение табл, 1 продукта ввиде ангидрида812180 То же о же ния,о мет 16,2 б 18 50,9 КОличестВО р Г исходногопродукта Из соединения имеюцего группу НН восстановление нз соединения, имевшего групп Из соеди соце ржац оксигруп Из соединениясодержацегоОН-группу ПРодолжение табл. 1 продукта ввиде ангидрида.812180 1 З РОСС10,2 26,0 53,0 25,9 5,3 0 ,.8 1 5 , 3 г 7 , 7 ЗО , 6 го,г 57,8 15,3 4,15, 3 5,15 28,4 5 8,0 15,2 15,3 29,2 3,6 9,2 5,З 6,07 8 36,н О Количество, г скодиогородукта Продолжение табл. 1 продукта ввиде ангидрида 1,7 6,8-мн 0 4,7 38,3 20,0 2,7 15,8 30,6 17,4 0,5 8,8 Х (Я" или МНР ) СН,д О Сц оСн МН оснмн-Я
СмотретьЗаявка
2566098, 18.01.1978
ПОЛ Л. ВАРНЕР МЛАДШИЙ, ЭДВАРД ДЖ. ЛУБЕР МЛАДШИЙ
МПК / Метки
МПК: C07D 487/04
Метки: 2-a-хиноксалинов, 4-замещенныхимидазо1, илиих, солей
Опубликовано: 07.03.1981
Код ссылки
<a href="https://patents.su/36-812180-sposob-polucheniya-4-zameshhennykhimidazo1-2-a-khinoksalinov-iliikh-solejj.html" target="_blank" rel="follow" title="База патентов СССР">Способ получения 4-замещенныхимидазо1, 2-a-хиноксалинов илиих солей</a>
Предыдущий патент: Способ получения алкиленкарбонатов
Следующий патент: Способ получения циклическихпроизводных 1, 4-бензоксазина или1, 4-бензтиазина или их кислотноаддитивных солей
Случайный патент: Волосяной гигрометр