Фрагмент дезоксирибонуклиновой кислоты, кодирующий промотор sp6 рнк-полимеразы
Похожие патенты | МПК / Метки | Текст | Заявка | Код ссылки
Номер патента: 1759873
Авторы: Артамонова, Горн, Назаренко
Текст
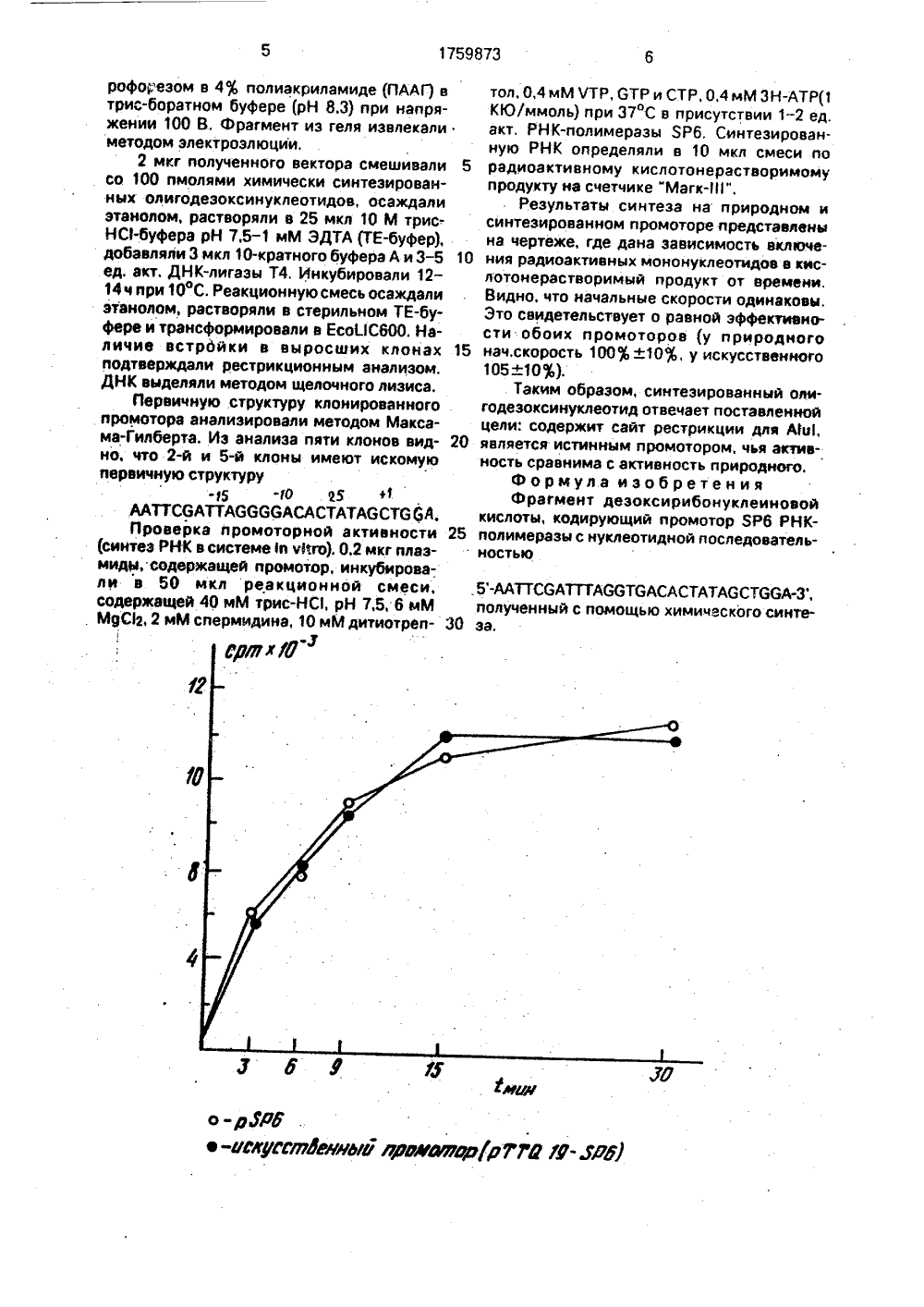
(54) ФРАГМ НОВОЙ КИ МОТОР ЯР 6 (57) Исполь гия, генетич гия, Сущно химическог ДНК, кодиру имеразы,венный унисомолаи Т,П. АртаЬВ 18, р.7035. екулярной рии и биользовано в получения зучения и огических ке, а функуклеотиды щения цеактера, таостика и торы для ей струк-5, -1+1 Т 6 АСАСТАТА 6 АА 666, Ф ц,а,где А - ад цитидин, а обнаружен РНК начин ации трансОдин и был,испол обеспечив цию в сист ГОСУДАРСТВЕННЫЙ КОМИТЕТПО ИЗОбРЕТЕНИЯМ И ОТКРЫТИЯМПРИ ГКНТ СССР АВТОРСКОМУ СВИДЕТЕЛЬСТВУ(56) йцс. Асбз йез, 1984. ч,12 Изобретение относится к молбиологии, генетической инженетехнологии, и может быть испоуказанных областях науки дляРНК в качестве субстрата для имоделирования основных биолпроцессов, протекающих в клетциональные РНК и олигорибонкрайне необходимы также для релого ряда задач прикладного харких как медицинская диагнискусственный синтез белка.Известны природные промоРНК-полимеразы ЯР 6 со следующтурой:-15АТТТА 66 енин; Т - тимин; 6 - гуанин; С - , , д, с - возможные замены, ные ь промоторах ЯР 6, Синтез ается с+1 позиции-сайта иницикрипции.з природных промоторов (ЯР 6 4) ьэован для. создания вектора, ающего эффективную транскрипеме и ч 1 го, Для этого фрагмент ЕНТ ДЕЗОКСИРИБОНУКЛЕИСЛОТЫ, КОДИРУЮЩИЙ ПРОРНК-ПОЛИМЕРАЗЫ зование: молекулярная биолоеская инженерия и биотехнолость изобретения: с помощью о синтеза получен фрагмент ющий промотор ЯР 6 РНК-полДНК фага ЯР 6, содержащий промотор, был клонирован в высокоскопийной плазмиде (риС 12 или риС 13), которая содержит полилинкер, узнаваемый рядом эндонуклеаз рестрикции. Полученные векторы получили название рЯР 64 и рЯР 65, Схема получения РНК с помощью этих векторов состоит а клонировании заданного фрагмента ДНК по полилинкеру, расщеплении плазмиды рестриктазой для обеспечения терминации а транскрипции и синтеза РНК в присутствии РН К-полимеразы.ЯР 6, СЛНедостатки прототипа заключаются в том, что при синтезе РНК невозможно пол-.учить молекулу, строго соответствующую заданной структуре, так как она всегда будет содержать от 5 до 10 "избыточных" нуклео тидов на 5-конце. Это происходит из-за того, что клонирование ДНК-матрицы происходит по полилинкеру, удаленному ота сайта инициации промотора, Поэтому транскрибируется +1 +6-фрагмент и ромотора и последовательность сайта рестрикции, по которому шла встройка.Цель изобретения - получение фрагмента дезоксирибонуклеиновой кислоты, кодирующего промотор ЯР 6, который по35 50 зволял бы встраивать фрагмент ДНК непосредственно к сайту инициации транскрипции, синтезировать РНК, не содержащие избыточной последовательности на 5-конце, что позволило бы получить молекулу, строго соответствующую заданной структуре, при сохранении высокой промоторной активности.Свойствами, обеспечивающими достижение цели мог бы обладать олигодезоксинуклеотид, содержащий сайт рестрикции, позволяющий расщепить ДНК с образованием "тупого" конца непосредственно перед сайтом инициации транскрипции. Очевидно, что РНК, синтезируемая под таким промотором будет строго соответствовать ДНК-матрице, т.е. не будет. содержать "избыточных" 5-нуклеотидных остатков,Синтезированный олигодезоксинуклеотид (искусственный промотор), где й - нуклеотидные остатки, были подобраны так, что стала возможной рестрикция с образованием "тупого" конца в непосредственной близости от сайта инициации, с одновременной высокой транскрипционной активностью олигодезоксинуклеотида. Синтезированный двухцепочечный олигодезоксинуклеотид имеет следующую структуру: ААТТСОАТТТАООТОАСАСТАТ ОСТ (Ваш Н Ц (Всой) бСТАААТССАСТОТОАТА ТСО ССТАО,где в скобках указаны "липкие" концы для клонирования олигонуклеотида по указанным сайтам рестрикции, а в рамку взят сайт узнавания рестриктазой А(ц 1, которая при расщеплении дает "тупой конец: АбфСТ. ЕсТООА ли сравнивать синтезированный олигонуклеотид со структурой природного ЗР 6-промотора, то видно, что для получения Ац 1-сайта необходимо ввести замены в+2 и +3: позиции. Для доказательства того, что такой измененный олигонуклеотидсохрзняет промоторную активность, химически синтезированный олигонуклеотид встраивали в плазмиду рТТЯ 19 по Есой 1 - Вав Н 1-сайтам, Полученную плазмиду назвали рТТЯ 19-ЗР 6 и испытывали на способность инициировать синтез РНК.в системеи ч 1 тго в присутствии РНК-полимераэы ЗР 6. Эффективность сравнивали с эффективностью транскрипции на природном промоторе в плазмиде рЗР 6 4.П р и м е р.Получение ЗР 6-лромотора, содержащего А 1 ц 1-сзйт в+2 позиции и проверка его промоторной активности.Синтез олигодезоксирибонуклеотидов .проводили на серийном Отечественном синтезаторе "Виктория-,5 М" производства 10152030 СКТБ спецэлектроники и аналитического приборостроения СО АН СССР с использованием фосфитамидного метода по стандартным программам. В реактор синтезатора помещали 30 мг полимера СР 6-500, Вцса, с присоединенными через остаток янтарной кислоты первым звеном - 5-диметокситритилнуклеозидом, Диметокситритильную группу удаляли 1,5 трифторуксусной кислотой в абс. СН 2 О 2 в течение 30 с, После промывки реактора абсолютным ацетонитрилом в реактор подавали смесь мо номера - 5-0-диметокситритил-й-ацилдезоксинуклеозид(Р-метил, диизопропиламидо)-фосфита (200 мкл 0,1 М раствора в абсолютном ацетонитриле) и активирующего агента - тетразола (200 мкл 0,45 М раствора в абсолютном ацетонитриле). Время конденсации 80 с. Остаток непрореагировавшего гидрокомпонента ацилировали 2 мин смесью: уксусный ангидрид-триэтиламин-й-метилимидазол-ацетонитрил. (4,5:4.5:1:30). Затем фосфидную группу окисляли 0,1 М йодом в смеси: пиридин-уксусная кислота (9:1) и промывали полимер ацетон итрилом.После завершения синтеза олигонуклеотиды, присоединенные к полимерному носителю, обрабатывали смесью диоксан-три- . этиламин-тиофенол (2:1;1) в течение 1 ч для удаления межнуклеотидных метильных групп, затем - концентрированным аммиаком в течение 1 ч при 20 С для удаления нуклеотидного материала с .полимера и в течение 15-16 ч при 50 С для деблокирования гетероциклических оснований, Аммиач- . ныйраствор упаривали, остаток растворили в 0,1 М трис-буфере (рй 9,0) и выделяли олигонуклеотид с 5-концевой диметокситритильной группой, обращенно-фазовой хроматографией на колонке с ОсЬгозогЬ ЙР("Мегск". ФРГ) в градиенте концентраций ацетонитрила 0-30 в 0,05 М О:С 104, Нужный пик, элюирующийся при 12-15 ацетонитрила, собирали, упаривали, удаляли диметокситритильную группу 80 уксусной кислотой (15 мин при 20 С); раствор упаривали и остаток рехроматографировали на той же колонке в приведенных выше условиях.Клонирование двухцепочечного олигонуклеотида в рТТЯ 19 Данный плазмидный вектор содержит уникальные сайты для рестриктаз ВааН 1 и Есой 1, 10 мг плазмиды в 500 мкл 10 мМ трис-НС 1-буфера (рН 7,5), содержащего 10 мМ МЯС 12, 10 мМ р меркаптоэтанола и 50 мМ ЙаО (буфер А), обрабатывали 10 ед. акт. ВаеН 1 и Есой 1 в течение 1 ч при 37 фС, Больший ВааН 1 и Есой 1 фрагмент выделяли препаративным гель-элект1759873 о -фригэ-иекуГгтйинье лрвМОаоррТМ 9-5 Р 61 рофорезом в 4 полиакриламиде (ПААГ) в трис-боратном буфере (рН 8.3) при напряжении 100 В. Фрагмент из геля извлекали методом электроэлюции.2 мкг полученного вектора смешивали со 100 пмолями химически синтезированных олигодезоксинуклеотидов, осаждали этанолом, растворяли в 25 мкл 10 М трисНС 1-буфера рН 7,5-1 мМ ЭДТА (ТЕ-буфер), добавляли 3 мкл 10-кратного буфера А и 3-5 ед. акт. ДНК-лигазы Т 4. Инкубировали 12- 14 ч при 10 С. Реакционную смесь осаждали этэнолом, растворяли в стерильном ТЕ-буфере и трансформировали в ЕсоОС 600. Наличие встройки в выросших клонах подтверждали рестрикционным анализом. ДНК выделяли методом щелочного лизиса.Первичную структуру клонированного промотора анализировали методом Максамэ-Гилбертэ. Из анализа пяти клонов видно, что 2-й и 5-9 клоны имеют искомую первичную структуру-го й 5 ф 1ААТТСОАТТАООООАСАСТАТАОСТО 6 А, Проверка промоторной активности (синтез РНК в системе и Иго). 0,2 мкг плазмиды, содержащей промотор, инкубировали в 50 мкл реакционной смеси, содержащей 40 мМ трис-НО, рН 7,5, 6 мМ МДС 2, 2 мМ спермидинэ, Ю мМ дитиотрептол, 0,4 мМ ЧТР, ОТР и СТР, 0,4 мМ ЗН-АТР(1 КЮ/ммоль) при 37 С в присутствии 1-2 ед.акт, РНК-полимеразы ЗРб. Синтезированную РНК определяли в 10 мкл смеси по 5 радиоактивному кислотонерастворимомупродукту нэ счетчике "Магк- И".Результаты синтеза на природном исинтезированном промоторе представлены на чертеже, где дана зависимость включе ния радиоактивных мононуклеотидов в кислотонерастворимый продукт от времени.Видно, что начальные скорости одинаковы.Это свидетельствует о равной эффективности обоих промоторов (у природного 15 нач,скорость 100+10, у искусственного105+Ю)Таким образом, синтезированный олигодезоксинуклеотид отвечает поставленной цели: содержит сайт рестрикции для А 1 ц, 20 является истинным промотором, чья активность сравнима с активность природного.Формула изобретения Фрагмент дезоксирибонуклеиновойкислоты, кодирующий промотор ЯР 6 РНК полимеразы с нуклеотидной последователь- ностью,5-ААТТСОАТТТАООТОАСАСТАТАОСТООА, полученный с помощью химического синте за.
СмотретьЗаявка
4859449, 14.08.1990
НОВОСИБИРСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ ИМ. ЛЕНИНСКОГО КОМСОМОЛА
НАЗАРЕНКО ИРИНА АНАТОЛЬЕВНА, ГОРН ВЛАДИМИР ВИКТОРОВИЧ, АРТАМОНОВА ТАМАРА ПАВЛОВНА
МПК / Метки
МПК: C12N 15/11
Метки: дезоксирибонуклиновой, кислоты, кодирующий, промотор, рнк-полимеразы, фрагмент
Опубликовано: 07.09.1992
Код ссылки
<a href="https://patents.su/3-1759873-fragment-dezoksiribonuklinovojj-kisloty-kodiruyushhijj-promotor-sp6-rnk-polimerazy.html" target="_blank" rel="follow" title="База патентов СССР">Фрагмент дезоксирибонуклиновой кислоты, кодирующий промотор sp6 рнк-полимеразы</a>