Способ получения вакцины против вируса гриппа
Формула | Описание | Похожие патенты | МПК / Метки | Текст | Заявка | Код ссылки
Формула
Способ получения вакцины против вируса гриппа путем прививки поверхностных белков вируса на полимерный носитель, отличающийся тем, что, с целью повышения технологичности способа за счет устранения побочных реакций, повышения эффективности очистки, увеличения иммуногенности, длительности иммунной защиты, в качестве полимерного носителя используют сукцинимидный эфир сополимера N-окиси этиленпиперазина и N-ацетилэтилен-пиперазиний бромида с ММ 20 40 тыс.Д, а в качестве поверхностных белков вируса гриппа смесь гемагглютина и нейтрамидазы при их весовом соотношении и носителю 1:1,5 3, взаимодействия проводят на холоде с последующим выделением и очисткой конъюгата на биогеле P-100.
Описание
Цель изобретения повышение технологичности способа за счет устранения побочных реакций, повышения эффективности очистки, увеличения иммуногенности, длительности иммунной защиты целевого продукта.
Изобретение иллюстрируется примерами.
Пример 1. Получение препарата ИПС-1 проводят в две стадии.
Первая стадия синтез активированного полиоксидония сукцинимидного эфира сополимера N-окиси этиленпиперазина и N-ацетилэтиленпиперазиний бромида по известной методике. 50 мг полиоксидония ( ММ 40 тыс. 0,15 ммоль COOH-группы) суспендируют в 2 мл диметилформамида, добавляют при перемешивании 38,6 мг (0,15 ммоль) дициклогексилкарбодиимида и 18 мг (0,15 ммоль) N-гидроксисукцинимида. Реакцию проводят при перемешивании и охлаждении (2-4oС) в течение 24 ч. Для очистки осадок многократно промывают диоксаном, эфиром и ацетоном, высушивают в вакуумном сушильном шкафу. Отсутствие низкомолекулярных примесей проверяют методом тонкослойной хроматографии на пластинах "Силуфол" в системе н-бутиловый спирт вода - уксусная кислота 4:1:1. Содержание активированных групп определяют стандартным методом (pH 8,5, 0,1 M водородный p-p NH3 259 нм, коэффициент экстинкции
Вторая стадия. 12 мг активированного полиоксидония растворяют в 2 мл фосфатного буфера pH 6,0, 0,05 M. При перемешивании и охлаждении добавляют раствор 4 мг гемагглютинина и нейраминидазы (соотношение соответственно 95:5) в 20 мл фосфатного буфера 0,05 M pH 7,5, содержащего 0,05 M NaCI (соотношение 3:1). Реакцию конденсации проводят в течение 18 ч при 0oC. После окончания реакции смесь наносят на колонку, заполненную биогелем P 100 (2,6 x 60), в качестве элюента используют фосфатный буфер 0,05 M pH 7,5, 0,05 M NaC1. Выход конъюгата (95) контролируют с помощью проточного спектрофотометра при 226 нм, собирают пик, выходящий в свободном объеме. Определение содержания блока проводят методами кругового дихроизма, флуоресцентной спектроскопии. Анализ конъюгата проводят методом электрофореза в ПААГ (10), морфологическое изучение методом электронной спектроскопии (JoeI 100 CX, негативное контрастирование). В 1 мг препарата содержится 0,25 мг белков гемагглютинина и нейраминидазы (процентное соотношение ГА:НА 95:5).
Пример 2. Получение препарата ИПС-3 проводят аналогично приведенному в примере 1 методу. ММ исходного полиоксидония 40000, на второй стадии синтеза в реакцию конъюгации вводят 12 мг активированного полиоксидония и 8 мг белков гемагглютинина и нейраминидазы (соотношение ГА НА составляет 95:5). В 1 мг препарата содержание белков составляет 0,5 мг.
Пример 3. Процесс проводят аналогично примеру 1, используя полиоксидоний ММ 20000, при 0oC и соотношении полимера к белку 1,5:1. В 1 мг препарата содержится 0,5 мг белков гемагглютинина и нейраминидазы.
Пример 4. Процесс проводят аналогично примеру 1 (ММ 20000, соотношение 3:1), при температуре 0oC. В 1 мг препарата содержит 0,25 мг белка.
Пример 5. Процесс проводят аналогично примеру 1 при соотношении полимер: белок, равном 1,5-1, и температуре 4oC. В 1 мг препарата содержит 0,5 мг белка.
Пример 6. Оценка специфической иммуногенной активности ИПС-вакцины.
Опыты проводились на мышах (CBA x C57BL)F1 весом 18 20 г. Мышей иммунировали двукратно внутрибрюшинно ИПС-вакциной, в дозе 0,1 мкг белка (гемагглютинина и нейраминидазы при соотношении 95:5) на мышь. Время между двумя иммунизациями составляет 3-4 недели. Через 12 дней после 2-й иммунизации отбирали кровь и выделяли сыворотку. В качестве контрольной использовали сыворотку неиммунизированных мышей. Для сравнения исследования также сыворотку крови мышей иммунизированных коммерческой инактивированной вакциной, выпущенной предприятием по производству бакпрепаратов им. Пастера (Ленинград), в дозе 5 мкг белка на мышь. Дозу вводили однократно в соответствии с наставлением по применению. Исследовали также сыворотку крови мышей, иммунизированных дважды указанной выше коммерческой вакциной в дозе 0,1 мкг белка на мышь. Проводилось сравнение иммуногенных свойств предлагаемой вакцины и прототипа.
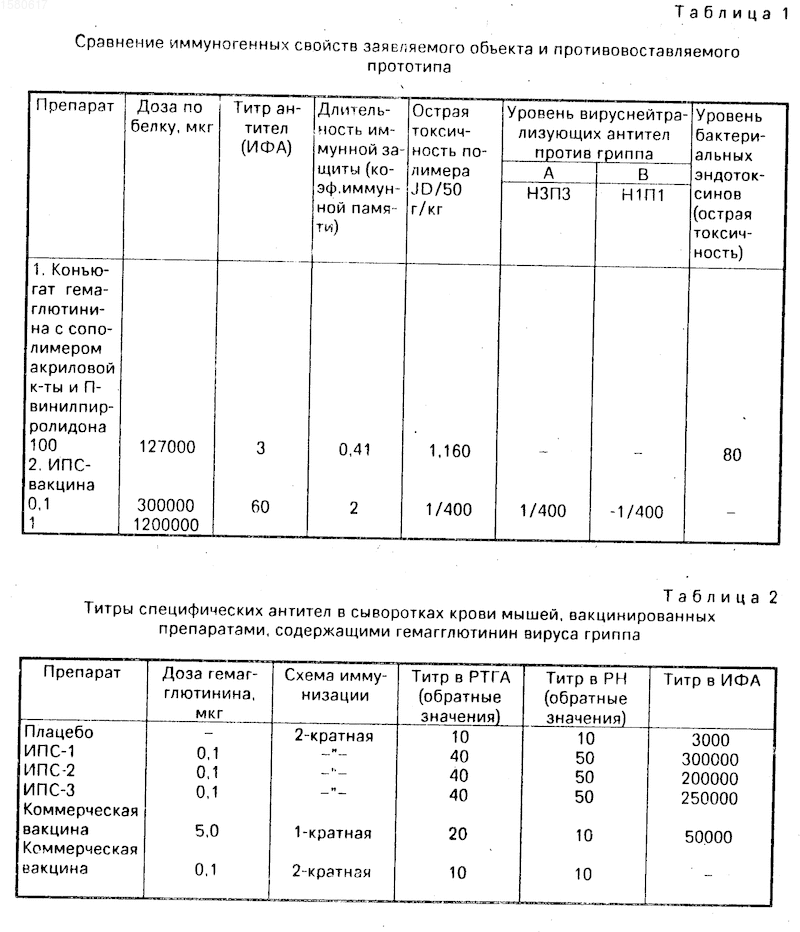
Уровень специфических антител изучали в реакции торможения гемагглютинации (РТГА), в реакции нейтрализации (PH) в стандартной постановке этих методов и методов иммуноферментного анализа (ИФА). За титр сыворотки в РТГА принимали наибольшее разведение сыворотки, при котором отмечается торможение гемагглютинации. За титр сыворотки в реакции нейтрализации принимали ее наибольшее разведение, вызывавшее не менее, чем в 50 эмбрионов (т.е. в 3 эмбрионах из 6) нейтрализацию вируса. Результаты представлены в табл. 1 и 2.
Из представленных в табл. 1 и 2 данных видно, что ИПС-гриппозная вакцина проявляет более выраженный иммуногенный эффект по сравнению с коммерческой вакциной и вакциной по способу-прототипу.
Таким образом, предлагаемый способ получения новой вакцины против вируса гриппа позволяет значительно увеличить иммуногенность, вызвать формирование иммунной памяти, значительно снизить дозу препарата.
Использование в способе носителя позволяет отказаться от конденсации карбодиимидным способом (бифункциональным агентом), который приводит к неконтролируемой сшивке макромолекул и потере функциональных свойств у конъюгета. Использование в качестве сорбента биогеля P-100 позволило существенно повысить процент выхода по конъюгату, который составляет 80 100% по сравнению с выходом 20 30% в способе-прототипе.
Способ заключается в ковалентной конъюгации активированного полиоксидония MM = 20-40 тыс. Д со смесью гемаглютинина и нейраминидазы, причем массовое соотношение полимера к белку составляет 1,5 - 3:1, и процесс ведут при 0-4oC. Предлагаемый способ получения новой искусственной полимер-субъединичной гриппозной вакцины позволяет значительно повысить ее иммуногенность, сформировать иммунологическую память, резко снизить дозу препарата м получить эффект от вируса гриппа актуального штамма. Вакцинный препарат является безвредным и может быть рекомендован для введения людям. 2 табл.
Рисунки
Заявка
4441018/14, 13.05.1988
Институт иммунологии
Петров Р. В, Хаитов Р. М, Некрасов А. В, Мельников С. Я, Атауллаханов Р. И, Пучкова Н. Г, Михеева А. В, Иванова А. С
МПК / Метки
МПК: A61K 39/145
Метки: вакцины, вируса, гриппа, против
Опубликовано: 10.02.1997
Код ссылки
<a href="https://patents.su/1-1580617-sposob-polucheniya-vakciny-protiv-virusa-grippa.html" target="_blank" rel="follow" title="База патентов СССР">Способ получения вакцины против вируса гриппа</a>
Предыдущий патент: Способ изготовления кристаллов резонаторов на поверхностных акустических волнах
Следующий патент: Детектор нейтронов
Случайный патент: Многоканальное устройство для задержки и воспроизведения прямоугольных импульсов