Способ получения иммуностимулирующих тимусных полипептидов
Формула | Описание | Похожие патенты | МПК / Метки | Текст | Заявка | Код ссылки
Номер патента: 1737798
Авторы: Антонов, Безгачев, Граков, Кожевников, Коненков, Лозовой, Мурников, Протопопов
Формула
СПОСОБ ПОЛУЧЕНИЯ ИММУНОСТИМУЛИРУЮЩИХ ТИМУСНЫХ ПОЛИПЕПТИДОВ, включающий гомогенизацию сырья в растворе хлористого натрия, центрифигурирование, нагревание недостаточной жидкости до 80oС и инкубацию, удаление осадка, охлаждение, обработку ацетоном, формирование преципитата, его высушивание, растворение ацетонового порошка в трис-HCl буфере, центрифугирование, хроматографию на сефадексе супернатанта с последующим сбором фракций, содержащих целевой продукт, его лиофилизацию, тельфильтрацию, повторную лиофилизацию, отличающийся тем, что, с целью повышения активности целевого продукта, в качестве сырья используют тимус северного оленя, который забирают у животных в возрасте до 3,5 лет, перед центрифугированием гомогената проводят его аутолиз, а перед хроматографией супернатант ультрафильтруют через мембраны с пределом удержания по белку 6000 - 12000 дальтон, гельхроматографию проводят на сефадексе 6 - 50 и собирают фракции, содержащие целевой продукт с мол.м. 1350 - 6000 дальтон, относительным содержанием пептидов и соединений нуклеотидной природы 1,4 - 1,6, удельным показателем поглощения Е10,1% см при длине волн 275 нм, равным 0,650 - 0,750, удельным вращением 1%-ного водного раствора от 75 до 85o.
Описание
Целью изобретения является повышение активности целевого продукта.
Способ осуществляется следующим образом.
Очищенный от жира и соединительной ткани тимус северного оленя от животных не старше 3,5 лет гомогенизируют в растворе 145 мМ хлористого натрия в соотношении 1:3, выдерживают в течение 12-18 ч при температуре 2-6оС, ядра и осколки мембран удаляют центрифугированием при 1500-2000 g или фильтрацией через капроновый или бязевый фильтр. Супернатант прогревают до 80оС и выдерживают при этой температуре 15 мин. Денатурированные белки удаляют центрифугированием или фильтрацией. Супернатант или фильтрат охлаждают до 0оС и медленно по каплям добавляют при интенсивном перемешивании в 5-кратный объем охлажденного до -20оС ацетона и оставляют при постоянном перемешивании и температуре -10-15оС на 18-20 ч. После этого выключают мешалку и формируют осадок, который трехкратно отмывают ацетоном, декантируют и высушивают под тягой.
Сухой ацетоновый порошок растворяют в 0,01 М трис-HCl буфере, декантируют нерастворимый осадок центрифугированием, повторяют растворение и доводят концентрацию белка в супернатанте до 10 мг/мл. Полученный раствор фильтруют через мембраны типа РМ-10, УМ-10 (Амикон) или любую другую аналогичную по размеру пор мембрану либо используют полые волокна с номинальными пределами удержания по глобулярным белкам от 6000 до 12000 дальтон. Образовавшийся на мембране осадок трижды промывают буфером, фильтрат объединяют и лиофилизируют.
Лиофилизированный препарат хроматографируют на колонке с гелем с разрешающей способностью от 1,3 до 30 кД (например, на сефадексе С-50, ультрагеле АсА 202) уравновешенным 0,05 мМ, трис-HCl буфером, рН 8,0 на 145 мМ хлористом натрии. Пептиды с мол.м. 1350-6000 дальтон собирают, лиофилизируют, обессоливают на сефадексе С-50, лиофилизируют и используют в тестах определения биологической активности.
В азотиапрановом тесте изучалась активность ультрафильтрата и активность продукта на стадии хроматографического фракционирования на сефадексе С-50.
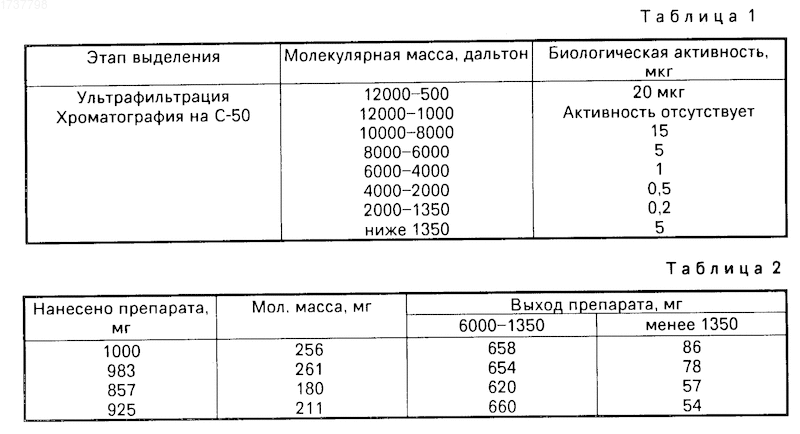
Результаты сравнительного изучения активностей разных фракций препарата представлены в табл. 1.
Результаты по выходу препарата по фракциям при нанесении на колонку с сефадексом С-50 препарата представлены в табл. 2.
Результаты, представленные в табл. 1 и 2, показывают, что фракция 6000-1350 максимально активна и на ее долю приходится более чем на 65% от общей суммы фракций по выходу их на заключительном этапе.
Сравнительный анализ активностей конечного продукта в изобретении и способе-прототипе в тесте определения биологической активности по восстановлению чувствительности Е-РОК селезенки тимэктомированных мышей С 57 В 1/6 показал, что активность целевого продукта, полученного по способу-прототипу, составила 10 мкг, а активность целевого продукта с мол.м. 1350-6000 дальтон, полученного по предложенному способу 0,5 мкг, т.е.
По данным исследований препарата "Олевил", проведенных Новокузнецким химико-фармацевтическим институтом по программе Фармкомитета на экспериментальных животных, он не обладает острой токсичностью при введении животным в дозе 100 мг/кг массы тела, не обладает пирогенностью, не являетcя аллергеном. В терапевтических дозах (1 мкг/кг) не влияет на анафилактические реакции, в дозе 5 мг/кг достоверно снижает проявления анафилактического шока. Препарат на тератогенен и не эмбриотоксичен в дозах, превышающих терапевтическую в 100 раз.
Таким образом, выделяемые по способу пептиды обладают более высокой по сравнению с прототипом активностью (в 20 раз), являются более гомогенными (мол. м. 1350-6000 л) по сравнению с прототипом и могут быть охарактеризованы такими общими физико-химическими свойствами: водный (0,1%) раствор имеет максимум поглощения при 275 нм. Отношение оптических плотностей при 280 и 260 нм (характеризует относительное содержание пептидов и соединений нуклеотидной природы) находится в пределах 1,4-1,6. Удельный показатель поглощения Е10,1% см для конечного продукта составляет 0,650-0,750. Удельное вращение 1% раствора препарат должно быть 75-85о.
Предложенный способ позволяет получить тимусные полипептиды аналогичного действия, что и прототип, но обеспечивает получение продукта с более высокой по сравнению с прототипом активностью.
Изобретение относится к получению биологически активных веществ из сырья животного происхождения, которые могут найти применение в медицине и ветеринарии. Целью изобретения является повышение активности целевого продукта. Поставленная цель достигается за счет того, что тимус дикого северного оленя в возрасте до 3,5 лет гомогенизируют в растворе хлористого натрия, гомогенат выдерживают 12 - 18 ч при 2 - 6°С, удаляют осадок, нагревают до 80°С и выдерживают при заданной температуре 15 мин, удаляют осадок, охлаждают, надосадочную жидкость обрабатывают ацетоном, формируют приципитат, который высушивают, растворяют в трис-HCl буфере, ультрафильтруют через мембраны с номинальными пределами удержания по глобулярным белкам 6000 - 12000 дальтон, хроматографируют на сефадексе С-50, собирая фракцию с мол.м 1350 - 60000 дальтон. 2 табл.
Рисунки
Заявка
4678398/14, 11.04.1989
Институт клинической иммунологии СО АМН СССР, Красноярский медицинский институт
Безгачев В. Г, Кожевников В. С, Лозовой В. П, Граков Б. С, Коненков В. И, Протопопов Б. В, Мурников В. Т, Антонов И. В
МПК / Метки
МПК: A61K 38/00
Метки: иммуностимулирующих, полипептидов, тимусных
Опубликовано: 20.03.1995
Код ссылки
<a href="https://patents.su/0-1737798-sposob-polucheniya-immunostimuliruyushhikh-timusnykh-polipeptidov.html" target="_blank" rel="follow" title="База патентов СССР">Способ получения иммуностимулирующих тимусных полипептидов</a>
Предыдущий патент: Насосная станция
Следующий патент: Сепаратор пароводяной смеси
Случайный патент: Устройство для выделения признаков при распознавании образов