Способ получения несимметричных дибензо-краун-эфиров
Похожие патенты | МПК / Метки | Текст | Заявка | Код ссылки
Номер патента: 1728246
Авторы: Городнюк, Иванов, Котляр, Лукьяненко
Текст
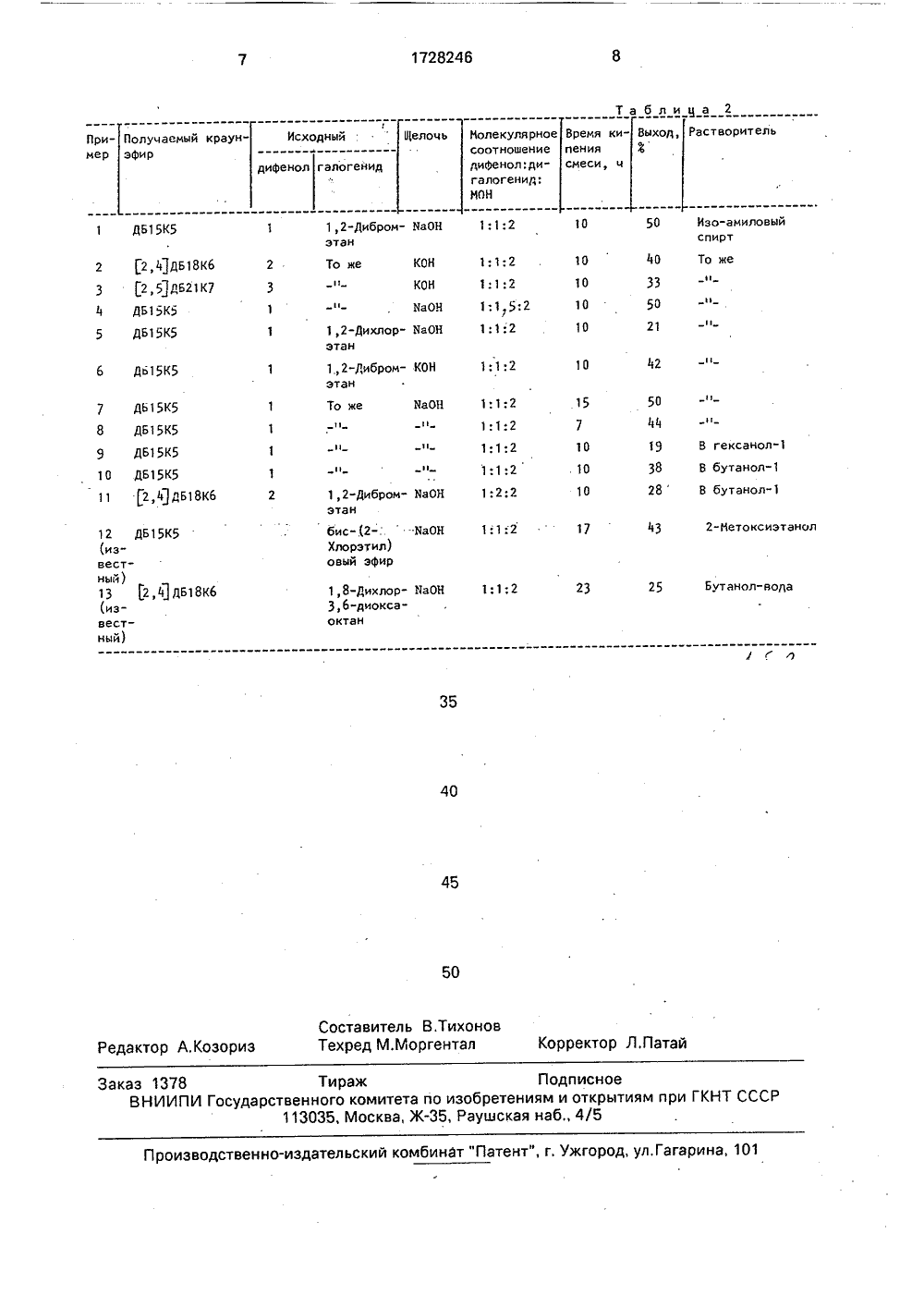
(19), (1) 1)5 С 07 О 323/О 8 Ц Н 0 ИОЮЗИАЙАЯМЖк наев А й институт к, О,В.Иванов динения, М.: Изобретен химии, а именн ных дибензоспособу полу 2,4 дибензокраун:-ОиО О ДБ 15 К 5 оторые испол онов ионов ых металлов олидибензокИзвестен 5-крауни лючд ющийс ГОСУДАРСТВЕННЫЙ КОМИТЕТПО ИЗОБРЕТЕНИЯМ И ОТКРЫТИПРИ ГКНТ СССР ИСАНИЕ ЗОБ ОРСКОМУ СВИДЕТЕЛЬСТВУ(54) СПОСОБ ПОЛУЧЕНИЯ НЕСИММЕТРИЧ Н ЫХ ДИ БЕ НЗО-КРАУН-ЭФИРОВ(57) Изобретение касается краун-эфиров, вчастности получения дибензо-крауние относится к органической о к получению несимметричкраун-эфиров, конкретно к чения дибензо-краун, -крауни 2,5 дибензо,4 ДБ 18 К 6 2,5 ДБ 21 К 7 ьзуются в качестве комплекщелочных и щелочноэемельи как мономеры для синтеза раун-эфиров.способ получения дибензо,4 дибензо-краун, зая в алкилировании 5,2,4-дибензо-крауни/или 2,5 дибензо1-краун, используемых в качестве комплексонов щелочных и щелочно-земельных металлов, Цель - расширение ассортимента получаемых продуктов и интенсификация процесса, Его ведут реакцией бис-(2-гидроксифенил) эфира олигоэтиленгликоля с последовательно добавляемой щелочью (КОН или МаОН) при одновременной отгонке образующейся воды с образованием соответствующей соли, которую при кипячении алкилируют 1,2-дибромэтаном в среде,изоамилового спирта. Эти условия обеспечивают в одну стадию, выход целевых веществ 33 - 500(, при длительности процесса до 10 ч против 17 - 23 ч, 2 табл. 1,2-бис-(2-гидроксифенокси)-этана бис-(2- хлорэтил)овым эфиром или 1,8-дихлор,6- диоксаоктаном в присутствии гидроксида натрия в 2-метоксиэтаноле или в водном бутаноле.Этому способу присущи следующие недостатки; длительность процесса (17 - 23 ч), трудоемкость получения исходного 1,2-бис- (2-гидроксифенокси)-этана; отсутствие данных о получении 2,5 дибензо-краун(недостаточная универсальность метода),Цель изобретения - расширение ассортимента целевых продуктов и сокращение времени процесса.Поставленная цель достигается тем, что согласно способу получения несимметричных дибензо-краун-эфиров, включающему взаимодействие бис-(2-гидроксифенил) ового эфира с галоидным алкилом и гидроксидом щелочного металла в спиртовой среде с последующим выделением целевого про 1728246О ОО ОН НО дукта, в качестве бис-(2-гидроксифенило)вого эфира используют соединение формулы где п =1,2,3,при этом к соответствующему бис-(2-гидроксифенил)овому эфиру олигоэтиленгликоля прибавляют гидроксид щелочного металла, уДаляют из реакционной смеси воду, а затем образующуюся смесь кипятят с 1,2-дибромэтаном в среде изо-амилового спирта.Процесс проводят в одну стадию без выделения промежуточного продукта - динатриевой (дикалиевой) соли бис-(2-гидроксифенил)ового эфира олигоэтиленгликоля.Используя в известном способе 1,5-дихлор-оксапентан(дихлорид диэтиленгликоля) и 1,8-дихлор,6-диоксаоктан (дихлорид триэтиленгликоля)не подвергаются щелочному/3-дегидрогалоидированию в присутствии образующихся при реакции с 1,2-бис-(2-гидроксифенокси)-этаном дибензо-краун-эфиров: дибензо-крауни (2,4-дибензо-краунв такой степени, в какой это имеет место для 1,2-дибромэтана (дибромида этиленгликоля), о чем свидетельствуют 25 - 43 - ные выходы указанных дибензо-краун-эфиров.Попытка получить (2,5-дибензо-крауниз 1,2-бис-(2-гидроксифенокси)-этана и 1,11-дихлор,6,9-триоксаундекана привела к образованию следовых количеств продукта (по данным ГЖХ), Данный факт подтверждает невозможность получения (2,5-дибензо-крауниз 1,2-бис-(2-гидроксифенокси)-этана.Для предотвращения побочной реакции Р- дегидробромирования 1,2= дибромэтана находящейся в реакционной смеси щелочью применено удаление из реакционной смеси воды на стадии получения динатриевой (дикалиевой)соли бис-(2-гидроксифенил)ового эфира олигоэтиленгликоля (образование подобной соли без удаления воды из сферы реакции обратимо),Способ осуществляют следующим образом.Смесь бис-(2-гидроксифенил)ового эфира олигоэтиленгликоля формулы (11) и водного раствора йаОН или КОН в изо-амиловом спирте кипятят с водоотделителем до полного удаления воды из реакционной смеси,5 10 15 20 25 30 35 40 45 50 55 затем к последней прибавляют 1,2-дибромэтан, кипятят смесь 10 ч, и после отгонки изо-амилового спирта проводят экстракцию продукта - смесью бензол-гептан из кипящего водно-щелочного раствора. Полученный сырой продукт подвергают перекристаллизации из гептана,П р и м е р 1. Получение дибензо-краун, Суспензию 58,0 г (0,2 моль) 1,5-бис(2= гидроксифенокси)-3-оксапентана (1) и 700 мл изо-амилового спирта нагревают при перемешивании до образования гомоген ного раствора, добавляют 28,0 мл 40%-ного водного раствора (0,4 моль) МаОН и кипятят с водоотделителем Дина-Старка в атмосфере азота до прекращения отделения воды (31 - 31,5 мл) около 1 ч. Затем к образовавшемуся раствору при кипячении и перемешивании прибавляют по каплям раствор 37,6 г (0,2 моль) 1,2-дибромэтана в 20 мл изо-амилового спирта в течение 10 мин. Смесь кипятят при интенсивном перемешивании еще 10 ч, охлаждают, фильтруют, фильтрат упаривают досуха в вакууме.Остаток растворяют в 100 мл 5 н. раствора КОН, добавляют 100 мл смеси бензол-гептан (2:3) и кипятят при сильном перемешивании 10 - 15 мин, горячий органический слой отделяют декантацией. Описанную "горячую" экстракцию проводят еще дважды, Органические экстракты объединяют, охлаждают до 10 С, выпавший осадок отфильтровывают сушат и перекристаллизовывают из минимального количества гептана, Бензольно-гептановый фильтрат упаривают досуха и описанной экстракцией и последующей перекристаллизацией из гептана выделяют дополнительное количество продукта, Выход продукта 31,6 г (50).Физико-химические характеристики и данные элементного анализа приведены в табл. 1; сведения о режимах выполнения примеров 1 - 13 и их результатах - в табл. 2.П р и м е р 2 - 3, Выполняются аналогично примеру 1 и иллюстрируют выполнение способа с целью получения (2,4-дибензо-крауни 2,5-дибензо-краун -7 соответственно,П р и м е р 4, Иллюстрирует выполнение способа при избытке 1,2-дибромэтана.П р и м е р 5. Иллюстрирует выполнение способа при эквимолярном соотношении реагентов с использованием в качестве алкилирующего агента 1,2-дихлорэтана. Понижение выхода до 210 связано с более низкой температурой кипения реакционной смеси (83 С против 124 С для примеров 1-11).П р и м е р 6. Иллюстрирует выполнение способа с применением КОН в качестве тем(2,5)Дибензокраун33 50-51 65,29 7 э 07 С 2 Рз 07 платного основания (ион К имеет радиус больший, чем полость макроцикла дибензо-к раун).П р и м е р 8, Иллюстрирует выполнение способа при большей продолжительности 5 процесса,Пример 7.Иллюстрирует выполнение способа при меньшей продолжительности процесса.Пример 9,Иллюстрирует выполнение 10 способа в более высококипящем гексаноле. Падение выхода целевого продукта обусловлено из-за сильного осмоления реакционной смеси вследствие высокой температуры последней, 15П р и м е р 10. Иллюстрирует выполнение способа в бутаноле. Снижение выхода целевого продукта связано с большей растворимостью воды в бутанолепо сравнению с изо-амиловым спиртом и, как 20 следствие этого, - неполным обезвоживанием реакционной смеси. Таким образом, предлагаемый способ . по сравнению с известным ускоряет прове 25 дение процесса в 2 раза: с 17-23 ч до 10 ч;позволяет получать с выходом 33 О 2,5-дибензо-краун, что указывает на большую универсальность. Формула изобретенияСпособ получения несимметричных дибензо-краун-эфиров формулы35 1где и =1,2,3,взаимодействием бис(2-гидроксифенилового(эфира олигоэтиленгликоля с галоидным алкилом и гидроксидом щелочного металла вспиртовой среде,отличающий ся тем, что, с целью интенсификации процесса и расширения ассортимента, в качестве бис(2-гидроксифенилового)эфира олигозтиленгликоля используют бис(2-гидроксифениловый)эфир олигоэтиленгликоля формулы И где п имеет указанное значение,а в качестве галоидного алкила используют 1,2-дибромэтан и процесс проводят последовательным добавлением гидроксида щелочного металла к бис(2-гидроксифениловому)эфиру олигоэтиленгликоля, удалением воды и обработкой реакционной смеси 1,2-дибромэтаном в среде изоамилового спирта при кипячении. 68,34 6,37 3,6-4,1 м1728246 та бли ца 2 Получаемый краунэфир Растворитель Время кипениясмеси, ц Исходный Выход,В Щелоць Пример галогейид дифенол ДБ 15 К 5 50 Изо-амиловый спирт1;1:2 10 1,2-Дибром- ЧаОНэтан КОН То же 10 КОН 10 НаОН 10 1,2-Дихлор- НаОНэтан 42 10 1;1:2 6 ДБ 15 К 5 1,2-Дибром- КОНэтан 15710 Дь 15 к 5 8 ДБ 15 К 5НаОН То же 1 О 1,2-Дибром- НаОНэтан 10 11 2 бис-,(2-:."НаОН Хлорэтил)овый эфир 43 2-Метоксиэтанол 17 1 8 Дихлор НаОН 3,6-диокса- октан 25 Бутанол-вода 1;1;2л 35 40 45 50 Составитель В.ТихоновРедактор А.Козориз Техред М.Моргентал Корректор Л,Патай Заказ 1378 Тираж Подписное ВНИИПИ Государственного комитета по изобретениям и открытиям при ГКНТ СССР 113035, Москва, Ж, Раушская наб., 4/5 Производственно-издательский комбинат "Патент", г. Ужгород, ул.Гагарина, 101
СмотретьЗаявка
4800070, 11.03.1990
ФИЗИКО-ХИМИЧЕСКИЙ ИНСТИТУТ ИМ. А. В. БОГАТСКОГО
КОТЛЯР СЕРГЕЙ АНАТОЛЬЕВИЧ, ГОРОДНЮК ВИКТОР ПЕТРОВИЧ, ИВАНОВ ОЛЕГ ВИКТОРОВИЧ, ЛУКЬЯНЕНКО НИКОЛАЙ ГРИГОРЬЕВИЧ
МПК / Метки
МПК: C07D 323/00
Метки: дибензо-краун-эфиров, несимметричных
Опубликовано: 23.04.1992
Код ссылки
<a href="https://patents.su/4-1728246-sposob-polucheniya-nesimmetrichnykh-dibenzo-kraun-ehfirov.html" target="_blank" rel="follow" title="База патентов СССР">Способ получения несимметричных дибензо-краун-эфиров</a>
Предыдущий патент: Способ получения оксида гексафторпропилена
Следующий патент: Способ получения 1 -(азиридинил-1)алкил-2, 5 диметилпирролов
Случайный патент: Устройство для смены кассет с дисками