Цис-хлордиаммин-1, 3-диметилксантинплатины (ii) хлорид дигидрат, проявляющий противоопухолевую активность
Похожие патенты | МПК / Метки | Текст | Заявка | Код ссылки
Номер патента: 1790190
Авторы: Бодягин, Иванова, Имсырова, Камалетдинов, Козлов, Коновалова, Переверзева, Стеценко, Трещалин, Яковлев
Текст
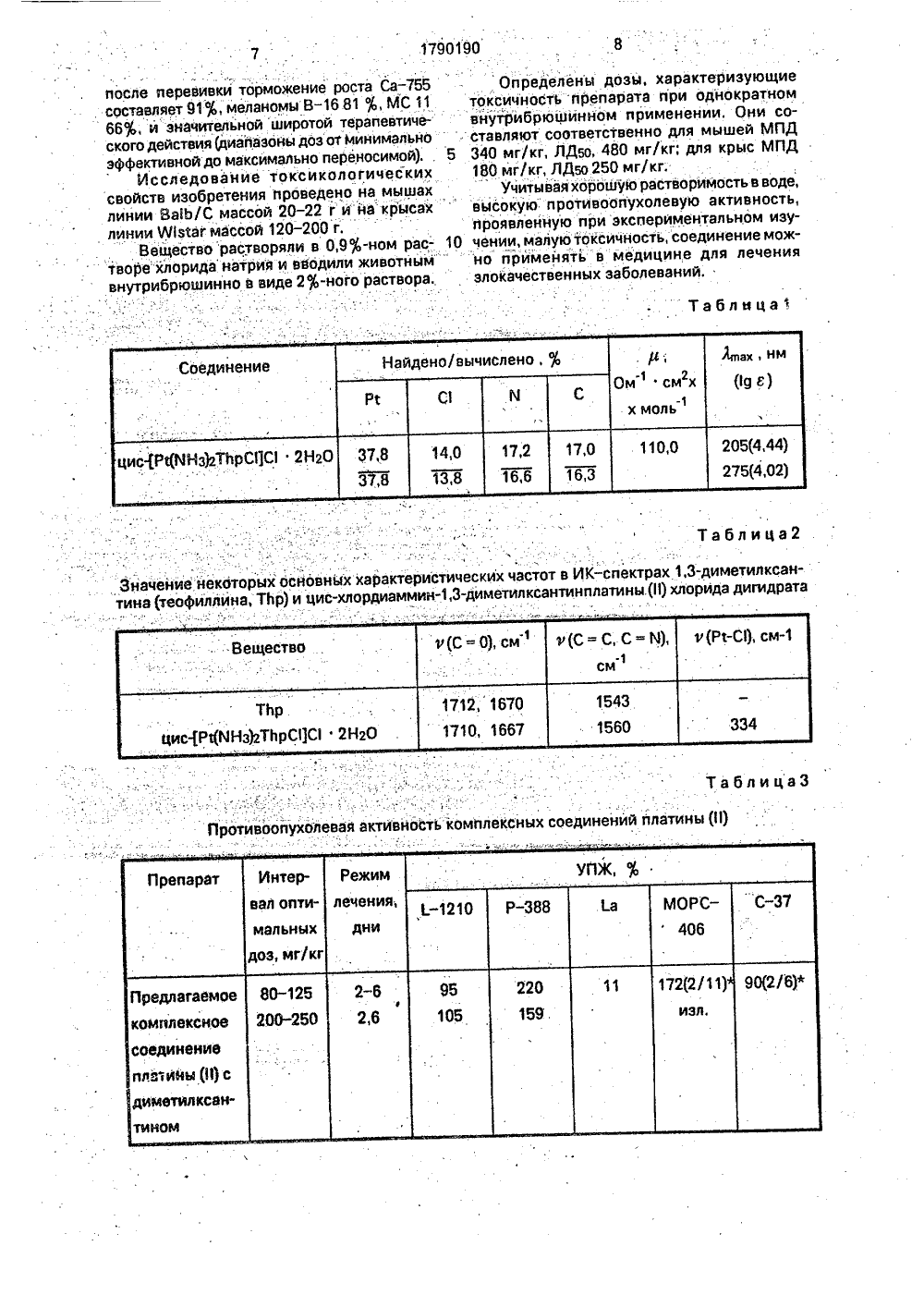
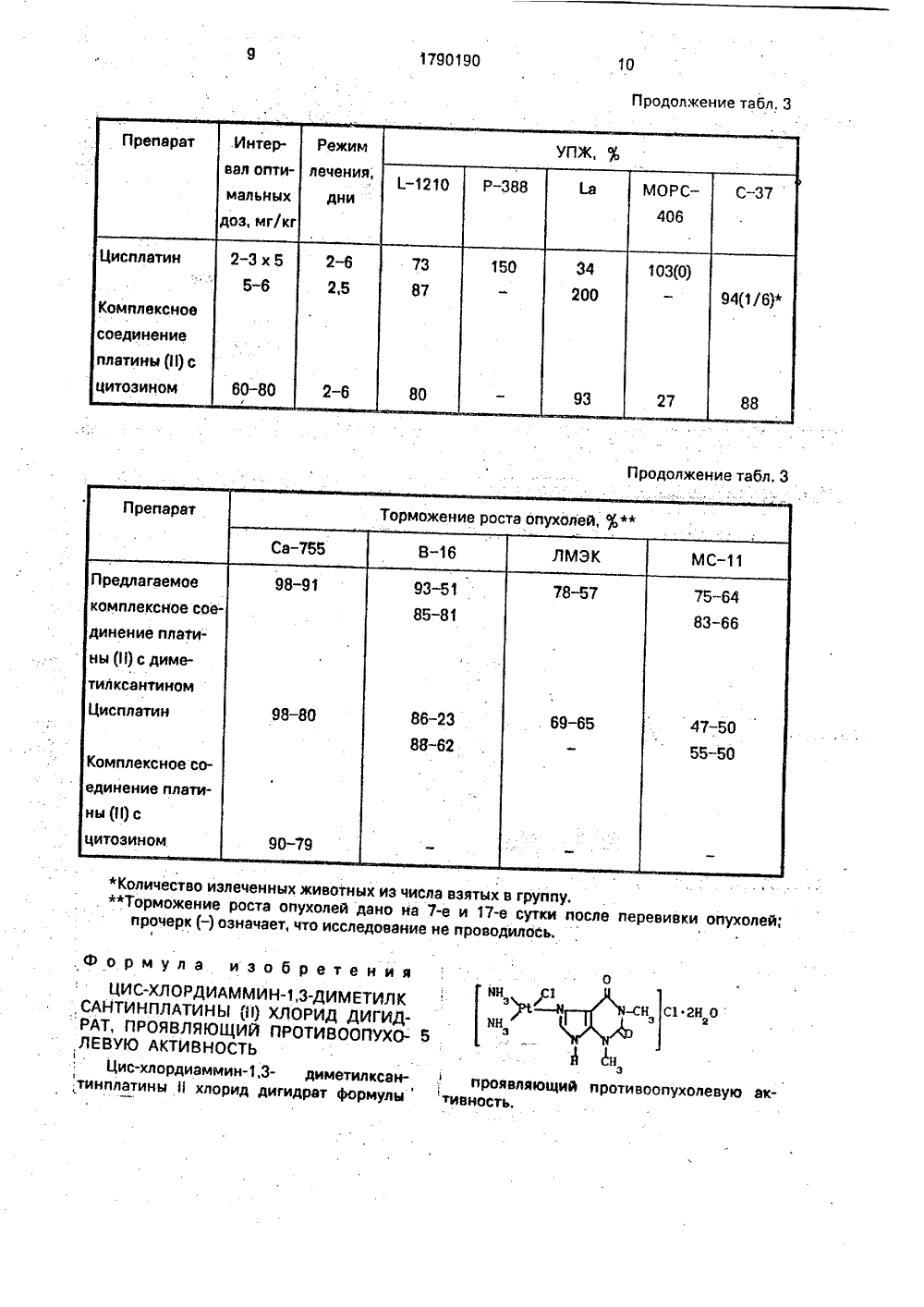
9019 О (1 З) А 00 А 61 К 31/295 19) ЗХЗ (11) 151) 6 С 07 Р рог) ОПИСАНИЕ ИЗОБРЕТЕНИЯк авторскому свидетельству 3-ДИМЕТИ ЛОРИД ДИ- ПРОТИВО- Ь(54) ЦИС-ХЛОРДИА ЛКСАНТИНПЛАТИН ГИДРАТ, ПРОЯВЛ ОПУХОЛЕВУЮ АК (57) Использование; обладающего против стью, Сущность изо хлордиаммин,3-дим (11), БФ С 7 Н 18 С 2 М200 С с р о дихлордиаммин плати метилксантин, Усло при рН 2, при нагре не, 3 табл,ММИН Ы (11) ЯЮЙЦИЙ ТИВНОСТ в качест оопухолев бретения; етилксант 604 Р 1, вы ением, Р на. Реаге вия реак ванин на Комитет Российской Федераципо патентам и това ным знакам(71) Ленинградский химико-фармацевтический институт, Всесоюзный онкологический научный центр АМН СССР(56) "С з-ра 1 и". Сштеп 1 з 1 а 1 цз Хев Вечеораеп 1 з. Ед. А. К, Ргпз 1 а 1 о, 8, Т. Сгоойе, Х. 3. К, СагЬоп, р, 317, Асад, Ргезз, 1980. Авторское свидетельство СССР Х 1085209, кл. С 07 Р 15/00, 1988. ве препарата, ой активнопродукт-цис инплатина ход 75%, т. еагент 1:циснт 2: 1,3-диции: в воде кипрей ба 1790190Изобретение касалеттся изыскания комп лексных соединений платины (И), обладающих противоопухолевой активностью, а именно препарата цис-хлордиаммин,3- диметилксантинплатины (И) хлорид дигидрат формулы МК ц С 1зГ : цнт Н С 12 зСН К известным противоопухолевым препаратамплатины относятся цис-дихлордиаминплатина(сзратпа, ра 1 с 1 ат,. раппо, пес рат и); цис-хлордиамийцитозинплатины (И) хлорид,Препарат цис-дихлордиаминплатина (И)относится к классу неэлектролитнцх ком.плексов платины. Недостатком этого пре"парата является невысокая воднаяраствбримость (0,1 оп), что осложняет клиническое применеййсе и технологйю "выделения" препарата методом лиофилизации.Недостатком препарата ци 6-хлодиэсминцитозинплатины (И) хлорид служит неустойчивость по отношению к кислороду воздуха вводном и физиологическом растворах, чтогриводист к образованию окрашейных примеСей, содержащих трехвалентную платину, и вызывает необходимость прйменятьйрепсасрнат сразу пОсле его растворения,Цель изобретения- синтез водорастворимого и устойчивого в водной среде, активного и малотоксич ного катион ногокохМплекса платины (П) триаминового типацис-рстроейия, содержащего молекулу. гетероцйклйчесского взотсодержащего лиганда,Отличие в строении и свойствах цисхлЬфнэмми н,3-дйметилкса нтин платины(1) иоридса дихгтихдх"ранта"от йеэлхехктролиптиыхкомЗЙксохв платины (И) заключается в следйщйй; комплекс содержит однозарядныйкатион платины (И); наличие в комйлексемолекулы липофильного лигандэ,3-дйме.йелксайтина (теофиллина, ТЬр)-способствус- Фст "ллирйхоп"фильн-ости комплекса и егоМбйбрйннотй проницаемости: наличие одноге а недвух, как в цис-дихлордиаминплатийец , ихойссах хлОра делает комплексС 46 бббйй К"ситному, чем у незлектролитов,Щ взаймодействия с ДНК, а именно кМбаофсунксцоиональному, а не бифункцио яФМНФй, как у неэлектролитов, связываййо. Различйе вмеханизме биохимического3 ИВтвиях катионных и неэлектролитныхкояеплькс сов перспективно е целях риффе. ренциации и возможного расширения противоопухолевого действия препаратов платины.К преимуществам изобретения в хими 5 ческом отношении следует отнести(по сравнению с прототипом), хорошую воднуюрастворимость (10); большую устойчивость по бтношению к окислению и при хранении в водной среде; больший выход в10 процессе синтеза (70 - 80 оь) и отсутствие вконечном продукте примесей трехвалентной платйны.Цис-хлордиаммин,3-диметилксантинплатиныхлорйд дигидрат получают вза 15 имодействием цис-(Рт(МНз)2 С 2) и 1,3-диметилксантина. Реакцию проводят всолянокислой среде (рН 2) при нагреваниина кипящей водяной бане взвеси в водеэквимолярных количеств реагирующих ве 20 ществ. Целевой продукт выделяют ацетоном в виде белого пЬрошка (пример 1).Состав и координсационная формула установлены элементным анализом и измерением молярной электропроводности (см. табл.25 1), Индивидуальность и чистота соединениядоказана методом тонкослойной хроматографии на пластинкаМ иСилуфол УФ" вдвух системах растворителей: 1 - этанол";ацетон:вода;уксусная кислота30 (конц,);аммиак (конц,)=50;40:10;10:10 (пообъему); 2 - пропанол:вода:уксусная кислота (конц,):аммиак (конц,)=70;30:10:10 (пообъему). Комплекс хроматографировался вобеих системахв виде одного пятна с35 Вг=0,62 (система 1) и 0,58 (система 2). Детекция пятен проводилась в парах иода и вУФ-излучении,Растворймость комплекса в воде 10.При нагревании до 200 ОС комплекс раэлага 40 ется до начала плавления. Для соединенияхарактерно наличие в УФ-спектре полосыпогхлощейия, характеристики которой приведены в табл. 1 Л пах и 9 я-длинаволны вмаксимуме полосы поглощения и логарифм45 коэффициента молярного погашения приэтой длйневолны.Ввиду йевозможности проведения рен-.тгеноструктурного анализа (из-за отсутствия монокристаллов) структура соединения50 определена методами МПР- и ИК-спектроскопии (табл, 2),Излучение спектров протонного маг-.нитного резонанса (ПМР) свободного теофиллина и предлагаемого соединения в55 дейтерированном диметилсульфоксиде(ДМСО-бб) показало, что в комплексе сигнал нелабильного протона Н(8) теофиллина(д =8,50 м. д.) сдвинут по сравнению со свободными лигандами (д =8,00 м, д,) в слабое."5 1 790 1 9 0 6поле на 0,50 м, д, В то же время в спектре СЕ 5 от, н, доза, вызывающая 50% тормоПМР комплекса наблюдается спин-спино- жения включения меченого тимидийавнвое взаимодействие протона Н(8) с магнит- клетки СаОЧ для ан ного соединенияым ядром изотопа Рт с константой составляет 6 10 М, для препарата1195 Р-н(8)=80 Гц, Полученные данные сви сравнения "(цисплатина) 5 10 6 М, Это свидетельствуют об участии к Н(8) атомов азота детельствует о меньшей молярной токсичимидазольного цикла в координационной ности полученного соедйнения.связи, что позволяет сделать однозначныйИзлучение противоопухолевой активновыводобобразованиисвязи Р 1 - й. сти йроведено на мышах линий СнВ 1,Как видно иэ табл,2, частоты полос по ВА 1 ЬС, гибридах первых ВОР, (С 5 тВ 1 Хглощения карбонильной группы .и(С=О) ДВА) и беспородных животных.практически не меняются при комплексооб- Использованы следующйе перевиваеразовании, чтосвидетельствует об отсутст- мые опухоли и лейкозы: лимфоидная лейкевии связи Р 1 - О, В то же время увеличение мия 1-1210, гемоцитобластоз 1 а, лейкозчастоты (С=С, С=К) на 17 см указывает на 15 Р - 388, плазмацитома МОРС - 406, асцитнаяобразование связи платины с гетероцикли- саркома 37, меланома В - 16, аденокарциноческим азотом лиганда, что подтверждает: ма молочной железы Са - 755, фибросаркомавыводы, сделаннЬе при изучении спектров МСи лимфогенно метастазирующая эмПМР, Наличие полосы поглощения Р(Рс - бриокарцинома(ЛМЭК),С) 334 см в ИК-спектре комплекса доказы Вещества вводили в физиологическомвает содержание в нем внутрисферного растворе хлористого натрия внутрибрюиона хлора.Пшинно. Схемы терапии различны: однократр и м е р. Навеску комплекса цис- ная ийьекция вмаксимально "переносимой,Рс(ИНз)2 С 2)(0,6 г,2 ммоль) и 1,3-диметилк- дозе (МПД), ежедневное введение в течесантина (0,35 г, 2 ммоль) помещают в стакан 25 ние 5 дней и с интервалами в 96 ч, Терапевс 50 мл дистиллированной воды, подкислен- . тический эффект оценивали по торможениюной до рН 2 соляной кислотой, закрывают роста солидных опухолей; увеличейию прочасовым стеклом и нагревают в течение 2 ч должительности жизни леченьях животнцхна кипящей водяной бане, поддерживая по сравнению с контролем (УПЖ) и излечеуровень воды в стакане, Далее смесь охлаж нию животных,дают при комнатной температуре, отфильт- Установлено,что терапевтические дозыровьвают от остатка непрореагировавшихв зависимости от штамма и линии животныхисходных веществ, испаряютпри комнат- находятсяв"йределах 80-120 мг/кг при 5 ной температуре до объема 3 мл и выделяют дневном"лечеййи, МПД при однократномконечный продукт добавлением 15-кратно введении 340 мг/кг.го избытка ацетона. Белый осадок конечногоРезультаты исследования, полученныепродукта отфильтровывают на воронке Гир-, при оптимальных дозах и режиме применеша, отсасывая досуха, промывают ацетономния препаратов, представлены в табл. 3,и высушивают на воздухе втечение 3 ч и далее Как видно из данных табл. 3, полученноедо постоянной массы при температуре 70 С. 40 соединение имеет широкий спектр противоод 0,85 г(75от теоретического), опухолевогодействия и проявляет высокуюИзучение биологической активности активность как при гемобластозах, так и напроведено "инвитро" и "ин вива" наразлич- асцитйых и плотных опухолях; на ряденых перевиваемых опухолях животных штаммов по эффективности значительно,Все исследования проведены в сравне превышаетсравниваемые аналоги (на 1:нии с близкими аналогами полученного со, Р, МОРС, МС - 11). На чувстединения: хлор-цис-диамминцитозинпла- вительных кпрепарату" опух 0 ляхтины (И) хлоридом и цис-дихлордиамминп- (МОРС - 406, С - 37) помимо увеличения пролатиной (11), получавшей название "циспла- должительности жйзни излечивает частЬтин" и широко применяемой в клинике для 50 животных (330). Цисплатин лишь увелйчилечения онкологических заболеваний, вает продолжительность"жизни животных СИсследование цитотоксической актив- плазмацитомой МОРС, без излечения.ости цис-хлордиаммин,3-диметилксан- В то же время вещество полностью неактиатинплатины (11) хлорида проведено на но на лейкозе 1 а, т, е. имеет определенныеклетках карциномы яичников человека 55 отличия по спектру противоопухолевого(СаОЧ) радиометрическим методом по влия- действия от сравниваемых препаратов.ток СаОЧ, Испю на включение Н-тимидина в ДНК кле- Полученное соединение характер э еиутСаОЧ, Использованы концентрации от сябольшойдлительностьюсохранени проятивоопухолевого.эффекта: на 17-е сутки7 . 1790190 8 Табл мца 1 а блица ТЗначение йекоторых основных характеристических частот в ИК-спектрах 1,3-диметина (теофиллина, Тпр) и цис-хлордиаммин,3-диметилксантинплатины. (И) хлорйда илксангидрат. вность кблица 3 Протйвоопухолевая лексных соединений йлатины И) после перевивки торможение роста Са. составляет 91, меланомы В81 , МС 11 66, и значительной широтой терапевтического действия (диапазоны доз от мийимально эффективной до максймально переносимой).Исследование токсикологических свойств изобретения проведено на мышах линии Ва 1 Ь/С массой 20-22 г и йакрысах линии Изтаг массой 120-200 г.Вещество растворяли в 0,9-ном растворе хлорида натрия и вводили животнымвнутрибрюшинно в виде 2-ного раствора. Определены дозы, характеризующиетоксичность препарата при однократном внутрибрюшинном применении. Они составляют соответственно для мышей МПД 5 340 мг/кг, ЯДА, 480 мг/кг; для крыс МПД180 мг/кг, ЯДА 250 мг/кг.Учитывая хорошую растворимость в воде,высокую противоопухолевую активность, проявленную при экспериментальном изу чении, малую токсичность, соединение мож но применять в медицине для лечениязлокачественных заболеваний.1790190 10 Продолжение табл, 3 одолжен Количество излеченных животных из числа взятых в группу.. "Торможение роста опухолей дано на 7-е и 17-е сутки посл прочерк (-) означает, что исследование не проводилось. еревивки опухо
СмотретьЗаявка
4867480/04, 08.08.1990
Ленинградский химико-фармацевтический институт, Всесоюзный онкологический научный центр АМН СССР
Стеценко А. И, Имсырова А. Ф, Яковлев К. И, Коновалова А. Л, Трещалин И. Д, Камалетдинов Н. С, Козлов А. М, Иванова Т. П, Бодягин Д. А, Переверзева Э. Р
МПК / Метки
МПК: A61K 31/295, C07F 15/00
Метки: 3-диметилксантинплатины, активность, дигидрат, противоопухолевую, проявляющий, хлорид, цис-хлордиаммин-1
Опубликовано: 27.04.1996
Код ссылки
<a href="https://patents.su/5-1790190-cis-khlordiammin-1-3-dimetilksantinplatiny-ii-khlorid-digidrat-proyavlyayushhijj-protivoopukholevuyu-aktivnost.html" target="_blank" rel="follow" title="База патентов СССР">Цис-хлордиаммин-1, 3-диметилксантинплатины (ii) хлорид дигидрат, проявляющий противоопухолевую активность</a>
Предыдущий патент: Способ получения 2, 5-диметокси-2-диметоксиметил-2, 5 дигидрофурана
Следующий патент: Способ получения поликапроамида
Случайный патент: Способ автоматического управления химическими реакциями