Способ получения высших первичных алкилмеркаптанов
Похожие патенты | МПК / Метки | Текст | Заявка | Код ссылки
Номер патента: 956469
Авторы: Вершинин, Держинский, Конюшкин, Коршунов, Курочкина, Мазаев, Мелехов, Прилежаева, Шишкова, Щапова
Текст
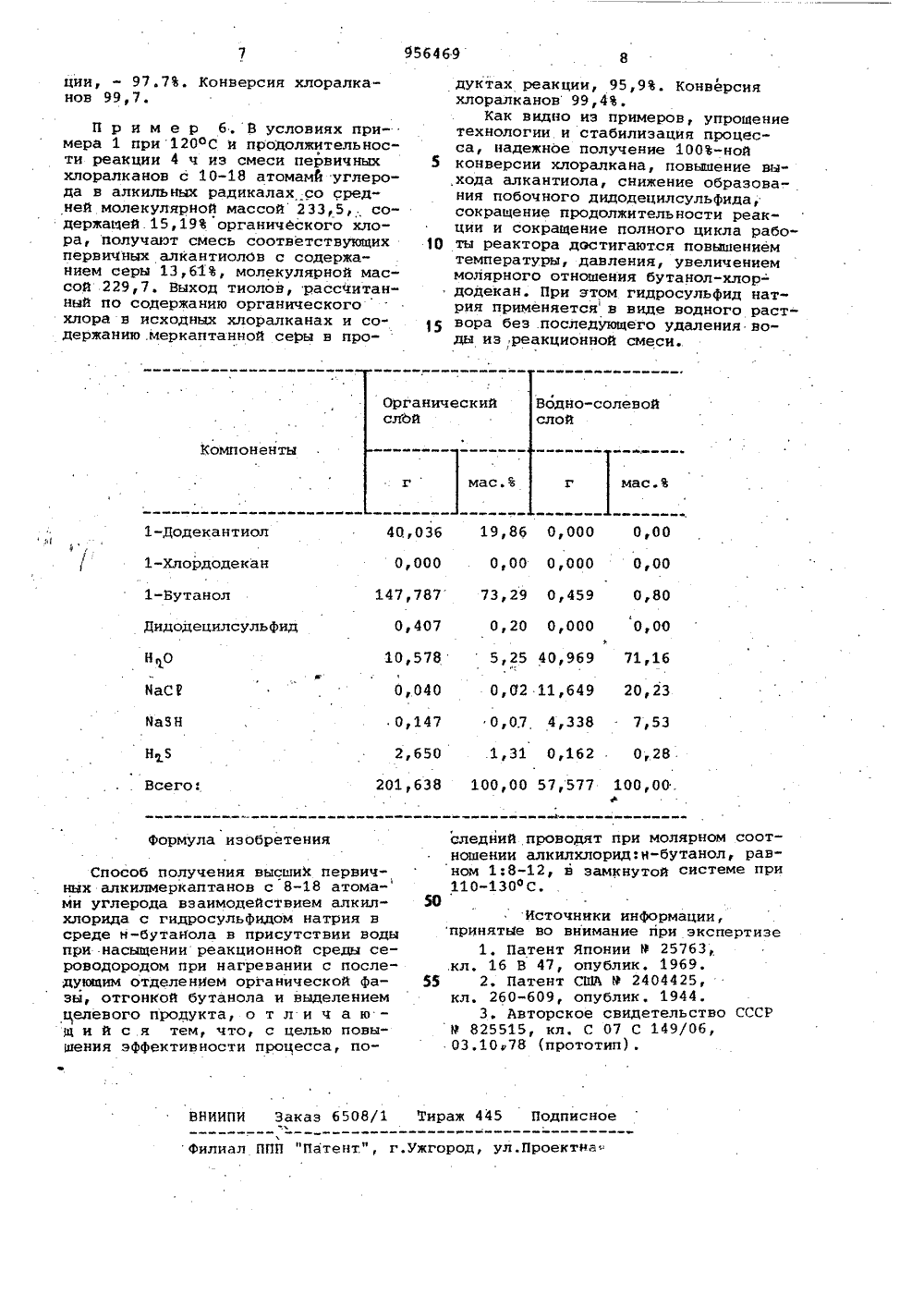
ОПИСАНИЕИЗОБРЕТЕНИЯК АВТОРСКОМУ СВИДЕТЕЛЬСТВУ Союз СоветскихСоциалистическихРеспублик иц 956469 г ="-.(22) Заявлено 06,03.81(21) 3255319/23-04 Р 1 М К з с присоединением заявки Мо С 07 С 149/06//С 08 К 5/37 Государственный комитет СССРо делам изобретений н открытий(23) Приоритет 53)УДК 547.269, .1.07 (088,8) Опубликовано 070982,Бюллетень МВ 33 Дата опубликования описания 07.09,82 Курочкина, )елехов, ЕПрей%П.В. Вершинин В.Е. Мазаев, М.А. Коршунов, С.А.Р.Н. Шишкова,. Н.В. Щапова, В.М.А.Р. Держинский, Л.Д. Конюшкин и(54) СПОСОБ ПОЛУЧЕНИЯ ВЫСШИХ. ПЕРВИАЛКИЛМЕРКАПТАНОВ рганическобутанола иодом 80 о есса Изобретение относится к способу получения высцжх первичных алкилмер-, каптанов с 8-18 атомами углерода, которые находят применение в качестве регуляторов молекулярного веса в производстве полимеров, в производстве пестицидов, флотоагентов и поверхностно-активных веществИзвестен способ получения высших первичных алкилмеркаптанов, например, взаимодействием соответствующих алкилгалогенидов с гидросульфидом натрия водном диметилформамиденагревании. Выход целевого прота 90-97 13 .Недостатком способа является ис пользование диметилформамида, гидролизующегося в условиях синтеза и плохо регенерирующегося из водных растворов.Известен способ получения высших первичных алкилмеркаптанов взаимодействием раствора соответствующих алкилгалогенидов в н-бутаноле в присутствии с кристаллическим гидросульфидом натрия с перемешиванием при 70-110 С и насыщении реакционной смеси сероводородом, при содержании воды в реакционной смеси 2,02 моль и выше в расчете на мольгидросульфида натрия с последующим добавле.нием воды, отделением о йфазы и отгонкой иэ неецелевого продукта с вых88,Продолжительность пр ц8 ч (21К недостаткам данного способа от"носится образование до 13 побочно.образующихся сульфидов и длительность процесса невысокая производи 10 тельность процесса.Наиболее близким к предлагаемомуявляется способ получения высших первичных алкилмеркаптанов с 8-18 атомами углерода, заключающийся во 15 взаимодействии алкилхлорида с насыщенным сероводородом водным раствором гидросульфида натрия, из которого предварительно отгоняют воду ввиде азеатропной смеси с н -бутанолом до остаточного содержания воды1-2 моль на моль гидросульфида натрия,при 70-110 С, атмосферном давлении и молярном соотношении алкилхлорид: и -бутанол: гидросульфид натрия, равном 1;3;1,1:1,3, и перемешивании в течение 4-5 ч с последующей обработкой реакционной смесиводным слоем иэ азеотропной смесидля растворения неорганических солей, Водную фазу, полученную после,отделения органической фазы от про 3Ф 95 б 4 б.9дуктов синтеза, обрабатывают минеральной кислотой с одновременной отгонкой сероводорода и водно-бутанольной смеси и рециркуляцией последнихв процесс на стадии насыщения и обработки реакционной смеси водой соответственно. Максимальный выход целевого продукта 94, конверсия хлоралкана до 98,9 33.К недостаткам данного способа относятся неполная конверсия и выход 10целевого продукта,необходимость .ограничения содержания воды в реакционной смеси для обеспечения приемОтемой глубины конверсии алкилхлоридаи снижения продолжительности синтеза, наличие твердого осадка гицросульфида натрия в исходной реакционной смеси и образование твердогоосадка хлористого натрия и не вступившего в реакцию гидросульфида натрия в продуктах реакции, увеличение цикла работ за счет времени,необходимого для отгонки водного азеотропа, необходимость дозированияводы для растворения солей в продуктах синтеза - что все в целом25снижает эффективность процесса,Целью изобретения является повышение эффективности процесса.Поставленная цель достигаетсятем, что получение высших первичных З 0алкилмеркаптанов с 8-18 атомами углерода заключается во взаимодействии алкилхлоридов с водным раствором гидросульфида натрия в среден-бутанола при насыщении реакционной смеси сероводородом в замкнутойсистеме, при 110-130 С, при молярномсоотношении алкилхлорид: н -бутанол,равном 1:8-12,.с последующим отделе-.нием органической Фазы, отгонкой бутанола и выделением целевого продукта.Выход 97,2-98,9, конверсия хлоралканов 99,3-100.Гидросульфид натрия применяют ввиде 22-27 водного раствора.Указанная цель достигается толькопри одновременном повышении температуры, давления и увеличении соотношения бутанол-хлоралкан, Изменениеодного или двух иэ этих трех параметров относительно условий, приведенных в прототипе, не дает положительного эффекта.С повышением давления в системеизменяются все основные закономернос" 55ти процесса, вследствие повышениярастворимости сероводорода в реакционной смеси и повышения растворимости гидросульфида натрия в органической Фазе. В случае синтеза 1"додекантиола 100-ная конверсия хлор-..додекана достигается при 110-115 фСпри малярном отношении бутанол:хлордодекан, равном 10:1, и давлении, создающемся при наГРевании 65 реакционной смеси, насыщенной серо-водородом при комнатной температуре (4,0 ати при 110 С, 4,5 ати при115 С). При этом выход 1-додекантиола достигает 98-99. Протекание реакции мало зависит от интенсивности перемешивания, Продолжительностьреакции снижается до 2-3 ч, а при130 С до 1,0-1,5 ч,В указанных условиях может бытьиспользован промышленный водныйраствор гидросульфида натрия безпредварительной отгонки воды, т.е.исключается необходимость в дози"ровании твердого кристаллогидратагидросульфида натрия или необходимость в азеотропной осушке реакцион-.ной смеси.Применение водного раствора гидросульфида натрия концентрации неболее 23 при молярном отношенииреагентов ЯСРИБ бутанол = 1:1,4:10позволяет получать продукты реакции, не содержащие твердого осадка ЙаС 2 и не вступившего в реакцию МИН. Опытным путем найденамаксимально допустимая концентрациясолей в нижнем водно-солевом слоепродуктов реакции 28 (для молярного отношения МаСВ:Ма 5 = 1:04) . Учитывая поступление воды вреакционнуюсмесь с возвратным бутанолом, промышленный гидросульфид натрия, который производится с концентрациейМа 5 Н 22-27, может применяться безпредварительного разбавления. Изцикла работы реактора исключаются,две операции: дозирование воды илинижнего слоя гетероазеотропаи операция перемешивания для обеспечениярастворения осадка солей.Отсутствие твердых осадков в исходной реакционной смеси и в продуктах реакции позволяет оформить реакционный узел по непрерывному способу.Продукты реакции разделяют надва слоя: на органический и водносолевой. Причем оба слоя неокрашены,граница раздела четкая, вспениваниепо границе раздела фаз полностьюотсутствует.Последнее объясняется,подавлением побочных процессов засчет повышения растворимости сероводорода в реакционной смеси.Из органического .слоя в условияхвакуумной ректификации отгоняют бутанол и используют его повторно. Изостатка прямой перегонкой выделяют1-додекантиол.Гарантированное достижение полнойконверсии хлоралкана позволяет отказаться от технологически сложной системы регенерации не вступившего вреакцию хлордодекана.При отсутствии рецикла хлордоде"кана, связанного с длительным нагреванием 1-додекантиола, и при ограничении температуры нагрева 1-додекан-тиола при его выделении (не ваде155 С) чистота получаемого 1-додекантиола зависит только от наличия примесей в исходном.хлордодекане. Обычная примесь в хлордодекане и, следовательно, в 1-додекантиоле - 1-додеканол,Основная масса сероводорода,требуемого для насыщения реакционной смеси в разработанном процессе,находится в замкнутом цикле, Сероводород, необходимый для превращения примеси сульфида натрия в гидросульфид натрия и для восполненияпотерь при рециркуляции сероводорода, получают обработкой соляной кислотой водно-солевого слоя, содержащего непрореагировавший гидросульфид натрия, Одновременно с отпаркойсероводорода из водно-солевого слоя,в котором содержится до 1 бутанола,происходит отгонка,водно-бутанольнойсмеси и возврат ее в процесс, чтообеспечивает полную регенерацию бутанола.Проводят лабораторныйсинтез 1-додекантиола в оптимальных условиях,позволяющих достигать максимальныйвыход целевого продукта, а такжебалансовый состав двухслойной системы.продуктов реакции.В условиях синтеза 1-додекантиола могут быть синтезированы с высоким выходом и практически 100-нойконверсией алкантиолы, содержащие8-18 атомов углерода в углеводородной цепи.Пример 1. В ампулу из не ржавеющей стали объемом 510 мл срубашкой для термостатированногообогрева, термопарой и манометромпомещают 67,262 г предварительно насыщенного сероводородом водногораствора гидросульфида натрия, содержащего 23,34 МаЗН 15,699 г;0,28 г-моль Ма 5 Н ). Сюда же добавляют40,956 г 10,2 г-моль) 100-ного 1 хлордодекана и 148,424 г2,00 г-моль)н-бутанола, содержащего 0,12 воды.Иолярное отношение хлордодекан:МаЭН: бутанол равно 1,0;1,4:10. Реакционную смесь насыщают,газообраэным сероводородом, ампулу гермети-.зируют, устанавливают на встряхивающую машину, обеспечивающую 150 качаний в минуту с амплитудой 35 мм,включают перемешивание и в течение10 мин нагревают до 115 С, перемешивание продолжают в течение 3 часов,В результате нагревания реакционнойсмеси давление в ампуле поднимается до 4,5 ати.По окончании реакции ампулу быстро охлаждают до комнатной температуры. Продукты реакции переносят вделительную воронку и разделяют надва слоя: органический и водйо-со%левойОба слоя анализируют на содержание 1 хлордодекана, 1-додекантиола, МаС и НаЯН потенциометрическими методами, Содержание воды ворганическом слое и бутанола в вод но-солевом слое определяют хроматографическим методом в соответствующих дистиллатах разгонок. Содержание дидодецилсульфида определяют по результатам анализа мер каптанной и сульфидной серы в кубо"вых продуктах после ректификацииорганического слоя. Ампулу промывают25 мл воды, промывание воды анали"зируют на содержание МаС 0 и МаЬН, 15 Полученные значения, 0,126 и0,014 г, соответственно относят кводно-солевому слою. Состав отдель.ных слоев приведен в таблице. Содержание сероводорода, приведенное 0 в таблице, рассчитано по значениямего растворимости в воде, бутанолеи 1-додекантиоле при комнатной температуре.Целевой 1-додекантиол концентрации 99,7 выделяют ректификациейорганического слоя. Выход 1-додекантиола 98,9, конверсия 1-хлордодекана 100.П р и м е р 2. В условиях примера 1 при 130 ОС и продолжительнос"ти реакции 1,5 ч из 1-хлордодекана.получен 1-додекантиол с выходом97,2. Конверсия 1-хлордодекана 100,П р и м е р 3. В условиях примера 1,из 1-хлороктана получают З 5 1-октантиол с выходом 99,1. Конверсия 1-хлороктана 100Выделенныйректификацией продукт имеет чистоту 99,8 хроматографически), содержание меркаптанной серы 21 у 88 Р ьЧО 40 1,4538, молекулчрную массу 145,9криоскопически в бензоле ).П р и м е р 4. В условиях примера 1 при 120 С и продолжительности реакции 4 часа из 1-хлороктадека на получают 1-октадекантиол с выходом 97,6. Конверсия 1-хлороктадека"на 99,3. Продукт после удалениярастворителя содержал 10,97 меркаптанной серы расчетная чистота ;О.продукта 98,0), п 1,4637, молекулярную массу 284,2 криоскопически в бензоле).П р и м е р 5. В условиях примера 1 из смеси первичных хлоралкановс 10-14 атомами углерода в алкильных радикалах, содержащей 16,82связанного хлора, 2,6 высших алканолов со средней молекулярной массой 204,2, получают смесь соответствующих первичных алкантиолов со 60 средним содержанием меркаптаннойсеры 15,14 молекулярной массой200,9. Выход тиолов, рассчитанный посодержанию органического хлора висходных хлоралканах и содержанию65меркаптанной серы в продуктах реак.1,31 0,162 О, 28 . 2,650201,638 100,00 57,577 100,00. Всего: формула изобретения ВНИИПИ Заказ 6508/1 Тираж 445 Подписноефилиал ППП "Патент.", г.ужгород, ул.Проектна ции, - 97.7. Конверсия хлоралканов 99,7. П р и м е р б. В условиях примера 1 при 1200 С и продолжительности реакции 4 ч из смеси первичных хлоралканов с 10-18 атомамй углерода в алкильных радикалах со средней молекулярной массой 233,5,. содержащей.15,19 органичбского хлора, получают смесь соответствующих первичных алкантиолов с содержанием серы 13,61, молекулярной мас" сой 229,7. Выход тиолов, рассчитанный по содержанию органическогохлора в исходных хлоралканах и содержанию .меркаптанной серы в проСпособ получения высшиМ первичных алкилмеркаптанов с 8-18 атома- ми углерода взаимодействием алкилхлорида с гидросульфидом натрия в среде н-бутанола в присутствии воды при насыщении реакционной среды сероводородом при нагревании с последующим отделением органической Фазы, отгонкой бутанола и выделением целевого продукта, о т л и ч а ю - щ и й с я тем, что, с целью повышения эффективности процесса, подуктах реакции, 95,9. Конверсияхлоралканов 99,4.Как видно из примеров, упрощениетехнологии и стабилизация процесса, надежное получение 100-ной5 конверсии хлоралкана, повышение выхода алкантиола, снижение образования побочного дидодецилсульФида,сокращение продолжительности реакции и сокращение полного цикла рабо 10 ты реактора достигаются повышениемтемпературы, давления, увеличениеммолярного отношения бутанол-хлор-додекан, При этом гидросульФид натрия применяется в виде водного раствора без последующего удаления воды из,реакционной смеси,следний проводят при молярном соотношении алкилхлорид:н-бутанол, равном 1:8-12, в замкнутой системе при 11 0-1300 С. Источники информациипринятые во внимание при экспертизе1, Патент Японии Р 25763,,кл. 16 В 47, опублик, 1969.2. Патент СШЛ 9 2404425,кл, 260-609, опублик, 19443. Авторское свидетельство СССРР 825515, кл. С 07 С 149/06,03.1078 (прототип).
СмотретьЗаявка
3255319, 06.03.1981
ПРЕДПРИЯТИЕ ПЯ В-8585
МАЗАЕВ ВЛАДИМИР ЕВГЕНЬЕВИЧ, КОРШУНОВ МИХАИЛ АЛЕКСЕЕВИЧ, КУРОЧКИНА СВЕТЛАНА АЛЕКСАНДРОВНА, ШИШКОВА РАИСА НИКОЛАЕВНА, ЩАПОВА НАТАЛИЯ ВИКТОРОВНА, МЕЛЕХОВ ВАЛЕНТИН МИХАЙЛОВИЧ, ПРИЛЕЖАЕВА ЕЛЕНА НИКОЛАЕВНА, ДЕРЖИНСКИЙ АРВИД РУДОЛЬФОВИЧ, КОНЮШКИН ЛЕОНИД ДМИТРИЕВИЧ, ВЕРШИНИН ПЕТР ВАСИЛЬЕВИЧ
МПК / Метки
МПК: C07C 321/04
Метки: алкилмеркаптанов, высших, первичных
Опубликовано: 07.09.1982
Код ссылки
<a href="https://patents.su/4-956469-sposob-polucheniya-vysshikh-pervichnykh-alkilmerkaptanov.html" target="_blank" rel="follow" title="База патентов СССР">Способ получения высших первичных алкилмеркаптанов</a>
Предыдущий патент: Способ очистки диоксидифенилсульфона
Следующий патент: Способ получения аммониевой соли этиленбисдитиокарбаминовой кислоты
Случайный патент: Быстроразъемное соединение труб