Способ получения модифицированной урокиназы
Похожие патенты | МПК / Метки | Текст | Заявка | Код ссылки
Текст
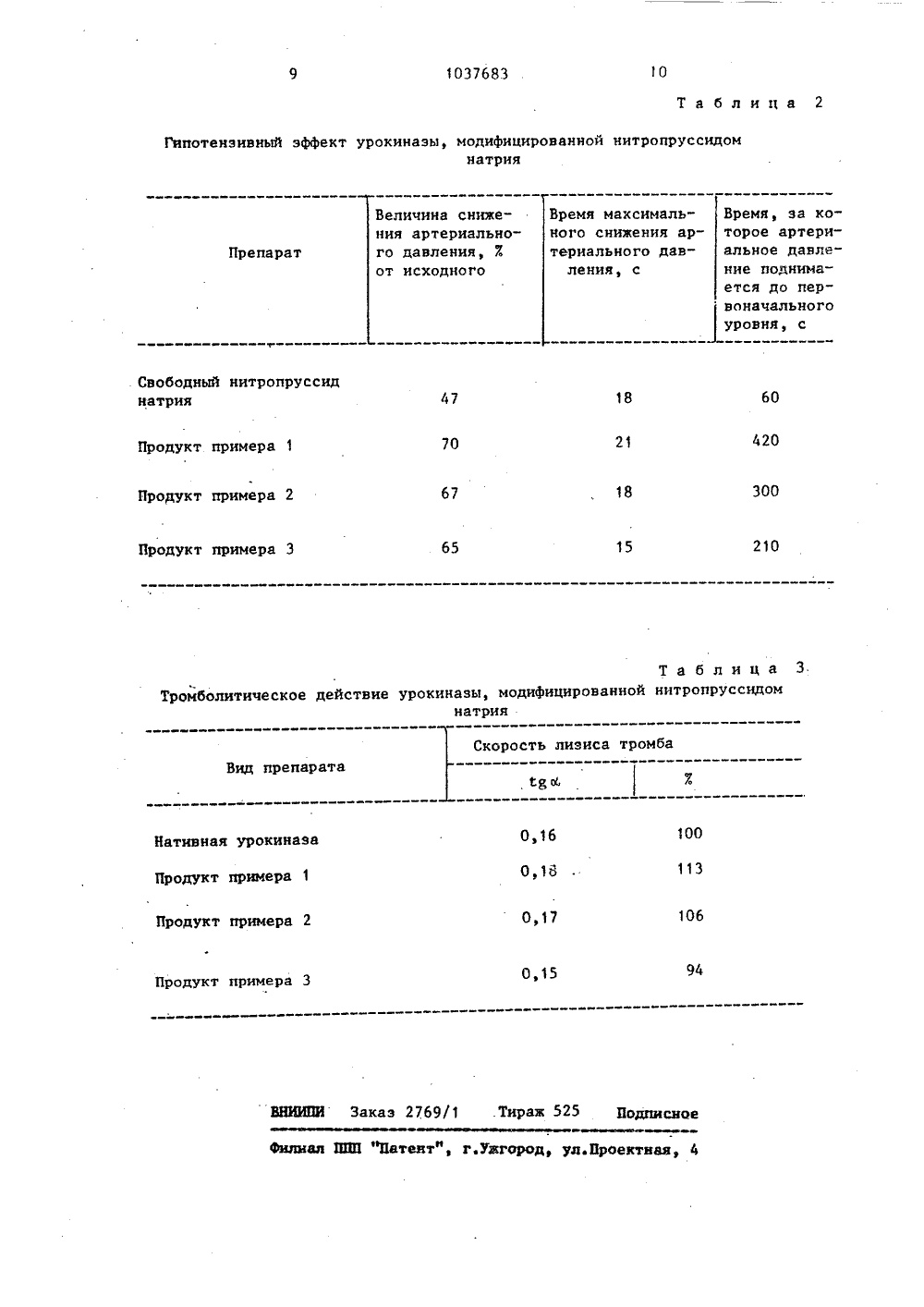
(51) С 12 Н 9/72; А 61 К 37/48 ТЕНИЯ ВТОРСНОМ ЕТЕЛЬСТВУ ГОСУДАРСТВЕННЫЙ КОМИТЕТ СССРПО ДЕЛАМ ИЗОБРЕТЕНИЙ И ОТКРЫТИИ ОПИСАНИЕ ИЗ(71) Всесоюзный кардиологическийнаучный центр АМН СССР н Научноисследовательский .институт Фармакологии АМН СССР.(56) 1, Т. К 1 Сао, К. На 1 йог.ТЪгошЬоз. Наеюозйаз, 1980, 43, 70.2. Авторское свидетельство СССРно заявке Р 2821712/23-04,кл, С 12 .Б 9/72, 1979.3. Авторское свидетельство СССР824053 кл 1, 01 1 т 33/86 1979.(54) (57) СПОСОБ ПОЛУЧЕНИЯ МОДИФИЦИРОВАННОЙ УРОКИНАЗЫ, о т л и ч аю щ и й с я тем, что, с целью обес"печения комплексной пролонгированной тромболитической и сосудорасширяющей активности целевого продук. та, урокиназу подвергают взаимодействию с нитропруссидом натрияпри рН 8,3-9,0.Изобретение относится к химикоФармацевтической промьппленности,а именно к синтезу биологическиактивных химических соединений, обладающих сосудорасширяющей и тромболитической активностью.Известен способ получения модиФицированной урокинаэы, связаннойс высокомолекулярными носителями,обладающей тромболитической активностью Я ,Способ заключается в том, чтоурокиназу связывают с помощью бифункционального реагента 4,4 -диизотиоциано,2 ."стильбен дисульфоната с эритроцйтарной массой человека.Такой способ получения производныхбелка довольно трудоемок, а образующийся продукт не растворим в воде, что затрудняет его медицинское 20использование.Более близким по достигаемомурезультату является способ голучения модифицированной урокиназы, который заключается в том, что урокивазу подвергают взаимодействию ссополимером акриламида и акриловойкислоты с молекулярным весом 10200 тыс. ед, и содержанием акриловой кислоты 1-207, предварительно 30обработанным карбодиимидом, причемпроцесс ведут при рН 8,0-8.3 2 .Получаемое производное обладает пролонгированной тромболитической активностью, растворимо в 35воде, является биосовместимым сживым организмом.Таким образом, известный способобеспечивает получение биологически активного вещества, обладающего 40лищь одним видом специфическогодействия на живой организм, что ог.раничивает сферу его возможногоиспользования,В связи с этим создание препаратов, обладающих одновременно несколькими видами биологическойактивности, весьма перспективно,поскольку за счет многосторонностидействия препарата снижается количество назначаемых больному лекарственных средств, из-за пролонгации действия компонентов препаратаповышается эффективность терапии11заболевания, уменьшается риск леНкарственной болезни,Целью изобретения является обеспечение комплексной биологической активности модиФицированной урокиназы, а именно - комплексной пролонгированной тромболитической и сосударасширяющей активности целевого продукта.Указанная цель достигается описываемым способом получения модифицированной урокиназы, который заключается в том, что урокиназу подвергают взаимодействию с нитронруссидом натрия при рН 8,3-9,0.Соединения, получаемые описываемым способом, представляют собой продукт связывания урокиназы с нитропруссидом натрия. Нитропруссид натрия обладает гипотензивным действием за счет дилятирующего воздействия на гладкую мускулатуру периферических кровеносных сосудов и снижения общего периферического сопротивления, Гипотензивное действие нитропруссида натрия при его введении в организм проявляется быстро, однако и быстро заканчивается при прекращении введения препарата.Урокиназа, являясь активатором плазминогена в организме, обладает тромболитическими свойствами, в связи с чем ее применяют при лечении заболеваний, сопровождающихся повышением внутрисосудистой коагуляции.При тромбозах и особенно при эмболиях довольно часто наблюдаются сосудистые спазмы. Ликвидация таких нарушений, очевидно, будет более эффективной не только при использовании тромболитических, но и сосудорасширяющих средств, Особенностью действия нитропруссида натрия является его способность влиять на тонус артериол и вен.Способ осуществляется следующим образом.К урокиназе в 0,001 - 0,3 М растворе Фосфатного буфера добавляют нитропруссид натрия, реакцию проводят при температуре от 0 до 25 С в слабощелочной среде в течение 0,3-5,0 ч. Затем полученное производное подвергают очистке диалиэом в течение 16 ч против дистиллированной воды.Взаимодействие урокиназы с нитропруссидом натрия происходит по+ОН С.щ Ю схеме циангидринного синтеза, когда карбонильная компонента белка связыВместе с тем связывание нитропрусси" да с урокиназой проходит и через взаимодействие трехвалентного железа с сульфгидрильными группами белка;Е-ВН+ Ге (СИ) ИО 1 Е-Ге (СМ)4 МО ++. НСЯ Именно таким способом. происходит растворение нитропруссида натрия в . крови и тканях, когда трехвалент-. ное железо из молекулы нитропруссида натрия взаимодействует с сульфгидрильными группами эритроцитов.Полученный продукт представляет собой урокиназу, модифицированную нитропруесидом натрия. При этом нитропруссид натрия оказывается переведенным в состояние, когда он постепенно "сходит" с белковой глобулы, проявляя свое пролонгированное гипотензивное действие, Фермент после модификации сохраняет 85-907 исходной каталитической активности (в качестве субстратаприменяют метиловый эфир.ацетилглициллизина),. но термостабкяъности весьма стоек и не уступает нативному белку, ингибируется алазмацитратом заметно меньше, чем нативный препарат. Про-. дукт сохраняет свою пролонгирован- . ную биологическую активйость при хранении в холодильнике .(4-5 С) в растворенном виде в течение месяца. ПримерВ 4 мл 0,1 м фосфатногобуфера рН 8,8 растворяют 25 ОООО 10 урокиназы ( " 80 мг сухого вещества, 10 И), затем вносят в раствор 50 мг нитропруссида натрия (2 10И) и смесь инкубируют прв 5 С в течение 3 ч.:Еаспе этого препарат подвергают очистке диализеи в течение ночи против дйстиплшреванной воды. Концентрация свявается с циановой компонентой нит-,ропруссида натрия: С=И5 эанного с Ферментом нитропруссида510М. Фермент сохраняет 853,.; своей эстеразной активности (АСЬ Ие),не уступает по термостабильности нативному белку, слабее чем.он26 ингибируется плазма цитратом. Содержание белка в препарате б 5 Ж.Продукт представляет. собой бурокоричневый порошок, легко растворимый в воде.и спирте (до 40 мг/мл)Ж , П р и м .е р 2. Процесс.проводят так же, как и в примере 1, заисключением того, что реакцию мо. дификации урокиназы нитропруссидомнатрия осуществляют в,0,001 И фосщ Фатом буфера, рН.9,0 при 25 С в те"чение 5; Остаточная каталитическая.активность фермента 872. При этомконцентрация связанного с белкомнитропруссида натрия 1. 10 ф М.Свойства урокиназы близки тем, что .приведены в примере 1,Содержание белка в препарате74 Х. П р и м е р 3. Процесс лрово- .40дят также, как и в .примере 1, эаисключением того, что,реакцию моди фикации урокиназы нитропруссидомнатрия ведут в 0,3 М растворе фос-.45Фатного буфера.рН 8,3 при ОС .втечение 0,1 ч. Остаточная каталитическая активность фермента 90 Х.При этом с ферментом связывается7 ф 10 И нитропруссида натрия, а5Эсвойства урокиназы близки тем .котоф рые указаны в нримере 1.Содержание белка в.препарате 8 ОХ,При этом модификацйя урокиназынитропруссидам натрия не вызывает 55сильного изменения свойств фермента, Так,реакция каталитическогогидролиза урокиназой синтетичес-.ого субстрата меткпового эфираацеткпглициллизииа осуществляетсяпо схеме активации хода реакциисубстратом (схема 1). Продукты примеров 1-3 также осуществляют этуреакцию по указанной схеме. КЭ Хс(йЬ 15 Еб Е+РИй сЕЬ рРсхема 1 10 Кинетические параметры этой реакции для препаратов нативной и модифицированной урокиназы приведены в табл. 1 (рН 8,3; 25 С; 0,1 М КСВ) . 1 этап опыта заключался во внутривенном введении нативного нитропруесида натрия в дозе 30 мкг/кг веса, животного. Прекарат вводили болюсом. Следили за максимальной величиной снижения среднего артериального давления и за временем его, возвращения к исходным цифрам. На П этапе опыта вводили нитро пруссид натрия, иммобилизованный на урокиназе, Оценивали те же парамет-, ры. Производные урокиназы, полученные в примерах 1-3, содержат различное количество нитропруссида нат рия, связанного с ферментом. Это объясняется важной ролью величинь 1 рН инкубационной смеси, когда реакционноспособные группы, важные для реакции связывания, должны быть ионизованы, а при этом сама реакция обратима. Оптимальным значением является рН 8,8. За счет связывания с глобулой белка выход в кровоток активной Формы иитропруссида натрия ЗО замедляется, в результате чего его сосудорасщиряющее действие приобретает пролонгированный характер.Для определения гипотензивиого эффекта иитропруссида натрия, связанного с урокиназой. был проведен эксперимент на крысах линии "Вистар". Юркоэ осуществляли с помощью тиопеитала натрия. Затем выделяли. сонную артерию и яремную вену, в. 4 Г которые вводили полиэтиленовые катетеры. Непрерывно регистрировали артериальное давление до введения препарата в момент и после введения. 4 Получены следующие результаты:введение нативного препарата вызывало снижение среднего АД на 40507. по отношению к исходному. Макси"мум снижения наблюдался через 1124 с после введения болюса. Возвращение АЦ к исходному уровню происходило в среднем через 1 мин.Введение иммобилизованного препарата вызывало снижение среднегоАД на 65-702 от исходного через 1521 с от начала введения. Вслед заэтим наблюдалось постепенное повышение АД и через 3,5-7 мин оно возвращалось к исходному уровню,Таким образом, нитропруссид натрия, связанный с урокиназой, в сопоставимой дозе при введении болюсомдействует в 3,5-. 7 раз дольше (длительнее), чем препарат нитропруссида натрия в свободном виде, о чемсвидетельствуют приведенные втабл. 2 результаты.Эксперименты по лизису тромбовпрепаратами урокиназы, модифицированной нитропруссидом натрия, были проведены в соответствии с известнойметодикой 131 с добавлением в раствор буфера человеческого плазминоге-,на (0,4 мг/мл). Препараты нативнойи модифицированной урокиназы быливзяты для тромболизиса в соотношении, обеспечивающем их одинаковуюэкстреразную активность по низкомолекулярному субстрату метиловомуэфиру ацетилглициллизина. Результаты экспериментов приведены втабл. 3, где с 0 Ь представляет собой отношение прироста оптическойплотности раствора (в результатедеструкции при тромболизисе нерастворимого фибринового сгустка и перехода его Фрагментов в раствор)к величине промежутка времени, эакоторый оно произошло и являетсяпараметром, характеризующим скоростьтромболизиса.Представленные в таблице результаты наглядно показывают, что поэффективности тромболизиса препараты модифицированной нитропруссидомнатрия урокиназы не уступают препаратам нативного фермента, являющегося высокоактивным тромболитиком. Пониженная ингибируемость(приблизительно в 3-5 раз) плазмацитратом препаратов модифицированной урокиназы го сравнению с натив1037683 ТаблицаКз,И Препарат Нативная урокиназаПродукт примера 1Продукт примера 2Продукт примера 3 2,14 х 10 5,7 х 10 4,3 х 10 3,2 х 10 5,5 х 10 9,1 х 107,0 х 10 6,7 х 10 42,72 28,47 36,81 38,93 1,82 1,88 ным белком обеспечивает более длительный период тромболитического действия этого препарата в организме.Таким образом, ковалентное при соединение нитропруссида натрия к урокиназе позволяет получить новый препарат, обладающий сосудорасширяющим и тромболитическим дейст,вием, При этом замедление перехо да фрагментов молекул нитропруссида натрия с глобулы урокиназы в раствор обуславливает пролонгированный характер действия этого вазодиллятатора, а модификация урокиназы та1 ким низкомолекулярным лигандом как нитропруссид натрия не меняет существенно кинетические свойства Фермента, понижает его ингибируемость компонентами крови, за счет чего 20 возрастает время активного функцио. нироваиия тромболитика в организме. Таким образом, полученный препарат представляет собой новое средство комбинированного воздействия на 25 заболевание, причем сосудорасширяющие и тромболитические свойства его компонентов оказываются у негоне адцнтивными частями, а усиливаютдруг друга, придавая характер пролонгированного действия получаемомупроизводному. Получение терапевтических средств расширенного спектра действия несомненно весьма актуально, поскольку ведет не только к развитию новых методов терапии, вооружает врачей высокоэффективными лекарственными средствами, но и облегчает сам курс лечения, является весьма удобным и для медицинской практики, сокращая число инъекций. больному. Простота и легкость синтеза модифицированной нитропруссидсм натрия урокиназы позволяет надеяться на возможность быстрого получения этого препарата комбинированного действия. Появление такого лекарственного средства в арсенале врача расширит возможности борьбы с заболеванием и позволит перейти от струйных методов введения препарата к инъекционным.1037683 Таблица 2 Гипотензивный зффект урокиназы, модифицированной нитропруссидомнатрия Препарат Свободный нитропруссиднатрия 47 60 420 21 70 Продукт примера 1 Продукт примера 2 300 Продукт примера 3 210 Таблица 3Тромболитическое действие урокиназы, модифицированной нитропруссидомнатрия Скорость лизиса тромба Вид препарата 100 0,16 Нативная урокиназаПродукт примера 1 113 106 0,17 Продукт примера 2 94 0,15 Продукт примера 3 ВНИИПО Заказ 2769/1 .Тираж 525 Подписное Филиал ППП патент", г.Ужгород, ул.Проектная, 4 Величина снижения артериального давления, Хот исходного Время максимального снижения артериального давления, с Время, за которое артериальное давгение поднимается до первоначального уровня, с
СмотретьЗаявка
3252672, 03.03.1981
ВСЕСОЮЗНЫЙ КАРДИОЛОГИЧЕСКИЙ НАУЧНЫЙ ЦЕНТР АМН СССР, НАУЧНО-ИССЛЕДОВАТЕЛЬСКИЙ ИНСТИТУТ ФАРМАКОЛОГИИ АМН СССР
МАКСИМЕНКО А. В, КУХАРЧУК В. В, ТОРЧИЛИН В. П, МЕДВЕДЕВ О. С, ЛЕЩИНСКИЙ П. М, АРАБИДЗЕ Г. Г, СМИРНОВ В. Н
МПК / Метки
МПК: A61K 38/49, C12N 9/72, C12N 9/96
Метки: модифицированной, урокиназы
Опубликовано: 15.04.1985
Код ссылки
<a href="https://patents.su/6-1037683-sposob-polucheniya-modificirovannojj-urokinazy.html" target="_blank" rel="follow" title="База патентов СССР">Способ получения модифицированной урокиназы</a>
Предыдущий патент: Гербицидный состав
Следующий патент: Мембранный компрессор
Случайный патент: Устройство для извлечения шпал из пути при бетонном основании