Способ количественного определения содержания маннита в растворах
Похожие патенты | МПК / Метки | Текст | Заявка | Код ссылки
Текст
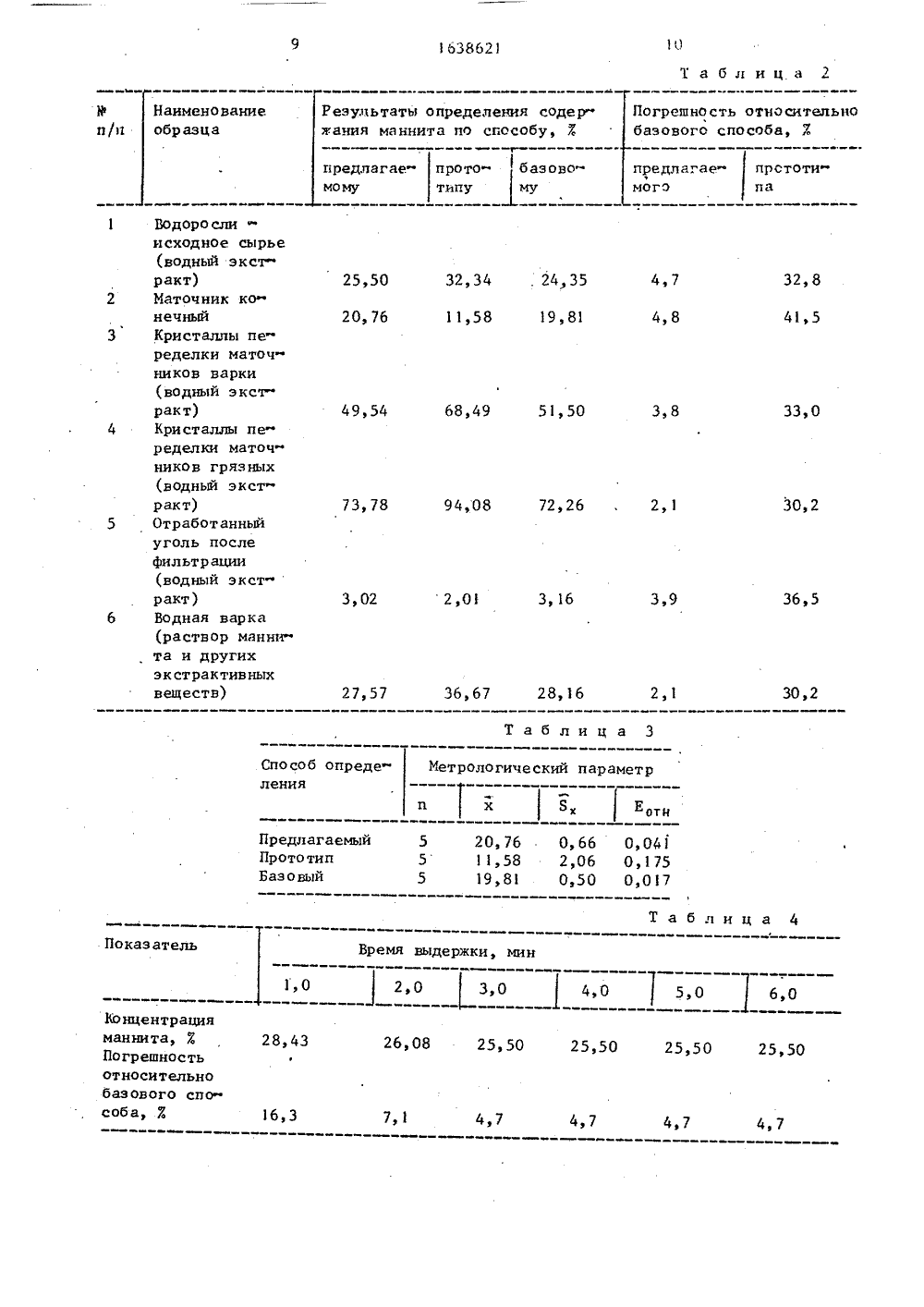
СОЮЗ СОВЕТСНИКСОЦИАЛИСТИЧЕСНИХРЕСПУБЛИН цо 163862) С 01 И 33/ ПИСАНИЕ ИЗОБРЕТЕНИ аствора(ф ГОСУДАРСТВЕННЫЙ КОМИТЕТпо изОБРетениям и ОтнРцтияцПРИ ГЙНТ СССР К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ(54) СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ МАННИТА В РАСТВОРАХ(57) Изобретение относится к рыбнойпромышленности и может быть использовано для контроля за содержаниемманнита в производственных р х1 Изобретение относится к рыбнойпромьппленности и может быть использовано для контроля за содержаниемманнита в производственных растворахпри его извлечении из морских водорослей,Целью изобретения является повы-.шение точности,Для осуществления предлагаемогоспособа определенный объем производстненного раствора маннита вводят вопределенный объем заранее приготовленной реакционной смеси, содержащейферрицианид и ферроцианид калия,Смесь выдерживают в течение заданного времени,. регистрируют потенциал при его извлечении из морских водорослей. Целью изобретения являетсяповышение точности Образец производственного раствора маннита вводятв определенный объем реакционнойсмеси, содержащей феррицианид и ферроцианид калия в растворе щелочи,Смесь выдерживают в течение 3-5 мин,регистрируют потенциал реакционнойсмеси. Затем вводят в реакционнуюсмесь в качестве катализатора ионымеди, вновь выдерживают при постоянном перемешивании в течение 1020 мнн, При этом за счет. реакции окисления маннита изменяется потенциалокислительновосстановительной системы Ре /Ре , По изменению потенз+ г+циала реакционной смеси рассчитываютконцентрацию маннита в исследуемомрастворе, 11 табл,реакционнои смеси и затем вводят в нее в качестве катализатора ионы меди вновь выдерживают заданное время и повторно регистрируют потенциал. По изменению потенциала реакционной смеси рассчитывают содержание маннита в анализируемом растворе.Для предотвращения влияния при месей, содержащихся в производственных растворах, таких как гликоген, крахмал, липиды, белки, нуклеиновые кислоты, альгиновые кислоты, хлорофилл, Э-каротин и:т,п на результаты определения отобранную пробу производственного раствора смешивают с реакпионной смесью и выдерживают в63862 ) течение 3-5 мин, За этот промежутоквремени примеси успевают окислитьсяи не мешают в дальнейшем определениюманнита, При этом соотношение маниита и окислителя должно находитьсяв пределах 1:7 " 1;70 (моль/моль).Реакционная смесь представляет собойсмесь Феррицианида и Ферроцианида калия в соотношении 80:1 - 120:1 (моль/10/моль), растворенную в щелочи концентрацией от 0,1 до 2 М, Затем вреакционную смесь в качестве катализатора вводят ионы двухвалентной медив концентрации 5:10 -1 О моль/л 15Вновь выдерживают раствор при постоянном перемешивании 10 20 мин, При этомза счет реакции окисления маннита изменяется потенциал окислительно-вос"становительной системы Рез /Ре, По 20изменению потенциала редокс системырассчитывают концентрацию маннита висследуемом растворе,П р и м е р:1, Для определениякалибровочной зависимости между изме 25нением показания прибора (ДЕ) (иономера) и логарифмом концентрации маннита в растворе (1 д С ман) готовятшесть растворов маннита со следующи,ми концентрациями: 1 г/л (5,5 10 моль/30(27,410 моль/л) Затем готовят щелочной раствор солей Феррицианида калия (ОХ-форма) и Ферроцианида калия(ген-форма) с соотношением С :С=100:1 (в качестве растворителя используют ИаОН концентрацией 1 моль/л).4040 мл приготовленного таким образомраствора помещают в стеклянный стаканчик и погружают в раствор платиновый и хлорсеребряный электроды,подключенные к иономеру, Затем отби 45рают 1 мп приготовленного раствораманнита концентрацией 1 г/л и вводятего в реакционную смесь, Выдерживаютраствор при постоянном перемешиванииВ течение 5 мин и Фиксируют потенфф 50циал смеси, равный 379+1 мВ (Е).После этого вводят в реакционный стаканчик 1 мл заранее приготовленногораствора нитрата меди с концентрацией 42.10 моль/л, снова выдерживают смесь в течение 10 мин, послечего Фиксируют потенциал раствора,Е.= 314+1 мВ, Затем освобождаютреакционный стаканчик от прореаги ровавшей смеси и промывают его дистиллированной водой, Повторяютэксперимент, при этом получаютЕ = 3793: мВ и Е = 313+ мВ, Рассчитывают величину Ь.Е = Е - Е 2 длядвух параллельных измерений, которые равны соответственно 65+1 мВ и.66+1 мВ,Аналогичные опыты проводят срастворами маннита других приготовленных концентраций Полученныерезультаты представлены в табл,.1,Методом наименьших квадратов рассчитывают коэффициенты уравнения Сц= а.ехр ЛЕ +Ь, величина коэффи циентов а и Ь приведена в табл,; кроме того, в.табл,1 приведены следующие параметры: А = (Св С) абсолютная ошибка определения, равная разности концентрации маннита, определенной по предлагаемому способу (С), и истиннсй, приготовлен ной из навески (С); О - относительСр- Сная ошибка ц = ---- 1007. г -Со коэффициент кореляцииТаким образом, концентрацию маннита по предлагаемому способу можно рассчитать по уравнениюС = 60,1 ехрДЕ + 63,32Используя полученную калибровоч,ную зависимость, определяют содер жание маннита в образцах производственных растворов, отобранных на различных стадиях процесса производ ства товарного маннита на Архангельском водорослевом комбинате,Для определения содержания маннита в водорослях (исходном сырье) оч бирают навеску анализируемой пробы (56,1611 г).и проводят экстракцию дистиллированной водой (Ч = 20 мл). Разбавляют полученный экстракт дис тиллированной водой в 125 раз1 мп разбавленного экстракта вводят в 40 мл реакционной смеси, приготов ленной как описано вышее, Выдерживают раствор в течение 5 мин и фиксируют значение Е379 шВ. Добавляют 1 мл раствора нитрата меди, выдерживают смесь 10 ьин и фиксируют величину Е = 292 шВ. Изменение потенциа ла ДЕ составляет:1ДЕ =Е Е =87 шВ.63862 П р и м е р 4. Определение маииита проводят так, как описано в приме" ре 1, но при этом варьируют концентрацию щелочи,5Полученные результаты, представлены в табл, 6 С ан= 276,27 г/л,276 27 10 : - -ф- --- 1 ООХ = 25,507мак 54,1611 20 20 Из табл,2 следует, что погрешность определения предлагаемого способа меньше погрешности прототипа в 8-10 разДля образца М 2 проведена метроло гическая оценка всех трех способов, полученные результаты представлены в табл: 3 П р и м е р 2, Определение содер жания маннита проводят так, как описано в примере 1, но при этом варьируют время выдержки раствора до введения в реакционную смесь нитрата меди,Полученные результаты представлены в табл,:4 Концентрация маннита, определеннаябазовым способом, составляет 24,35 ,по прототипу - 32,347. ( 8 = 32, 47.). щИз сравнения полученных результатоввидно, что оптимальное время выдержкиреакционной смеси должно быть не менее 3 мин,П р и м е р 3, Определеннф. макнита проводят так, как описано в примере 1, но при этом варьируют добавку2+Полученные результаты представлены в табл,:5 50 По уст ановл ен ной з ави симо сти С н = й(ЬЕ) рассчитывают с учетом предварительного разведения концентрацию маннита в экстракте: а содержание маннита в образце составляет: Анапогично определяют содержаниеманнита в других образцах, Также вэтих.же образцах определяют содержание маннита по прототипу, и по способу, принятому за базовый,Полученные результаты сведены втабл,: 2,Концентрация маннита, определенная базовым способом, составляет24,35 Х, по прототипу - 32,347,( 3 = 32,4 Х). Из сравнения полученныхрезультатов видно, что допустимыепределы концентрации ионов Сизиф врастворе 5 10 "-10 фМ, наиболее пред-Фпочтительна концентрация 10 М,Концентрация маннита, определенная базовым спо собом, сост авля ет24,35 Х, по прототипу - 32,34 Х(о = 32,47). Таким образом, концентрация щелочи должна находиться впределах 0,1-2:МП р и м е р :5. Определение маннита проводят так, как описано впримере 1, но при этом используютгидроксиды различных металлов одинаковой концентрации.Полученные результаты представлены в табл,.7По полученным результатам можносделать вывод, что вид щелочи неоказывает на определение маннита икакого влиянияП р и м е р 6Определение маннита проводят так, как описано в примере 1, но при этом меняют концентрацию окислителя при постоянном соот"ношении С ( . С(1 = 100:1,Полученные результаты приведены втабло . 8 аКонцентрация маннита, определенная базовым способом, составляет24,35 Х по прототипу 32,34 Х(3 = 32,47). Таким образом, проведенный эксперимент показывает, что впределах концентраций окислителя0,01-0,1 моль/л концентрация маннитапрактически не меняетсяП р и м е р 7, Определение маннита проводят так, как описано впримере 1, но при этом меняют соотношенне С/С(1 при постоянной концентрации окислителя С= 0,01 моль//л,Полученные результаты приведеныв табл, 9Концентрация маннита, определенная базовым способом, составляет24,357., по прототипу32,347.1 = 32,4 Х). Таким образом, соотношение Со( С должно находитьсяв пределах 80:1 - 120:1,П р и м е р 8, Определение маннита проводят так, как описано впримере 1, но при этом меняют времявыдержки раствора после введения каталитической добавки,Та блица Истинная Экспериментальная концентрация маннита, С де, АмВ моль/л%(ф32,4%), Таким образом, время выдаржки должно быть в пределах 1020 мин,П р и и е р ;9, Определение мании "та проводят так, как описано в примере 1 но при этом меняют мольное соьФотношение маннита и окислителя (Ре ).Результаты приведены в табл, 11,Концентрация маннита,определеннаябазовым способом,составляет 24,35%,по прототипу - 32,34% ( 8 = 32,4%).Таким образом, опыты показывают чтосоотношение (мольное) маннит/Редолжно находиться в пределах 1 71 Ф 70 ь 20 Формула изобретения Способ количественного определе-ния содержания маннита в растворах, 25преимущественно в производственныхсредах, включающий окисление маннитав водно щелочной среде в присутствиикатапитической добавки ионов метапла,установление расхода окислителя с последующим определением содержанияманнита, о т л и ч а ю щ и й с ятем, что, с целью повышения точностиопределения, окисление маннита проводят раствором феррицианида и ферроцианида калия 80:1 ь 120:1 моль/мольпри соотношении маннита и окислителя1: 7 1:,70 моль/моль, концентрациищелочи 0,1-2 моль/л при использовании в качестве каталитическай добавки ионов и двухвалентной меди(5 10;,1 О 4 моль/л) ь причем расходокислителя устанавливают по изменению потенциала редокс системыРе /Ре , при этом перед введением,ионов меди анализируемую пробу сокислителем выдерживают 3-5 мин, астадию окисления маннита в присутствии ионов меди проводят 1 9.20 мин,1прототипа предлагаетмого предпагаемому 32,8 32,34 , 24 35 11,58 19,81 4,7 25,50 20,76 41,5 4,8 33,0 3,8 68,49 51,50 49,54 30,2 2,1 94,08 72,26 73,78 36,5 3,9 3, 162,01 3,02 36, 67 28,16 2,1 30,2 27,57 Таблиц а 3 Метрологический параметрт х8 х Ео Способ определения О, бб 0,041 2,06 0,175 0,50 0017 ПредлагаемыйПрототипБазовый 20, 7611,5819,81 5 5 Таблица 4 Показатель Время выдержки, мин 2,0 3,0 4,0 5,0 6,0 1,0 Концентрацияманнита, 7Погрешность относительнобазового способа, 7 28,43 26,08 25,50 25,50 25,50 25,50 4,7 16,3 7 х 1 4,7 4,7 Водоро слиисходное сырье (водный экстракт)Маточник конечныйКристаллы переделки маточников варки (водный экстракт)Кристаллы пе ределки маточников грязных (водный экстракт)Отработанный уголь после фильтрации(водный экст ракт)Водная варка (раствор маннита и других экстрактивных веществ) Результаты определения содержания маннита по сгособу, 7 Погрешность относительнобазового способа, 7.,Показатель г+Концентрация ионов Сц в ячейке, моль/л 50-4. О 10 20,1 25,5 25,5 26,4 28,17,4 4,7 4,7 8,4 15,4 Таблиц а 6 Концентрация НаОН, м0 1 1 1 5 2 3 Показатель 0,05 5 21,121,825,5 25,5 29,9 30,0 32,5 3,3 10,5 4,7 4,7 6,4 23,2 33,5 Таблица 7 Показатель Щелоч ь ЬхОН НаОН КОН 255 25 е 5 2515 4,7 4,7 4,7 Т аблица 8 Концентрация ОХ, моль/л Показатель 27 еО 26 у 225 э 2 25 э 5 25 ф 7 25 ф 9 26 е 2 10,9 6,4 7,6 4,7 4,7 7,6 Таблица 9 Соотношение Са /С щ,Показатель 75:1 25,5 27,1 25,5 23,4,7 4,7 5,1 СманПогрешность относительно базавого способа, Ж Сма, г/лПогреюность относительно базавого способа, 7 Смаке ЖПогрешностьотноси тельнобазового способа, У. СманПогрешность относительно базового способа, Х Сманф %Погрешностьотносительнобазового способа, Е 0,01 0,015 0,02 О, О,5,Показ атель 25,4 25 вб 255 26 э 28 ф 5 21,9 25,5 7,2 17,0 10,5,1 4,7 4,7 4 фЗ Составитель: И ПинуевТехред Л,Олийнык Корректор О. Ципле Редактор; А,Лвкнина Заказ 924 Тираж 417 Подпи сно еВНИИПИ Государственного комитета по изобретениям и открытиям при ГКНТ СССР 113035, Москва, Ж, Раушская иаб., д. 4/5 Производственно-издательский комбинат "Патент", г.ужгород, ул. Гагарина,101 Саари) Погрешность относительно базового способа,Концентрацияманнита, 311 огрешность относительно базовогоспособа, Мж ша ее ее шеей ш ш1/5/7 1/10 1/50 1/70 1/80 1/ 00
СмотретьЗаявка
4641039, 25.01.1989
АРХАНГЕЛЬСКИЙ ЛЕСОТЕХНИЧЕСКИЙ ИНСТИТУТ ИМ. В. В. КУЙБЫШЕВА
БОГОЛИЦЫН КОНСТАНТИН ГРИГОРЬЕВИЧ, БОГДАНОВ МИХАИЛ ВЛАДИСЛАВОВИЧ, АЙЗЕНШТАДТ АРКАДИЙ МИХАЙЛОВИЧ, ГЕЛЬФАНД ЕФИМ ДМИТРИЕВИЧ, КРУНЧАК ВЛАДИМИР ГЕОРГИЕВИЧ, РОДИЧЕВ АЛЕКСАНДР ГРИГОРЬЕВИЧ, ЛЬВОВА ТАТЬЯНА ИГОРЕВНА, СУСАРЕВА ОЛЬГА МИХАЙЛОВНА, ШАРКО КСЕНИЯ ДМИТРИЕВНА
МПК / Метки
МПК: G01N 33/02
Метки: количественного, маннита, растворах, содержания
Опубликовано: 30.03.1991
Код ссылки
<a href="https://patents.su/7-1638621-sposob-kolichestvennogo-opredeleniya-soderzhaniya-mannita-v-rastvorakh.html" target="_blank" rel="follow" title="База патентов СССР">Способ количественного определения содержания маннита в растворах</a>
Предыдущий патент: Способ определения силикатного модуля жидкого стекла
Следующий патент: Кондуктометрический агрегатограф
Случайный патент: 234376