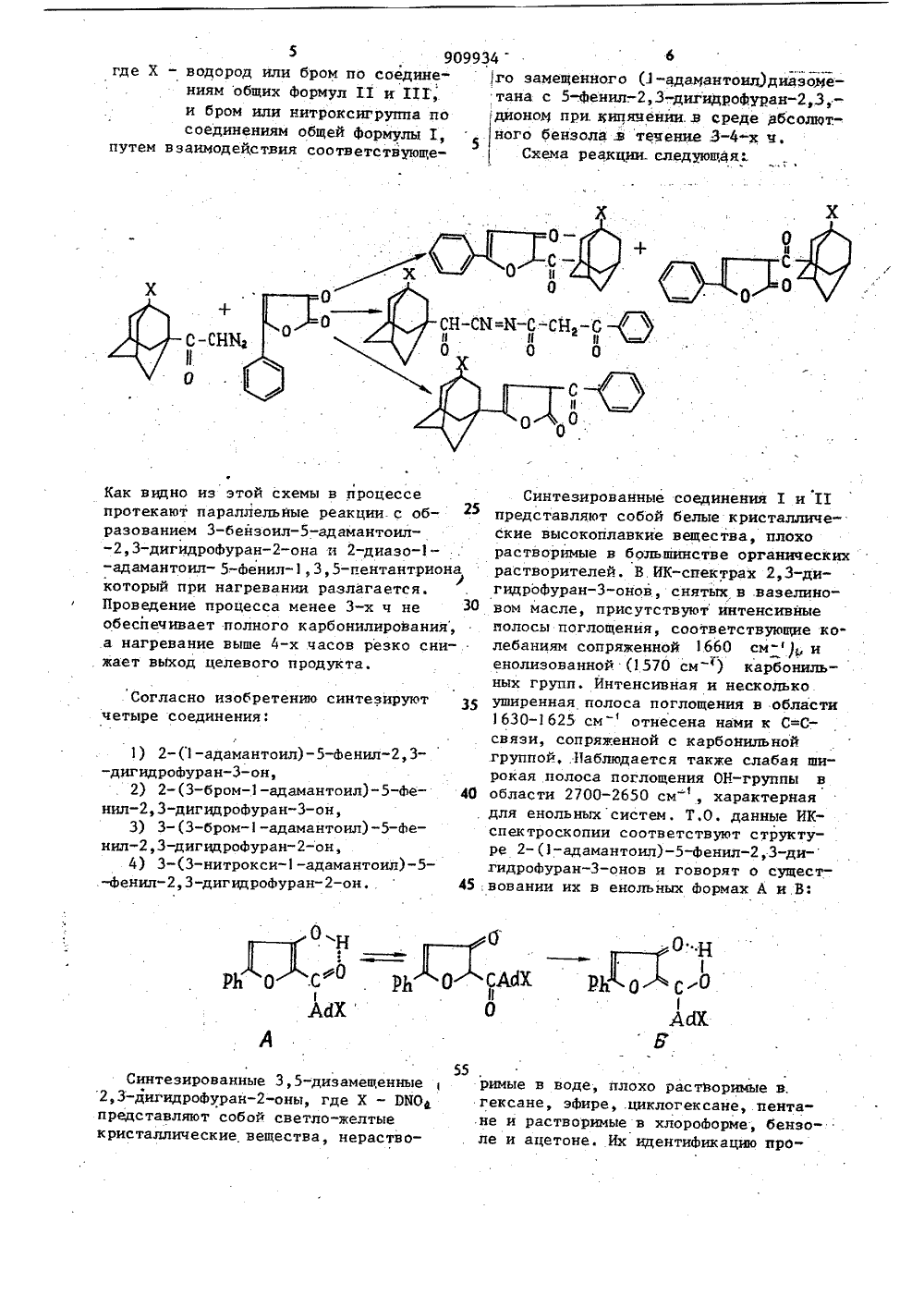
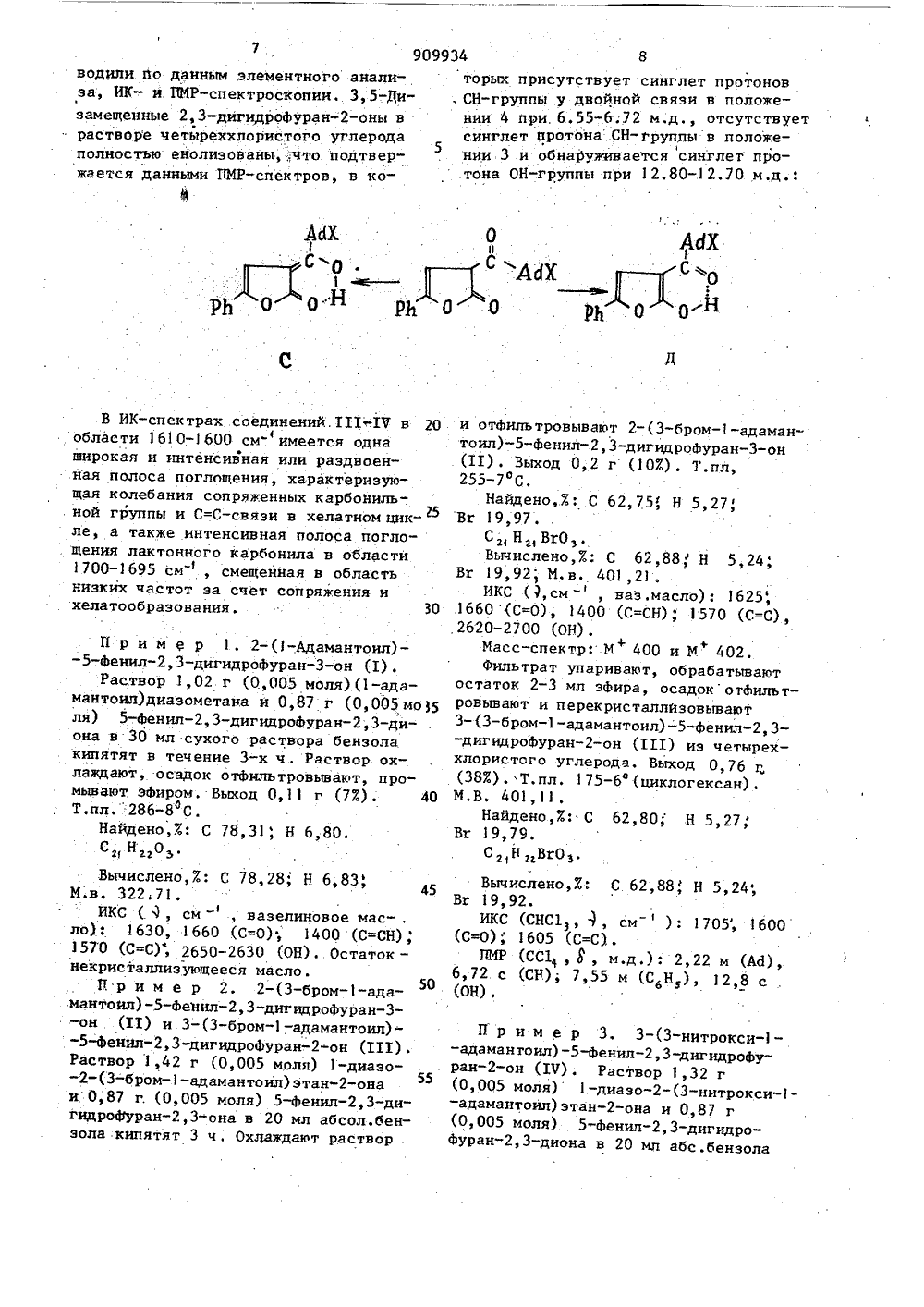
Способ получения адамантилсодержащих 2, 3-дигидрофуранонов
Похожие патенты | МПК / Метки | Текст | Заявка | Код ссылки
Номер патента: 909934
Авторы: Андрейчиков, Сивкова
Текст
=С =О 18 до соедииз-за синтевыход продуктов к 903 в зависимости нений. Этот спосо леблется оот исходныхограниченмых методополучениени 3-осулярной цик формулы:- фенил) нокислой сане или соли при 20 Нтсутствия прием ароилкетонов.Далее известноных дигидрофурвнутримолек аме щен в пу- изатем ОО 2,3-дигидрофувеществ,держащихступныхПост нов эт ле аралленная стигается ноадамантилсоанонов общих ову 50 вым спо обом пол 2,3-диг 11,111 нияИзобретение относится к химии про-.изводных адамантана, а именно к новому способу получения новых адаман.тилсодержащих 2,3-дигидрофуранонов,которые могут быть использованы длясинтеза различных соединений, содержащих адамантильный радикал, и какпотенциальные биологически активныевещества. 1 ОИзвестны способы получения различных замещенных адамантана, содержащих фурановый цикл.Так, 2,5-ди(1-адамантил)фуран получают действием серной, кислоты (дегидратация)на/1,4-ди(1-адамантил) бутан,4,-дион.Нри ацидолизе этилового эфира (3(1 -адамантоил) -акриловой кислоты по-.лучают соответствующую кислоту, при 20циклизации которой образуется-гидооксилактон,В ООССНС СНЫ П й О к видно из этой. схемы, полученим способом приводит к двум п льно образующимся продуктам, что лучае адамантанзамещенных продукт е позволяет прогнозировать структ у получающихся соединений. Цель изобретения - разработкаспособа получения новых адамантилс В этих способах синтеза для образования Ненасыщенного-лактонового кольца из различных карбонильных соединений обычно применяют щелочные или кислые агенты. Поэтому даже при наличии необходимых кислот или их производных, действие тех или иных агентов будет приводит к отщеплению заместителей в ядре адамантана из-за легкости образования 1-адамантилкатиона, что.делает полученные галоидили нитроксизамещенных адамантана невозможным.Кроме того, следует отметить, что известен способ получения 3,5-дизамещенных 2,3-дигидрофуран-онов, при взаимодействии диазокетонов с кетенами в среде абсолютного ксилола или толуола при температуре от минус бО до комнатной, например,.в реакции пь схеме: ции Ф -диазокетонов ННННОНН(К)НООК , где К этил, в присутствии сер Меди в кипящем циклогек рисутс твин комплексно СНзО)РНц 1 в бензол ыходом 13-4 ОЖ.Схема реакции:5 909934 6где Х - водород или бром по соедине- го замещенного (1-адамантоил)дщэомениям общих Формул 11 и ПГ, тана с 5-Фенил-. 2,3-дигидрофуран,3, - и бром или нитроксигруппа по диона при. кипяяении.в среде Фбсолют. - соединениям общей формулы 1 . ного бензола з течение 3-4-х ч.ф 5путем в заимодействия соответствующе- Схема реакции. следующдяСф О -Н 1) 2- (1 -адамантоил) -5-Фенигидрофуран-З-он, 2) 2-(3-бром-адамантоило "нРЬ о с 11 1О Адх ированные 3,5-дизамешрофуран-оны, где Хяют собой светло-желтеские вещества, нера римые в во гексане, э не и раство ле и ацето Синте 2,3-дигид представл к рис таллич де, плохо расФире, .циклогеримые в хлорне. Их иденти ные 0 ИО творимые в. ксане, пентаоформе, бензофикацию протво Как видно из этой схемы в процессе протекают параллельные реакции, с образованием 3-бензоил-адамантоил- -2,3-дигндрофуран-она и 2-диазо- -адамантоил-фенил3 5-пентантрионаь в/торый при нагревании разлагается. Проведение процесса менее 3-х ч не обеспечивает полного карбонилирования, а нагревание выше 4-х часов резко снижает выход целевого продукта.Согласно изобретению синтезируют четыре соединения: Синтезированные соединения 1 и 11представляют собой белые кристаллические высокоплавкие вещества, плохорастворимые в большинстве органическихрастворителей. В. ИК-спектрах 2,3-дигидрофуран-З-онов, снятых в вазелино вом масле, присутствуют интенсивныеполосы поглощения, соответствующие колебаниям сопряженной 1660 см-), иенолизованной (1570 см ) карбонильных групп. Интенсивная и несколькоуширенная полоса поглощения в области1630-1625 смотнесена нами к С=Ссвязи, сопряженной с карбоннльной.группой, .Наблюдается также слабая широкая полоса поглощения ОН-группы в О области 2700-2650 см , характернаядля енольныхсистем. Т.О. данные ИКспектроскопии соответствуют структуре 2-(1-адамантоил)-5-фенил,3-ди-гидрофуран-онов и говорят о сущест вовании их в енольных формах А и В:909934 торых присутствует синглет протонов , СН-группы у двойной связи в положении 4 при, 6.55-6.72 м.д., отсутствует синглет протона СН-группы в положе 1нии 3 и обнаруживается синглет протона ОН-группы при 12.80-12.70 м,д.: П р и м е р 1. 2-(1-Адамантоил)- -5-фенил,3-дигидрофуран-З-он (1).Раствор 1,02 г (0.,005 моля)(1 -адамантоил)диазометана и 0,87 г (0005 мо 35 ля) 5-фенил, 3-дигидрофуран; 3-диона в 30 мл сухого раствора бензола кипятят в течение 3-х ч, Раствор охлаждают, осадок отфильтровывают, промывают эфиром, Выход 0,11 г (7%), 40 Т,пл. 286-8 С.Найдено,%: С 78,31, Н 6,80.С,Н О Вычислено,7: С 78,28 Н 6,83,М.в. 322,71,ИКС (.1см - вазелиновое мас-,ло) Ф 1630, 1660 (С=О); 1400 (СщСН)1570 (С=С) 2650-2630 (ОН), Остаток -некристаллизующееся масло.П р и м е р 2. 2-(3-бром-ада 50мантоил)-5-Фенил-дигидрофуран-он . (П) и 3-(3-бром-адамантоил) --5-Фенил3-дигидрофуран-он (111) .Раствор 1,42 г (0,005 моля) 1-диазо-(3-бром-адамантоил)этан-онаи.0,87 г. (0,005 моля) 5-фенил,3-дигидробуран"23-она в 20 мл абсол.бенэола кипятят 3 ч . Охлаждают раствор водили по данным элементного анализа, ИК- и ПИР-спектроскопии. 3,5-,Дизамещенные 2,3-дигидрофуран-оны в растворе четыреххлористого углерода полностью ейолизованы,что подтвержается данными ПМР-сйектров в коМ В ИК-спектрах соединений.1 П .17 в 20 области 1610-1600 см- имеется одна широкая и интенсивная или раздвоенная полоса поглощения, характеризующая колебания сопряженных карбонильной группы и С=С-связи в хелатном цик" ле, а также интенсивная полоса погло. щения лактонного карбонила в области 1700-1695 смсмещенная в область низких частот за счет сопряжения и хелатообразования. 30 и отфильтровывают 2-(3-бром-адамантоил)-5-фенил,3-дигидрофуран-З-он909934 Найдено,7.: С 65,65, Н 547,М 3,56. С ,Н НО,. сТехред Л.Сердюкова Корректор М.Максимишинец Редактор И.Ленина Заказ 1693 Тираж 319 ПодписноеВНИИПИ Государственного комитета по изобретениям н открытиям при ГКНТ СССР 113035, Москва, Ж, Раушская наб , д. 4/5 Производственно-издательский комбинат "Патент", г.ужгород, ул. Гагарина,101 9кипятят 3-3,5 ч. Охлаждают раствор,фильтруют, фильтрат упаривают, остаток промывают эфиром и получают0,50 г (267) 3-(3-нитрокси-адамантоил) -5-фенил,3-дигидрофуран-она (Е 7). Т,пл. 148-50 фС (циклогексан). М,в. 383,21,1 ОИКС (СНС 1, 9, см): 16 0 1695(ОН) .Соединения ЕЕЕ и Е 7 при разведении 1:8000 подавляют рост золотистого стафилококка, а в разведении1 4000 (для ЕЕЕ) и 1:2000 (для Е 7)подавляют рост кишечноф палочки.
СмотретьЗаявка
2924172, 18.03.1980
ПЕРМСКИЙ ГОСУДАРСТВЕННЫЙ ФАРМАЦЕВТИЧЕСКИЙ ИНСТИТУТ
АНДРЕЙЧИКОВ Ю. С, СИВКОВА М. П
МПК / Метки
МПК: C07D 307/58
Метки: 3-дигидрофуранонов, адамантилсодержащих
Опубликовано: 23.04.1990
Код ссылки
<a href="https://patents.su/5-909934-sposob-polucheniya-adamantilsoderzhashhikh-2-3-digidrofuranonov.html" target="_blank" rel="follow" title="База патентов СССР">Способ получения адамантилсодержащих 2, 3-дигидрофуранонов</a>
Предыдущий патент: Совмещенная антенна
Следующий патент: Устройство для определения реактивной силы паров
Случайный патент: 221593