Способ определения активности фитоадаптогенов
Похожие патенты | МПК / Метки | Текст | Заявка | Код ссылки
Текст
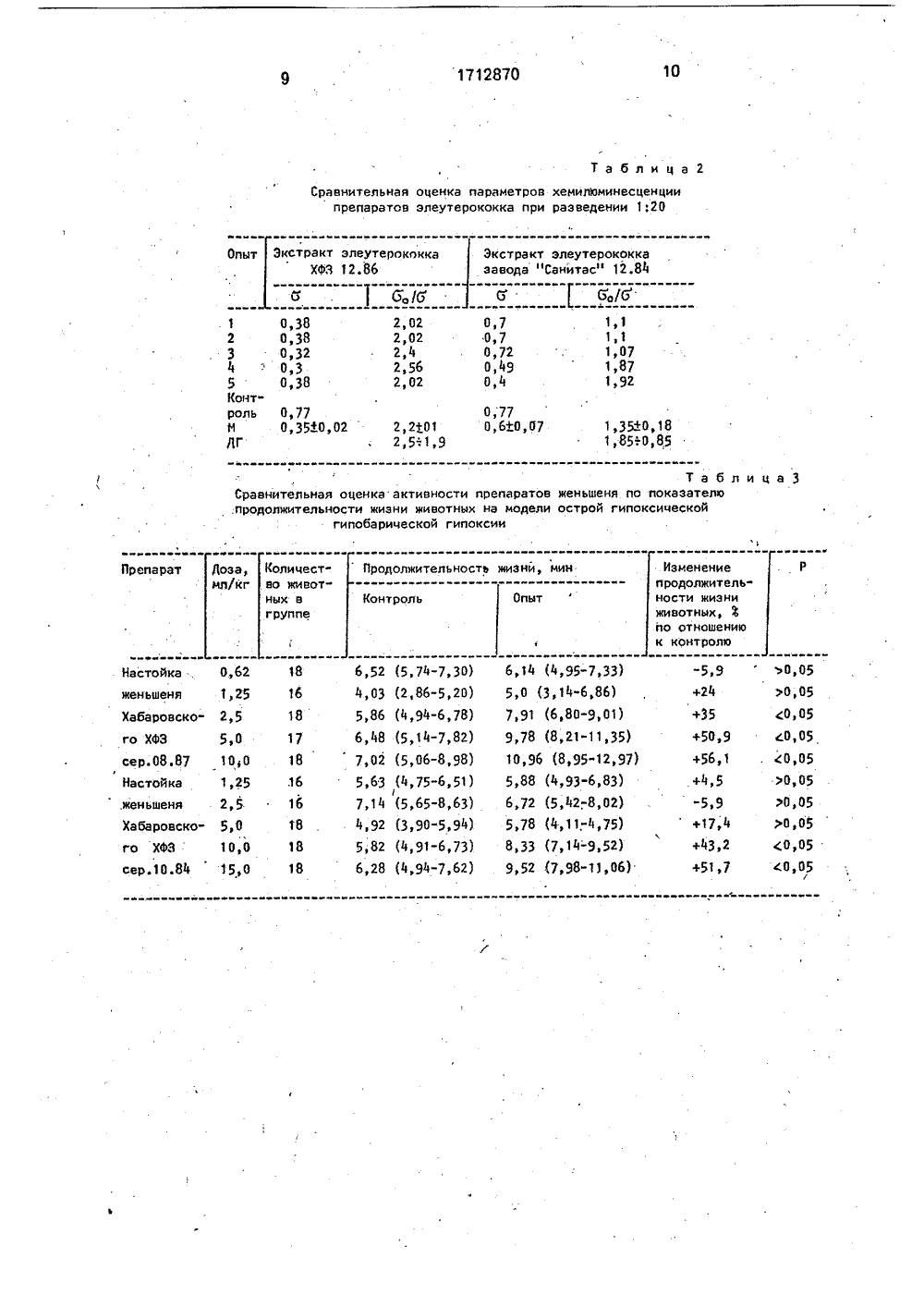
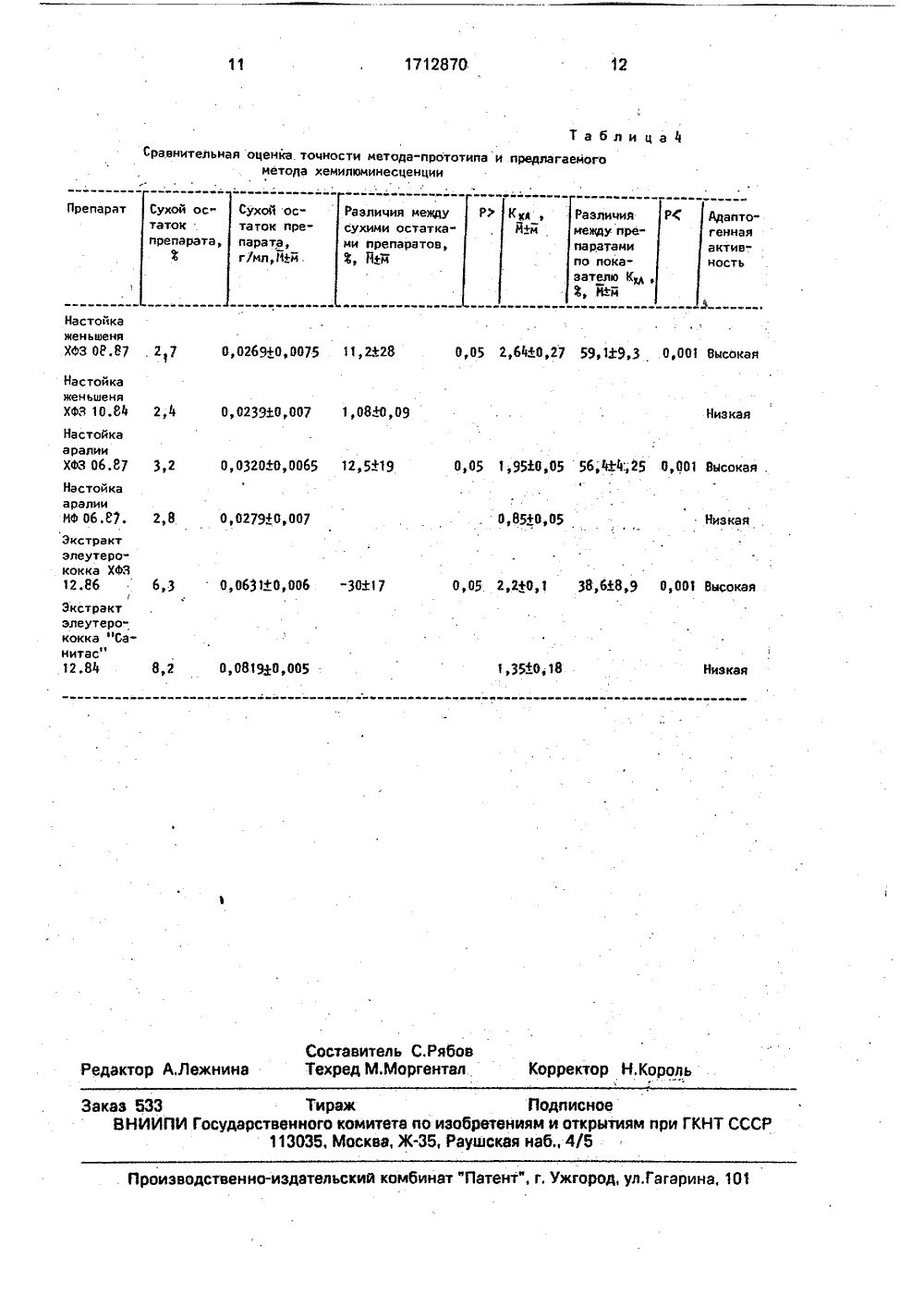
(19) ц 5 о 01 м 33 й ПИС РЕТЕНИ К АВ ский институт лекарственных юковская, Л. Р. . Каплан, Ф, П; ЛЕНИЯ АКТИВНОНОВдназначено для ис-фармацевтическойицинедля определемедицине, а фективности ет быть исевтической. М (Я я повыш пределения о остатка на й вспышки несценции(ХЛ),Спосозом. бр 5 млосуха прованнойения пр:40. 1:80 иваютилли- азве 1:20; ления ГОСУДАРСТВЕННЫЙ КОМИТЕТПО ИЗОБРЕТЕНИЯМ И ОТКРЫТПРИ ГКНТ СССР АНИЕ ИЗОБ МУ СВИДЕТЕЛЬСТ(54) СПОСОБ ОПРЕД СТИ ФИТОАДАПТОГЕ (57) Изобретение пре пользования в химик промышленности и мед Изобретение относится к именно к способам оценки эф лекарственных средств, и мож пользовано в химико-фармац промышленности.Целью изобретения являет ние точности способа.Цель достигается путем о влияния водного раствора сухог показатель скорости медленно Ре -индуцированной хемилюм 2+ б осуществляют следующимспиртового раствора выпари 70 С, разводят в 1 мл дистводы, Изучают следующиеепаратов; 1:1; 1:2; 1;5; 1:101:100; 1:200 с целью выяв ния активности фитоадаптогенов. Цель изобретения - повышение точности способа. Цель достигается за счет определения антиокислительной активности (АОА) препаратов. 5 мл исследуемого фитоадаптогена упаривают (до полного удаления спирта) до сухого остатка и далее готовят водный раствор с содержанием его в 1 мл не менее 10 мг и не более 12 мг, определяют влияние водного раствора на показатель скорости "медленной вспышки" Ее -индуцирован 2+ной хемилюминесценции (ХЛ), рассчитывают коэффициент ХЛ, пропорциональный АОА, и при значении этого коэффициента ХЛ, находящегося в пределах более 1, 9, определяют высокую адаптогенную активность препаратов. 4 табл,степени ингибирования ими перекисного окисления липидов (ПОЛ). Эффективными являются разведения, ингибирующие ПОЛ на 50, Для настойки аралии такое разведение составляет 1:4, для экстракта элеутерококка - 1:20, для настойки женьшеня - 1;2 (содержание сухих веществ в ячейке составляет 0,2 мг в 1 мл суспензии для всех вышеуказанных препаратов в данных разведениях). Остальные разведения изучаемых препаратов либо вызывали полное, ингибирование ПОЛ, либо давали результаты, достоверно не отличающиеся от контроля. Суспензию готовят из желтка куриных яиц путем перемешивания его с фосфатным буфером (20 мл КН 2 РОа, 105 ммоль КС 1, рН 7,4) в соотношении 1:1 на магнитной мешалке со скоростью 500 об/мин в течение 10 мин. 1 мл липосом помещают в термостатируемую кювету (при 37 С), которую устанавливают в светонепроницаемой камере над торцом фотоэлектронного умножителя ФЭУА-хемилюминометра, К липосомам добавляют 2,9 мл фосфатного буфера и 0,1 мл раствора препарата. После 3 мин инкубации при постоянном перемешивании содержимого при 380 об/мин открывают шторку, отделяющую дно кюветы от торца ФЭУ, регистрируют исходный уровень ХЛ, после чего в ячейку вводят 1 мл 10 М раствора Ре 50 с последующей регистрацией всех стадий ХЛ (быстрая вспышка, латентный период, медленная вспышка). Таким образом оценивается действие всех укаэанных выше разведений препаратов, концентрация сухого остатка в которых была известна. Рассчитывают скорость медленной вспышки ХЛ, измеренную как 19 угла наклона начальной экспоненциальной,части медленной вспышки,. Затем рассчитывают коэффициент ХЛ, пропорциональный антиокислительной активности лекарственных препаратов:Кхл= юго;где о, -ц угла начальной экспоненциальной части медленной вспышки ХЛ липосом без препарата;о - щ угла наклона начальной экспоненциальной части медленной вспь 1 шки ХЛ липосом в присутствии препарата,П р и м е р 1. Настойка аралии ХФЗ 06.87, и настойка аралии МФ 06,87. Проведена сравнительная оценка адаптогенной активности на моделях гипоксической гидоксии, гипероксии и ишемии ЦНС и сердечно-сосудистой системы у лягушек.Гипоксическая гипоксия. Опыт проводили на белых беспородных мышах массой 20 г средней устойчивости к гипоксии. Предварительно в течение 2 дней мышам вводили по 0,1 мл водного раствора препарата внутрибрюшинно, контрольной группе вводили по 0,1 мл дистиллированной воды. На третий день(день эксперимента) препараты вводили за три часа до начала эксперимента. Гипоксическая гипоксия достигалась разряжением на высоте 11 км, подьем осуществляли втечение 110 с. Определяли срок гибели мышей.Гипербарическая оксигенация. Эксперименты проводили на белых беспородных мышах массой 20 г. Предварительно в течение 2 дней мышам вводили по 0,1 мл водного раствора препарата внутрибрюшинно, контрольной группе вводили. такое же количество дистиллированной воды, На третий рень (день эксперимента) препараты вводили за три часа до начала эксперимента, Гипербарическую оксигенацию создавали в барокамере при 5 ати в течение 40 мин, Срок компрессии и декомпрессии равен 20 мин.Определяли время наступления судорог, срок жизни в барокамере и процент гибели.Ишемия ЦНС и сердечно-сосудистойсистемы. Исследования проводили на лягушках-самцах (Яапа теврогаг а) на модели ишемии ЦНС и сердечно-сосудистой систе мы, предложенной А. Н. Кудриным, Водныерастворы препаратов вводили лягушкам в задний лимфатический мешок в течение 2дней. В первый день препараты вводилидважды с интервалом в 3 ч. На второй день(день эксперимента) препараты вводили за3 ч до начала эксперимента, Контрольным 20 25 30 35 40 45 50 55 лягушкам вводили в течение 2 дней по 0,1 мл дистиллированной воды. До начала введения препаратов лягушки сутки находились при комнатиой температуре (+18 С) и далее во время эксперимента также находились при той же температуре, У лягушек прекращали кровообращение путем каложения лигатуры на дугу аорты, Затем фиксировали сроки угасания простого рефлекса спинного мозга (вынимание лапки из 0,35 ф/- ного раствора серной кислоть 1). После пре- кращения рефлексов оставляли лигатуру на аорте в течение 20 мин (срок относительной биологической смерти для ЦНС, после которого происходит самопроизвольное восстановление рефлексОв), Затем проводили реперфузию ЦНС и всего организма возобновлением кровообращения путем снятия лигатуры с дуги аорты и наблюдали за последующим восстановлением рефлексов ЦНС. Отмечали срок восстановления простого рефлекса спинного мозга и процент гибели лягушек после реперфузии.Для определения антиокислительной активности и расчета коэффициента ХЛ, пропорционального антиокислительной активности лекарственных препаратов, измеряли скорость медленной вспышки ХЛ липосом при инкубации с водным раствором препарата, содержащим сухих веществ в ячейке 0,2 мг в 1 мл суспензии. Определение проводили для двух серий настоек аралии (табл. 1). При определении коэффициента ХЛ настойки аралии ХФЗ 06.87. оо= = 1,51, значение о =. 0,76. Кхл= СМг = =1,51/0,76=1,99, что выше нижнего уровня доверительного интервала значений коэфФициента ХЛ для настойки аралии. Это свидетельствует о высокой антиокислительной активности. При определении коэффициента ХЛ настойки аралии МФ 06.87. значение о,= 1,51, значение а = 1,42. Кхл= а,/а =- =1,510,42=1,06, что ниже нижнего уровнядоверительного интервала значений коэффициента ХЛ для настройки аралии (это свидетельствует о низкой антиокислительнойактивности).Настойка аралии ХФЗ 06,87. обладает 5более высокой адаптогенной активностьюпри ишемии ЦНС лягушки, гипероксии, приотсутствии, достоверных различий междуними при гипоксической гипоксии. Коэффициент ХЛ настойки аралии с высокой адаптогенной активностью составляет 1,9 ивыше, Сухой остаток в настойке аралииХФЗ 06.87, составляет 3,2 о , в настойке аралии МФ 06,87. - 2,8 о , Адаптогенная активность настойки аралии ХФЗ 06.87. 15отличаетсяот настойки аралии МФ 06,87. пометодике ишемии ЦНС лягушкисоответственно на ЗЗо , по значению коэффициентаХЛ - на 59,2%, то по сухому остатку - на13 о , что свидетельствует о том, что способ 20стандартизации по значению коэффициента ХЛ является более точным, чем прототип.П р и м е р 2. Экстракт элеутерококказавод "Санитас" 12,84. и экстракт злеутерококка ХФЗ 12,86. Проведена оценка адаптоген ной активности на моделяхгипоксической гипоксии, гипероксии и ишемии ЦНС и сердечно-сосудистой системы улягушек, Методики проведения идентичныдля настойки аралии, Измеряли скорость 30медленной вспышки ХЛ при инкубации сводным раствором препарата, содержащимсухих веществ в ячейке 0,2 мг в 1 мл суспензии. Определение проводили для двух серий экстракта элеутерококка (см. табл. 2). 35При определении коэффициента ХЛ для экстракта элеутерококка ХФЗ 12,86. Оо ==0,77/0,3=2,56, что выше нижнего уровнядоверительного интервала значений козффициента ХЛ для экстракта элеутерококка,Это свидетельствует о высокой антиокислительной активности. При определениикоэффициента ХЛ для экстракта элеутерококка завода "Санитас" 12.84. значение оо= 45=0,77/0,7=1,1, что ниже нижнего уровня доверительного интервала значений коэффициента ХЛ для экстракта элеутерококка, Этосвидетельствует о низкой антиокислительной активности,Экстракт элеутерококка ХФЗ 12.86, обладает более высокой адаптогенной актив-ностью при ишемии ЦНС лягушки,гипероксии, гипоксической гипоксии. Коэффициент ХЛ экстракта элеутерококка свысокой адаптогенной активностью составляет 1,9 и более. Сухой остаток в экстрактеэлеутерококка завода "Санитас" 12,84, равен 8,2, в экстракте элеутерококка ХФЗ 12.86. - 6,3 . Адаптогенная активность экстракта элеутерококка ХФЗ 12,86, отличается от экстракта элеутерококка завода "Санитас" 12.84. по методике ишемии ЦНС лягушки соответственно на 15,4, значение коэффициента ХЛ - на 42,9, по методике прототипа, содержание сухого остатка в экстракте элеутерококка завода "Санитас" больше на 23,2. Это свидетельствует о том, что способ стандартизации с использованием коэффициента ХЛ является более точным, чем прототип.П р и м е р 3. Настойка женьшеня ХФЗ 10,84. и настойка женьшеня ХФЗ 08.87. Проведена сравнителная оценка адаптогенной активности на моделях гипоксической гипоксии и на устойчивость животных к повторным физическим нагрузкам. Методика проведения гипоксической гипоксии (см. пример 1).Полученные результаты приведены в табл, 3,Изучение влияния препаратов женьшеня на устойчивость животных к повторным физическим нагрузкам. В экспериментах былииспользованы белые беспородные мыши - самцы массой 18 - 25 г. Предварительно животные были подвергнуты отбору по показателям физической работоспособности- плавание до полного утомления в бассейне с постоянной температурой 25 С. Критерием обора служила продолжительность плавания не менее чем 4 мин. При проведении исследований животным при первом плавании предлагалась физическая нагрузка, составляющая 80 оот максимальной. При повторном плавании, которое осуществлялось спустя 2 ч после завершения первого плавания, животные выполняли физическую нагрузку до максимального утомления. Критерием оценки эффективности препаратов служило увеличение длительности повторного плавания по сравнению с контролем, Для получения стабильных результатов и уменьшения "разброса" вариационного ряда экспериментальных данных животным подвешивали специально при- . способленный груз, не затрудняющий движений и составляющий 5 оот массы тела. Препараты вводили опытным животным в течение 7 дней, а в последний день за 1 ч до повторного плавания внутрибрюшинно в дозах 1 - 20 мл/кг. Контрольным животным в том же режиме внутрибрюшинно вводили физиологический раствор в тех же объемах, что и опытным животным. Продолжительность плавания животных регистрировали в секундах,1712870 Таблица 1 Сравнительная оценка параметров хемилюминесценции препаратов аралии при разведении 1:4Измеряли скорость медленной вспышки ХЛ липосом при инкубации с воднымраствором препарата, содержащим сухихвеществ в ячейке 0,2 мг в 1 мл суспензии,При определении коэффициента ХЛ, пропорционального антиокислительной активности, для настойки. женьшеня ХФЗ 08.87.значение Оо= 1,09, значение о= 0,46. Кхл== сго/и =1,09/0,46=2,46, что выше нижнегоуровня доверительного интерала значений 10коэффициента ХЛ. Это свидетельствует овысокой антиокислительной активности,При определении коэффициента ХЛ для настойки женьшеня ХФЗ 10,84 значение Оо==1,09/1,28=0,85, что ниже нижнего уровня,доверительного интервала значений коэффициента ХЛ. Это свидетельствует о низкойантиокислительной активности,Настойка женьшеня ХФЗ 08.87, обладает более высокой адаптогенной активностью при гипоксической гипоксии,устойчивости животных к повторным физическим нагрузкам, Сухой остаток настойкиженьшеня ХФЗ 08.87, составляет 2,7 о , а внастойке женьшеня ХФЗ 10.84,-2,4%,Адаптогенная активность настойки женьшеня ХФЗ 08,87. отличается от настойкиженьшеня ХФЗ 10,84, по показателю их влияния на физическую выносливость продолжительность повторного плавания) при дозе5 мл/кг соответственно на 63,7 о , по методугипоксической гипоксии - на 33,5%, по значению коэффициента ХЛ - на 40,3%; а пометодике прототипа содержание сухого ос татка отличается на 0,3 о . Это свидетельствует о том, что способ оценки эффективности с использованием коэффициента ХЛ является более точным, чем прототип.Таким образом, результаты изучения влияния водного раствора на показатель скорости медленное вспышки Ее -индуци+ рованной ХЛ свидетельствует о том, что при значении коэффициента ХЛ для настоек аралии и женьшеня, а также экстракта эле-. утерококка выше 1,9 при содержания сухих веществ в ячейке 0,2 мг в 1 мл суспензии) препараты обладают высокой адаптогенной активностью (табл, 4).Ф ар мула изобретен ия Способ определения активности фитоадаптогенов путем исследования сухого остатка раствора фитоадаптогена, о т л и ч а ющ и й с я тем, что, с целью повышения точности способа, исследуют влияние водного раствора фитоадаптогена на скорость+2медленной вспышки Ге;индуцированной хемилюминесценции, затем рассчитывают коэффициент хемилюминесценции, пропорциональный антиокислительной активности фитоадаптогена по формуле Кхл= = (то/о, где 0 о - щ угла наклона начальной экспоненциальной кривой медленной вспышки хемилюминесценции липосом без препарата; о-тц угла наклона той же кривой в присутствии исследуемого фитоадаптогена и при значении коэффициента хемилюминесценции выше 1,9, определяемой высокую адаптогенную активность препарата.1712870 Таблица 2 Сравнительная оценка параметров хемилюминесценции препаратов элеутерококка при разведении 1;20Опыт Экстракт элеутерококка ХФЗ 12.86 Экстракт элеутерококка завода "Санитас" 12.84о/3 БоФ 0 38 0,38 0,32 0,3 0 38 1,11,071,871,92 0,7 0,7 0,72 0,49 0,4 2,02 2,02 2,4 2,56 2,02 О,770,6+0,07 0,770 35+0 02 1,35+0, 18 1,85-:0,85 2, 2+012,5-:1,9 Таблица 3Сравнительная оценка активности препаратов женьшеня по показателю.продолжительности жизни животных на модели острой гипоксицескойгипобарической гипоксии Продолжительность жизнй мин Коли 4 ество животных вгруппе Изменение продолжительности жизни животных, Ф по отношениюк контролю Препарат Доза, мл/кг Опыт Контроль+24 Настойка женьшеня Хабаровского ХФЗ сер. 08.87Ф Настойка1712870 Таблица 4С равнительная оценка точности метода-прототипа и предлагаемогометода хемилюминесценцииГ Препарат Сухой остаток .препарата,км эЙ+м Настойка женьшеня 0,0269+0,0075 11,2+28 0,05 2,64+0,27 59,129,3 0,001 Высокая хфэ ОЕ,87 . 2,7 Настойка женьшеня хфз 1 оЯ 4 2,4 0,.023910,007 1,0840,09 Низкая Настойкааралии хфз ОБЯ 7 0,05 1,9 М 0,05 56,Ю:,25 0,001 Высокая1 о,озго+а,аа 65 12,5+19 3,2 НастойкааралииИф Об.с 7. 0,85+0,05 Низкая 2,8 0,0279+0,007 0,05. 2)2+0,1 38,618,9 0,001 Высокая 6,30,0631+0,006 -ЗОН 7 Экстракт элеутерококка "Санитас"12,84 8,2 0,0819+0,005 1,35+0,18 Низкая Составитель С,РябовТехред М.Моргентал Корректор Н,Король Редактор А.Лежнинэ Заказ 533 Тираж Подписное ВНИИПИ Государственного комитета по изобретениям и открь 1 тиям при ГКНТ СССР 113035, Москва, Ж, Раушская наб., 475 Производственно-издательский комбинат "Патент, г. Ужгород, ул.Гагарина, 10 Экстрактэлеутерококка Хфя12.86 Сухой ос"таток препарата,гlмл,ЙФм . Различия между сухими остатками препаратов Ф ВФм Различиямежду препаратамипо показателю Кю
СмотретьЗаявка
4659595, 06.03.1989
НАУЧНО-ИССЛЕДОВАТЕЛЬСКИЙ ИНСТИТУТ ТЕХНОЛОГИИ И БЕЗОПАСНОСТИ ЛЕКАРСТВЕННЫХ СРЕДСТВ
ГУКАСОВ ВАДИМ МИХАЙЛОВИЧ, КРЮКОВСКАЯ ЕЛЕНА ВЛАДИМИРОВНА, ГАЛУШКИНА ЛИДИЯ РОБЕРТОВНА, КУДРИН АЛЕКСАНДР НИКОЛАЕВИЧ, КАПЛАН ЕЛИЗАР ЯКОВЛЕВИЧ, КРЕНДАЛЬ ФЕЛИКС ПЕТРОВИЧ, ЛЕВИНА ЛЮДМИЛА ВЛАДИМИРОВНА
МПК / Метки
МПК: G01N 33/48
Метки: активности, фитоадаптогенов
Опубликовано: 15.02.1992
Код ссылки
<a href="https://patents.su/6-1712870-sposob-opredeleniya-aktivnosti-fitoadaptogenov.html" target="_blank" rel="follow" title="База патентов СССР">Способ определения активности фитоадаптогенов</a>