Способ получения 1r, 3s-2, 2-диметил-3-(2-оксопропил) циклопропанацетонитрила
Формула | Описание | Похожие патенты | МПК / Метки | Текст | Заявка | Код ссылки
Номер патента: 1689376
Авторы: Володарский, Пентегова, Рукавишников, Ткачев
Формула
1. СПОСОБ ПОЛУЧЕНИЯ 1R,3S-2,2-ДИМЕТИЛ-3-(2-ОКСОПРОПИЛ)-ЦИКЛОПРОПАНАЦЕТОНИТРИЛА формулы 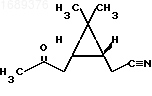
исходя из (+)-3-карена, отличающийся тем, что, с целью увеличения выхода и упрощения процесса, (+)-3-карен обрабатывают эквимолярным количеством нитрозилхлорида в инертном низкокипящем хлорсодержащем органическом растворителе при температуре (-10)-0oС затем к реакционной смеси добавляют метанол и водный раствор диметиламина в молярном соотношении карен метанол диметиламин, равном 1 (3,4 5,0) (2,5 3,5), и образующийся при этом оксим 3-N, N-диметиламинокаран-4-она подвергают в присутствии основания взаимодействию с уксусным ангидридом, при молярном соотношении оксим: уксусный ангидрид, равном 1 (1,1 2,2).
2. Способ по п. 1, отличающийся тем, что процес взаимодействия оксима 3-N, N-диметиламинокаран-4-она с уксусным ангидридом проводят в среде хлороформа, диэтилового эфира или смеси вода-диоксан или вода-бензол.
Описание
(1)
 C
C Цель изобретения увеличение выхода целевого продукта и упрощение процесса.
Изобретение иллюстрируется нижеприведенными примерами.
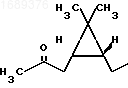
П р и м е р 1. Получение аминооксима (2).
Получение продукта (2) иллюстрируется следующей схемой:
(2)
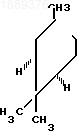
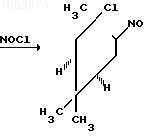
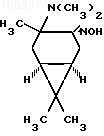
10 г (73,5 ммоль) (+)-3-карена, выделенного при ректификации основного скипидара и имеющего [
П р и м е р ы 2-8. Получение аминооксима проводят по общей методике примера 1, но с использованием различных хлорсодержащих растворителей и различными реакционными условиями. Полученные результаты представлены в таблице.
Проведение процесса присоединения хлористого нитрозила к карену при температуре ниже, чем -10оС нецелесообразно, так как не приводит к увеличению выхода аминооксима (пример 4). При увеличении температуры выше 0оС может произойти разложение реакционной массы.
Добавление метанола необходимо, так как в противном случае (пример 6) образуется большее количество побочных продуктов. Проведение же процесса с избытком метанола более 4-х (см. пример 7) не приводит к увеличению выхода.
Далее, теоретически, на 1 моль карена должно расходоваться 2 моля диметиламина, практически же для достижения максимального выхода аминооксима (2) необходимо брать избыток диметиламина; наилучший выход аминооксима достигается при мольном соотношении карен:диметиламин=1,0:(3-3,5); при уменьшении количества диметиламина выход аминооксима снижается (см. пример 5).
П р и м е р 9*. Получение кетонитрила (1) (пример сравнительный).
Получение продукта (1) осуществляют по схеме
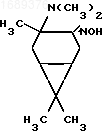
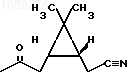
(I) при использовании стандартной методики, в которой вместо пара-толуолсульфохлорида показана возможность использования уксусного ангидрида.
К раствору 1 г едкого кали (17,9 ммоль) в 5 мл воды прибавляют раствор 1 г аминооксима (2) (4,8 ммоль) в 5 мл диоксана. Смесь нагревают до 40оС и при интенсивном перемешивании по каплям прибавляют 1 г уксусного ангидрида (9,8 ммоль). Затем добавляют еще 1 г едкого кали и после растворения щелочи прикапывают 1 г уксусного ангидрида. Эту операцию повторяют еще дважды. Всего прибавляют 4 г (39,2 ммоль) уксусного ангидрида и 4 г (71,6 ммоль) едкого кали. После этого растворитель и побочные продукты отгоняют в вакууме при температуре бани 100оС и остаточном давлении 20 мм рт.ст. к остатку прибавляют 10 мл воды, органические продукты экстрагируют эфиром (2х10 мл). Эфирный экстракт промывают насыщенным водным раствором хлористого натрия (10 мл), сушат безводным сульфатом натрия (1 г), упаривают в вакууме и получают 0,75 г (4,5 ммоль, выход 94% от теоретического в расчете на аминооксим (2)) кетонитрила (1), который имеет характеристики (
П р и м е р 10. Получение кетонитрила (1).
К раствору 6 г аминооксима (2) (28,5 ммоль) в 40 мл хлороформа добавляют 3 г измельченного карбоната натрия (28,3 ммоль) и при интенсивном перемешивании при комнатной температуре по каплям прибавляют 4 мл уксусного ангидрида (4,3 г, 42,3 ммоль). После окончания прибавления уксусного ангидрида реакционную смесь выдерживают при перемешивании около 1 ч, после чего фильтруют, фильтрат упаривают в вакууме водоструйного насоса на водяной бане, остаток нагревают в вакууме (остаточное давление 5 мм рт.ст. температура бани 100оС) в течение получаса для удаления диметилацетамида и получают 4,5 г (выход 96% в расчете на аминооксим (2)) кетонитрила (1).
П р и м е р 11. Получение кетонитрила (1).
К раствору 2,1 г аминооксима (2) (10 ммоль) в смеси 2,2 г триэтиламина (22 ммоль), 0,2 мл воды и 5 мл бензола при нагревании на водяной бане (50-60оС) и интенсивном перемешивании по каплям в течение получаса прибавляют 2,3 г уксусного ангидрида (22 ммоль). Реакционную смесь нагревают при той же температуре еще 30 мин, после чего охлаждают до комнатной температуры, органический слой отделяют, водный слой экстрагируют эфиром (2х5 мл) и объединенный органический экстракт промывают насыщенным водным раствором хлористого натрия (5 мл) и сушат безводным сульфатом натрия (1 г), после отгонки растворителя в вакууме водоструйного насоса остаток выдерживают в вакууме при 5 мм рт. ст. и температуре бани 100оС в течение получаса для удаления диметилацетамида и получают 1,5 г кетонитрила (1) (9,1 ммоль, выход 91% в расчете на аминооксим (2)).
П р и м е р 12. Получение кетонитрила (1).
Выход 90%-ного нитрила (1) достигается при использовании хлороформа вместо бензола при тех же количествах реагентов, что и в примере 9.
П р и м е р 13. Получение кетонитрила (1).
Выход 89% нитрила (1) достигается при использовании диэтилового эфира вместо бензола и проведении реакции при 35-40оС, при тех же количествах реагентов, что и в примере 9.
П р и м е р 14*. Получение кетонитрила (1).
При проведении процесса по методике и с количествами, приведенными в примере 9, но при соотношении диоксан:вода=1,5:1, выход кетонитрила (1) составляет 66% от теоретического в расчете на аминооксим (2).
П р и м е р 15*. Получение кетонитрила (1).
При проведении процесса по методике и с количествами, приведенными в примере 9, но при соотношении диоксан:вода=1:1,5 в результате реакции получают смесь кетонитрила (1) и исходного продукта (2) в соотношении 2:1.
П р и м е р 16. Получение кетонитрила (1).
Аминооксим (2) (12,0 г, 0,057 моль) растворяют в 250 мл диэтилового эфира, добавляют 6 г (0,057 моль) порошкообразного карбоната натрия, по каплям при перемешивании добавляют 8,6 г (0,084 моль) уксусного ангидрида, реакционную смесь кипятят с обратным холодильником при перемешивании в течение 4 ч. Реакционную смесь фильтруют от осадка, осадок на фильтре промывают эфиром (5х5 мл), фильтрат упаривают в вакууме, остаток нагревают в вакууме (остаточное давление 5 мм рт.ст. Т=100оС) в течение получаса и получают 8,9 г кетонитрила 1 (0,054 моль, выход 94%).
Мольное соотношение реагентов аминооксим:карбонат натрия:уксусный ангидрид 1:1:1,5.
П р и м е р 17. Получение кетонитрила (1).
К смеси аминооксима (2) (158 г. 0,75 моль) и триэтиламина (84,6 г, 0,84 моль) при перемешивании и охлаждении добавляют по каплям 85,3 г (0,84 моль) уксусного ангидрида, не допуская подъема температуры в реакционной смеси выше 23-25оС. После прибавления ангидрида реакционную смесь оставляют при комнатной температуре на 3 ч, охлаждают до +10оС, при интенсивном перемешивании вливают в один прием 600 мл воды, нагревают реакционную смесь до 70оС, выдерживают при этой температуре в течение 1 ч, охлаждают, добавляют 150 мл эфира, встряхивают, эфирный слой отделяют, водный слой экстрагируют эфиром (2х50 мл), эфирные экстракты объединяют, промывают 50 мл 3%-ной водной серной кислоты, 50 мл 0,5 н. водного карбоната натрия, 50 мл насыщенного водного хлористого натрия, сушат безводным сульфатом натрия, упаривают в вакууме, остаток перегоняют в вакууме, собирая фракцию с т.кип. 115-116оС при 5 мм рт. ст. и получают 115,5 г кетонитрила 1 (0,70 моль, выход 93%), идентичного продукту, получаемому по примеру 9.
Мольное соотношение реагентов аминооксим:триэтиламин:уксусный ангидрид1: 1,1:1,1.
Хотя для превращения 1 моля аминоксима (2) в кетонитрил достаточно 1 моля уксусного ангидрида, однако для более полного превращения аминооксима в кетонитрил целесообразно использовать уксусный ангидрид в избытке от 0,1 до 1,1 моля на 1 моль аминооксима. Дальнейшее увеличение количества взятого уксусного ангидрида (пример 9) не приводит к увеличению выхода продукта (1).
Таким образом, предложенный способ получения 1R, 3S-2,2-диметил-3(2-оксопропил)-циклопропанацетонитрила позволяет повысить выход целевого продукта с 50% в известном способе до 72-82% в расчете на исходный карен и упростить способ его получения за счет сокращения числа стадий процесса (с 4-х в известном способе до 2-х в предложенном).
Изобретение относится к производным нитрилов, в частности к получению 1R, 3S - 2,2 - диметил - 3 - (2 - оксопропил) - циклопропанацетонитрила, используемого в синтезе инсектицидов - пиретроидов. С целью увеличения выхода и упрощения процесса (+) - 3 - карен обрабатывают эквимолярным количеством нитрозилхлорида в инертном низкокипящем хлорсодержащем органическом растворителе при (-10) - 0°С. Затем добавляют метанол и водный раствор диметиламина. Процесс ведут в молярном соотношении карен : метанол : диметиламин 1 : (3,4 - 5,0) : (2,5 - 3,5). Образующийся оксим - 3 - N, N - диметиламинокаран - 4 - она подвергают в присутствии основания взаимодействию с уксусным антигидридом при молярном соотношении оксим : уксусный ангидрид 1 : (1,1 - 2,2) и предпочтительно в среде хлороформа, диэтилового эфира или смеси вода - диоксан или вода - бензол. Выход до 82%. Число стадий процесса сокращается до двух (против четырех). 1 табл.
Рисунки
Заявка
4709729/04, 22.06.1989
Новосибирский институт органической химии СО АН СССР
Рукавишников А. В, Ткачев А. В, Володарский Л. Б, Пентегова В. А
МПК / Метки
МПК: C07C 253/00, C07C 255/30
Метки: 2-диметил-3-(2-оксопропил, 3s-2, циклопропанацетонитрила
Опубликовано: 27.06.1995
Код ссылки
<a href="https://patents.su/1-1689376-sposob-polucheniya-1r-3s-2-2-dimetil-3-2-oksopropil-ciklopropanacetonitrila.html" target="_blank" rel="follow" title="База патентов СССР">Способ получения 1r, 3s-2, 2-диметил-3-(2-оксопропил) циклопропанацетонитрила</a>
Предыдущий патент: Способ корреляционного анализа газов и устройство для его осуществления
Следующий патент: Устройство приведения в действие поверхностей управления
Случайный патент: Смазка для изложниц при сифонной разливке стали под теплоизолирующими смесями






