Способ кулонометрического определения кадмия в ртутьсодержащих материалах
Похожие патенты | МПК / Метки | Текст | Заявка | Код ссылки
Текст
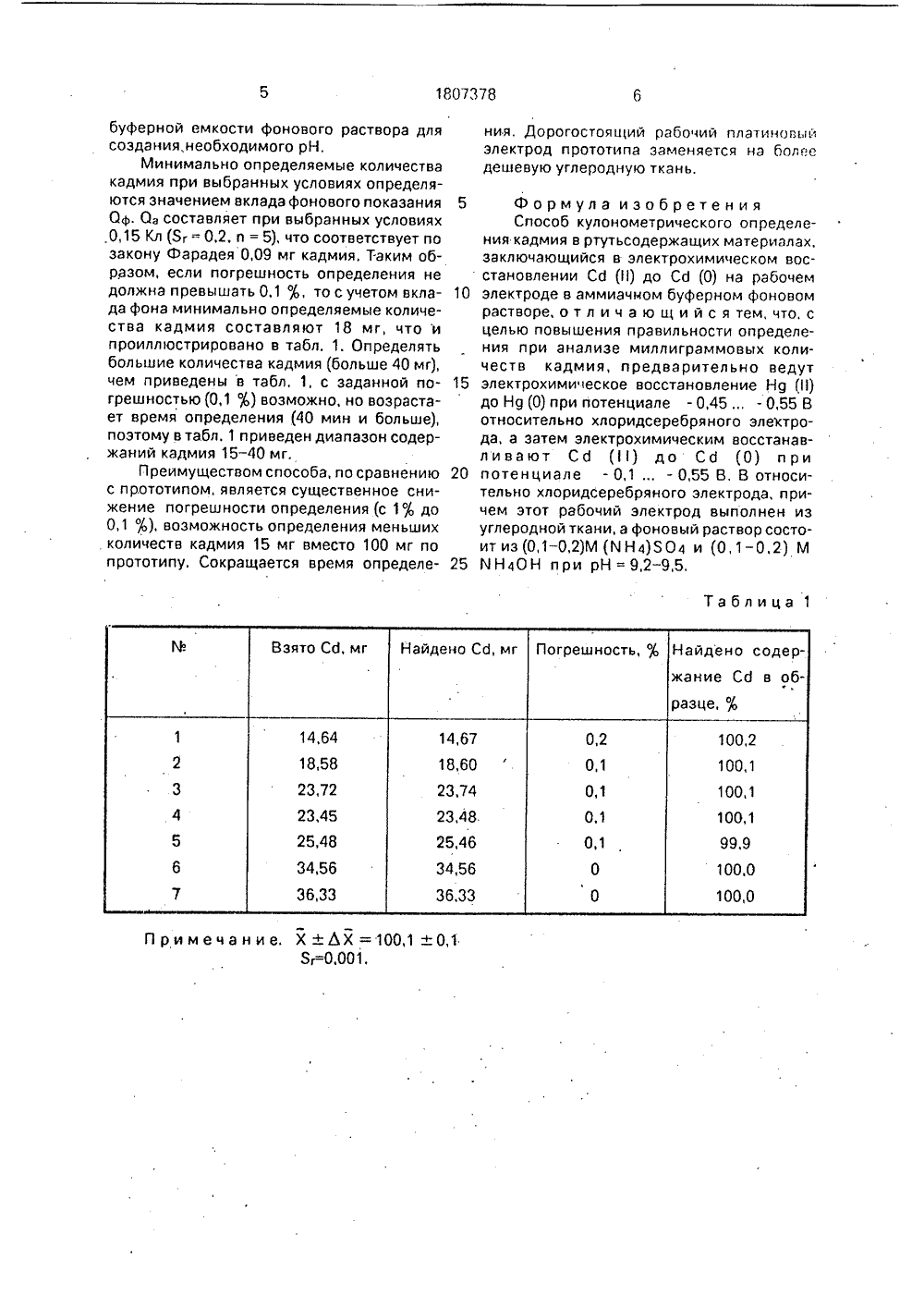
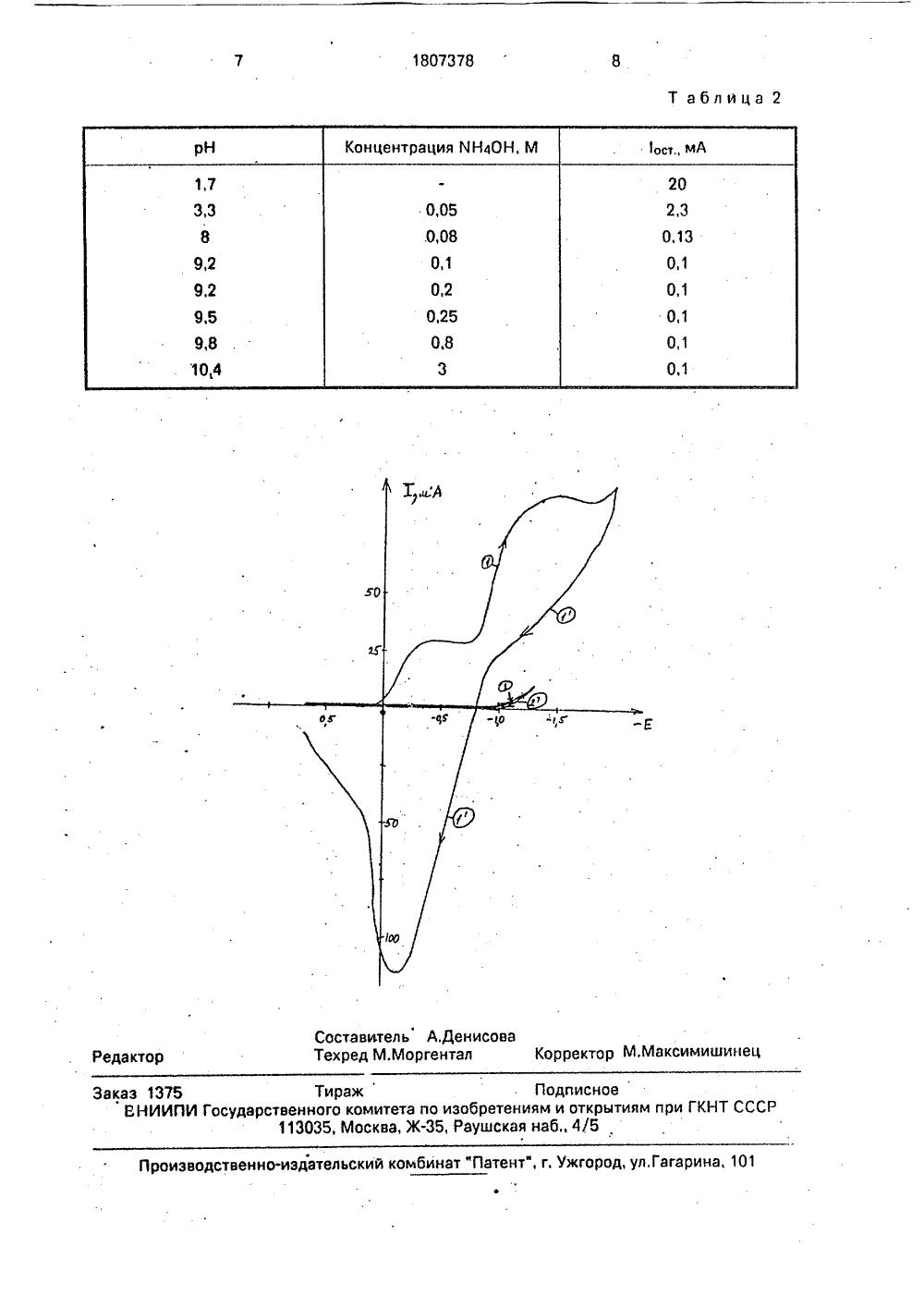
., Саар р. 1079, Вцпзес цассг. 1957, М 8,Сс1,05 В ектроолнен аствор - 0,2)М ми- улоится к электрох , в частности к к руемом потенц ано для анализ тности полупро ГОСУДАРСТВЕ Н ЮЕ ПАТЕНТНОЕВЕДОМСТВО СССРсГОСПАТЕНТ СССР) ВТОРСКОМУ СВИДЕТЕЛЬСТВУ(46) 07.04.93. Бюл. М 13 (71) Институт геохимии мии им, В,И,Вернадско (72) А.Е,Денисова и О,Л (56) Вагео АОцсоц С 43, Ф 4, р. 607,Юзе Н/,М е 1966. 38, Р 8,(54) СПОСОБ КУЛОНОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ КАДМИЯ В РТУТЬСОДЕРЖАЩИХ МАТ,ЕРИАЛАХ Изобретение относ ческим методам анализа нометрии, при контроли и может быть использоо единений кадмия, в час никовых материалов. Цель изобретения вильности определения лиграммовых количеств Поставленная зада что по способу кулономе ления кадмия в ртутьсо лах, заключающемуся в восстановлении Ссд электроде в аммиачным. растворе предваритель мическое восстановлен при потенциале,45. но хлоридсеребряного- повышение прапри анализе милкадглил.а достигается тем, трического опредедержащих материаэлектрохимическом о Сс (О), на рабочем буферном фоновом но ведут электрохиие Н 9до Н 9 (О) - 0,55 В относительэлек 1 рода, а затем(57) Использование: электрохимические методы анализа, например кулонометрия при контролируемом потенциале, для анализа соединений кадмия, в частности полупроводниковых материалов. Сущность изобретения; предварительно ведут электрохимическое восстановление Н 9до Н 9 (О) при потенциале - 0,45- 0,55 В относительно хлоридсеребряного электрода, а затем электрохимическое восстановление Ссдо Сс (О) при потенциале - 1,0 - 1,05 В относительно хлоридсеребряного электрода, причем рабочий электрод выполнен из углеродной ткани, а фоновый электролит состоит из (0,1 - -0,2)М (КНл)504 + +(0,1 - 0,2)М ИНлОН при рН 9,2-9,5. 2 табл. электрохимически восстанавливают до Сс (О) при потенциале - 1,0 ,- относительнохлоридсеребряного э да, причем этот рабочий электрод вы из углеродной ткани, а фоновый р состоит из (0.1 - 0,2)М (ННл)2 ЯОл и (О, КНлОН Рри рН 9,2-9,5,Применение электрода из углероднои ткани известно для кулонометрического определения ртути, но для кулонометрического определения кадмия такой электрод не пригленялся, Была выбрана покрытая пироуглеродом углеродная ткань, обладающая- хорошей электропроводностью, механической прочностью, способностью к регенерации, а также имеющая малые фоновые токи в отрицательной области потенциалов, в которой определяется кадмий.В качестве фонового электролита был в ыРан (0,1 -0,2) М раствор (ч Н л)23 О+ (0,1- 0,2)М КН ОН (рН 9,5), Кислые среды не использовались в связи с восстановлением+Н -ионов фонового электролита в области восстановления Сб, что дало бы высокое2+значение вклада фона в аналитический сигнал, Ион аммония необходим для образования аммиачных комплексов с Сг и, таким образом, предотвращения образования осадка Сг 1(ОН)2 при работе с рас-,вором с высоким значением рН, Было обнаружено, что нитрат-ион мешает определению Сг в присутствии ионов аммония, поэтому после вскрытия пробы в конц. НИОз проводилось последующее удаление нитрат-ионов выпариванием с серной кислотой,На чертеже представлены вольтамперные кривые раствора ионов Нц (1) и Сг (11) при катодной (кривая 1) и анодной (кривая 1) поляризации электрода, Кривые сняты на фоне 0,1 М (МН 4)2504 и 0,1 У МН 4 ОН, рН = 9,5. На чертеже приведены также вольтамперные кривые фонового раствора (кривые 2, 2). Исходя иэ приведенных вольтамперных кривых был выбран потенциал для проведения предварительного электрохимического восстановления Нц ( 1), равный - 0,45-0,55 В, и потенциал для кулонометрического определения кадмия, равный - 1,0- 1,05 В, При больших значениях потенциала при определении Сс (11) существенно возрастает вклад фонового показания,Согласно потенциалам минимума тока нэ анодной ветви кривой 2 электрохимическую очистку электрода от Сс (О) и Нц (О) рекомендуется проводить при потенциале 0,5-0,6 В.П р и м е р, Кулонометрическое определение кадмия вели на рабочем электроде из покрытой пироуглеродом ткани марки ТМП с видимой поверхностью 12 см, Выходной2контакт рабочего электрода с потенциостатом осуществляли при помощи нитей из той же ткани, которыми прошивалась ткань электрода, Выходящие концы нитей переплетали с никелевой проволокой и убирали в тефлоновый шланг, конец которого парэфинировали, Использовали трехэлектродную ячейку с анодным и катодным отделениями, разделенными пористой диафрагмой. Вспомогательный электрод - платиновая сетка; электрод сравнения - насыщенный хлоридсеребряный электрод. Общий обьем раствора в рабочем отделении 15 мл.Раствор освобождался от кислорода воздуха и перемешивался инертным газом, Заданный потенциал поддерживался по 45 ученные в условиях эксперимента, описанных в примере, показывают, что для 50 55 5 10 15 20 25 30 35 40 тенциостатом ПМ, Количество электричества определяли с помощью интегратора тока ИП,Растворение металлического кадмия и металлической ртути проводят в концентрированной НМОз с последующим удалением нитрат-ионов упариванием с серной кислотой на водяной бане,Определение начинали с регистрации величины фона при выбранных потенциалах для введения поправки на вклад фонового показания, который составляет при выбранных условиях 0,1 Кл,Взвешенную аликвотную часть анализируемого раствора (2 г) вводили в ячейку, приливали фоновый раствор до объема 15 мл, продували аргон в течение 15 мин. Затем проводили восстановление ионов ртути катодной поляризацией при потенциале,5 В относительно хлоридсеребряного электрода в течение 20 мин до остаточного тока 0,03 мА.В том же растворе проводили восстановление ионов кадмия катодной поляризацией электрода при потенциале - 1,0 В в течение 30 мин до остаточного тока 0,08 мА, фиксируют количество электричества с помощью интегратора, вводили поправку на вклад фона и рассчитывали содержание кадмия в растворе,Результаты кулонометрического определения кадмия в присутствии ртути по предложенной методике приведены в табл.1,.из которой видна правильность и хорошая воспроизводимость определений.Правильность определения улучшается с уменьшением вклада фонового показания, который зависит от величины остаточного тока, рН раствора и соответственно концентрация ИНОН выбрана такой, чтобы вклад фонового показания был минимальным,В табл. 2 представлены данные по оптимальности выбора концентрацииКНЯЖОН.Данные, приведенные в табл. 2 и полсоблюдения этих условий рН раствора должно быть больше 8 и соответственно концентрация МН 4 ОН больше 0,1 М. Но с ростом рН потенциал полуволны Е 1(2 кадмия сдвигается в отрицательную область потенциалов. Область предельного тока, в которой проводится определения, также сдвигается в отрицательную область потенциалов, Поэтому оптимальным для определения кадмия является диапазон рН 9,2-9,5 и соответственно концентрация МН 4 ОН 0,1 - 0,25 М.Диапазон содержаний (МН 4)2304 0,1-0,2 М выбран достаточным для поддерживания1807378 5 Формула изобретенияСпособ кулонометрического определения кадмия в ртутьсодержащих материалах,заключающийся в электрохимическом восстановлении Сд (И) до Сд (О) на рабочем10 электроде в аммиачном буферном фоновомрастворе, отл и ч а ю щи й с я тем, что, сцелью повышения правильности определения при анализе миллиграммовых количеств кадмия, предварительно ведут15 электрохимическое восстановление Н 9 (1)до Нц (О) при потенциале - 0,45 . - 0,55 Вотносительно хлоридсеребряного электрода, а затем электрохимическим восстанавливают Сб (1) до Сц (О) и ри20 потенциале - 0,1- 0,55 В, В относительно хлоридсеребряного электрода, причем этот рабочий электрод выполнен изуглеродной ткани, а фоновый раствор состоит из (0,1 - 0,2)М (МНа)304 и (0,1 - 0,2) М25 й Н 40 Н при рН = 9,2 - 9,5,Таблица 1 П р и м е ч а н и е. Х + ЬХ = 100,1 . 0,13 г 0,001. буферной емкости фонового раствора для создания, необходимого рН.Минимально определяемые количества кадмия при выбранных условиях определяются значением вклада фонового показания Оф. Оз составляет при выбранных условиях 0,15 Кл (Яг =- 0,2, и = 5), что соответствует по закону Фарадея 0,09 мг кадмия, Таким образом, если погрешность определения не должна превышать 0,1, то с учетом вклада фона минимально определяемые количества кадмия составляют 18 мг, что и проиллюстрировано в табл. 1, Определять большие количества кадмия (больше 40 мг), чем приведены в табл. 1, с заданной погрешностью(0,1) возможно, но возрастает время определения (40 мин и больше), поэтому в табл. 1 приведен диапазон содержаний кадмия 15 - 40 мг.Преимуществом способа, по сравнению с прототипом, является существенное снижение погрешности определения (с 1 до 0,1), возможность определения меньших количеств кадмия 15 мг вместо 100 мг по прототипу. Сокращается время определения. Дорогостоящий рабочий платиновыйэлектрод прототипа заменяется на болеедешевую углеродную ткань.1807378 Т аблица 2 эктор зводственно-издательский комбинат "Патент", г. Ужгород, ул.Гагарина, 101 Заказ 1375 БНИИПИ Госуд Составитель А.ДенисоваТехред М.Моргентал Корректор М,Максимишинец Тираж Подписноетвенного комитета по изобретениям и открытиям при ГКНТ С 113035, Москва, Ж, Раушская наб., 4/5
СмотретьЗаявка
4954748, 24.05.1991
ИНСТИТУТ ГЕОХИМИИ И АНАЛИТИЧЕСКОЙ ХИМИИ ИМ. В. И. ВЕРНАДСКОГО
ДЕНИСОВА АННА ЕВГЕНЬЕВНА, КАБАНОВА ОКТЯБРИНА ЛЬВОВНА
МПК / Метки
МПК: G01N 27/42
Метки: кадмия, кулонометрического, материалах, ртутьсодержащих
Опубликовано: 07.04.1993
Код ссылки
<a href="https://patents.su/4-1807378-sposob-kulonometricheskogo-opredeleniya-kadmiya-v-rtutsoderzhashhikh-materialakh.html" target="_blank" rel="follow" title="База патентов СССР">Способ кулонометрического определения кадмия в ртутьсодержащих материалах</a>